+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0552 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | human m-AAA protease AFG3L2, substrate-bound | |||||||||
 マップデータ マップデータ | Composite map containing the stitched maps of the ATPase domains from subunits B-E, the ATPase domains from subunits A & F, and the protease domains | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | AAA+ / ATPase / protease / mitochondria / protein quality control / neurodegeneration / inner membrane / AFG3L2 / m/AAA protease / translocase | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cellular response to glutathione / m-AAA complex / mitochondrial protein processing / regulation of calcium import into the mitochondrion / mitochondrial protein quality control / Processing of SMDT1 / mitochondrial calcium ion homeostasis / membrane protein proteolysis / calcium import into the mitochondrion / cristae formation ...cellular response to glutathione / m-AAA complex / mitochondrial protein processing / regulation of calcium import into the mitochondrion / mitochondrial protein quality control / Processing of SMDT1 / mitochondrial calcium ion homeostasis / membrane protein proteolysis / calcium import into the mitochondrion / cristae formation / righting reflex / 加水分解酵素; 酸無水物に作用 / nerve development / muscle cell development / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; その他のペプチターゼ / mitochondrial fusion / neuromuscular junction development / ATP-dependent peptidase activity / protein autoprocessing / protein maturation / regulation of multicellular organism growth / myelination / axonogenesis / Mitochondrial protein degradation / protein catabolic process / protein processing / metalloendopeptidase activity / metallopeptidase activity / unfolded protein binding / mitochondrial inner membrane / ATP hydrolysis activity / mitochondrion / proteolysis / zinc ion binding / ATP binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
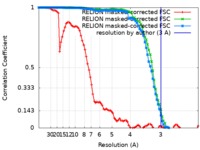
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.0 Å | |||||||||
 データ登録者 データ登録者 | Lander GC / Puchades C | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2019 ジャーナル: Mol Cell / 年: 2019タイトル: Unique Structural Features of the Mitochondrial AAA+ Protease AFG3L2 Reveal the Molecular Basis for Activity in Health and Disease. 著者: Cristina Puchades / Bojian Ding / Albert Song / R Luke Wiseman / Gabriel C Lander / Steven E Glynn /  要旨: Mitochondrial AAA+ quality-control proteases regulate diverse aspects of mitochondrial biology through specialized protein degradation, but the underlying mechanisms of these enzymes remain poorly ...Mitochondrial AAA+ quality-control proteases regulate diverse aspects of mitochondrial biology through specialized protein degradation, but the underlying mechanisms of these enzymes remain poorly defined. The mitochondrial AAA+ protease AFG3L2 is of particular interest, as genetic mutations localized throughout AFG3L2 are linked to diverse neurodegenerative disorders. However, a lack of structural data has limited our understanding of how mutations impact enzymatic function. Here, we used cryoelectron microscopy (cryo-EM) to determine a substrate-bound structure of the catalytic core of human AFG3L2. This structure identifies multiple specialized structural features that integrate with conserved motifs required for ATP-dependent translocation to unfold and degrade targeted proteins. Many disease-relevant mutations localize to these unique structural features of AFG3L2 and distinctly influence its activity and stability. Our results provide a molecular basis for neurological phenotypes associated with different AFG3L2 mutations and establish a structural framework to understand how different members of the AAA+ superfamily achieve specialized biological functions. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0552.map.gz emd_0552.map.gz | 5.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0552-v30.xml emd-0552-v30.xml emd-0552.xml emd-0552.xml | 30.8 KB 30.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_0552_fsc_1.xml emd_0552_fsc_1.xml emd_0552_fsc_2.xml emd_0552_fsc_2.xml emd_0552_fsc_3.xml emd_0552_fsc_3.xml | 8.6 KB 8.6 KB 8.6 KB | 表示 表示 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_0552.png emd_0552.png | 331.6 KB | ||
| Filedesc metadata |  emd-0552.cif.gz emd-0552.cif.gz | 7.4 KB | ||
| その他 |  emd_0552_additional_1.map.gz emd_0552_additional_1.map.gz emd_0552_additional_2.map.gz emd_0552_additional_2.map.gz emd_0552_additional_3.map.gz emd_0552_additional_3.map.gz emd_0552_additional_4.map.gz emd_0552_additional_4.map.gz emd_0552_half_map_1.map.gz emd_0552_half_map_1.map.gz emd_0552_half_map_2.map.gz emd_0552_half_map_2.map.gz | 7.3 MB 7.3 MB 7.4 MB 7.4 MB 7.3 MB 7.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0552 http://ftp.pdbj.org/pub/emdb/structures/EMD-0552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0552 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0552_validation.pdf.gz emd_0552_validation.pdf.gz | 832.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0552_full_validation.pdf.gz emd_0552_full_validation.pdf.gz | 832.4 KB | 表示 | |
| XML形式データ |  emd_0552_validation.xml.gz emd_0552_validation.xml.gz | 8.5 KB | 表示 | |
| CIF形式データ |  emd_0552_validation.cif.gz emd_0552_validation.cif.gz | 9.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0552 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0552 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0552 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0552 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0552.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0552.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Composite map containing the stitched maps of the ATPase domains from subunits B-E, the ATPase domains from subunits A & F, and the protease domains | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.15 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: ATPase domains from subunits B-E half map 1
| ファイル | emd_0552_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ATPase domains from subunits B-E half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: ATPase domains from subunits B-E half map 2
| ファイル | emd_0552_additional_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ATPase domains from subunits B-E half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: ATPase domains from subunits A & F half map 2
| ファイル | emd_0552_additional_3.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ATPase domains from subunits A & F half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: ATPase domains from subunits A & F half map 2
| ファイル | emd_0552_additional_4.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ATPase domains from subunits A & F half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Protease domains half map 1
| ファイル | emd_0552_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Protease domains half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Protease domains half map 2
| ファイル | emd_0552_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Protease domains half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : AFG3L2
| 全体 | 名称: AFG3L2 |
|---|---|
| 要素 |
|
-超分子 #1: AFG3L2
| 超分子 | 名称: AFG3L2 / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 詳細: Soluble domains of the AFG3L2, comprising the AAA+ ATPase and protease domains. |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 360 KDa |
-分子 #1: AFG3-like protein 2
| 分子 | 名称: AFG3-like protein 2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO EC番号: 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; その他のペプチターゼ |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 58.331629 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SNARRGPAGI GRTGRGMGGL FSVGETTAKV LKDEIDVKFK DVAGCEEAKL EIMEFVNFLK NPKQYQDLGA KIPKGAILTG PPGTGKTLL AKATAGEANV PFITVSGSEF LEMFVGVGPA RVRDLFALAR KNAPCILFID QIDAVGRKRG RGNFGGQSEQ E NTLNQLLV ...文字列: SNARRGPAGI GRTGRGMGGL FSVGETTAKV LKDEIDVKFK DVAGCEEAKL EIMEFVNFLK NPKQYQDLGA KIPKGAILTG PPGTGKTLL AKATAGEANV PFITVSGSEF LEMFVGVGPA RVRDLFALAR KNAPCILFID QIDAVGRKRG RGNFGGQSEQ E NTLNQLLV EMDGFNTTTN VVILAGTNRP DILDPALLRP GRFDRQIFIG PPDIKGRASI FKVHLRPLKL DSTLEKDKLA RK LASLTPG FSGADVANVC NEAALIAARH LSDSINQKHF EQAIERVIGG LEKKTQVLQP EEKKTVAYHQ AGHAVAGWYL EHA DPLLKV SIIPRGKGLG YAQYLPKEQY LYTKEQLLDR MCMTLGGRVS EEIFFGRITT GAQDDLRKVT QSAYAQIVQF GMNE KVGQI SFDLPRQGDM VLEKPYSEAT ARLIDDEVRI LINDAYKRTV ALLTEKKADV EKVALLLLEK EVLDKNDMVE LLGPR PFAE KSTYEEFVEG TGSLDEDTSL PEGLKDWNKE REKEKEEPPG EKVAN UniProtKB: Mitochondrial inner membrane m-AAA protease component AFG3L2 |
-分子 #2: Substrate
| 分子 | 名称: Substrate / タイプ: protein_or_peptide / ID: 2 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 799.871 Da |
| 組換発現 | 生物種:  |
| 配列 | 文字列: AAAAAAAAAA A |
-分子 #3: ZINC ION
| 分子 | 名称: ZINC ION / タイプ: ligand / ID: 3 / コピー数: 6 / 式: ZN |
|---|---|
| 分子量 | 理論値: 65.409 Da |
-分子 #4: PHOSPHOAMINOPHOSPHONIC ACID-ADENYLATE ESTER
| 分子 | 名称: PHOSPHOAMINOPHOSPHONIC ACID-ADENYLATE ESTER / タイプ: ligand / ID: 4 / コピー数: 3 / 式: ANP |
|---|---|
| 分子量 | 理論値: 506.196 Da |
| Chemical component information |  ChemComp-ANP: |
-分子 #5: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 5 / コピー数: 3 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #6: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 6 / コピー数: 1 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
詳細: DTT and ATP were added fresh before sample preparation | ||||||||||||||||||
| グリッド | モデル: Quantifoil, UltrAuFoil, R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 時間: 6 sec. / 前処理 - 雰囲気: OTHER 詳細: Grids were plasma cleaned using a Solarus plasma cleaner (Gatan, Inc.). | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 278 K / 装置: FEI VITROBOT MARK III 詳細: Sample was blotted for 3 seconds using Whatman No. 1 filter paper immediately prio to plunge-freezing.. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI ARCTICA |
|---|---|
| 温度 | 最低: 100.0 K / 最高: 100.0 K |
| アライメント法 | Coma free - Residual tilt: 0.07 mrad |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3710 pixel / デジタル化 - サイズ - 縦: 3838 pixel / デジタル化 - 画像ごとのフレーム数: 1-30 / 撮影したグリッド数: 5 / 実像数: 5707 / 平均露光時間: 7.0 sec. / 平均電子線量: 40.0 e/Å2 / 詳細: Data collected with Leginon |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 倍率(補正後): 43478 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 18.0 µm / 最小 デフォーカス(公称値): 8.0 µm / 倍率(公称値): 36000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー













 Z
Z Y
Y X
X