+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1653 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Aquareovirus capsid proteins. | |||||||||
 マップデータ マップデータ | VP1 protein | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  aquareovirus / aquareovirus /  capsid proteins (カプシド) / grass carp reovirus capsid proteins (カプシド) / grass carp reovirus | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報host cell surface binding / viral inner capsid / viral outer capsid / permeabilization of host organelle membrane involved in viral entry into host cell / symbiont entry into host cell via permeabilization of inner membrane / 7-methylguanosine mRNA capping /  カプシド / カプシド /  mRNA guanylyltransferase activity / mRNA 5'-cap (guanine-N7-)-methyltransferase activity / mRNA guanylyltransferase activity / mRNA 5'-cap (guanine-N7-)-methyltransferase activity /  RNA helicase activity ...host cell surface binding / viral inner capsid / viral outer capsid / permeabilization of host organelle membrane involved in viral entry into host cell / symbiont entry into host cell via permeabilization of inner membrane / 7-methylguanosine mRNA capping / RNA helicase activity ...host cell surface binding / viral inner capsid / viral outer capsid / permeabilization of host organelle membrane involved in viral entry into host cell / symbiont entry into host cell via permeabilization of inner membrane / 7-methylguanosine mRNA capping /  カプシド / カプシド /  mRNA guanylyltransferase activity / mRNA 5'-cap (guanine-N7-)-methyltransferase activity / mRNA guanylyltransferase activity / mRNA 5'-cap (guanine-N7-)-methyltransferase activity /  RNA helicase activity / RNA helicase activity /  hydrolase activity / hydrolase activity /  ヘリカーゼ / GTP binding / ヘリカーゼ / GTP binding /  ATP binding / ATP binding /  metal ion binding metal ion binding類似検索 - 分子機能 | |||||||||
| 生物種 |   Grass carp reovirus (ウイルス) Grass carp reovirus (ウイルス) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 4.5 Å クライオ電子顕微鏡法 / 解像度: 4.5 Å | |||||||||
 データ登録者 データ登録者 | Cheng L / Zhu J / Hui WH / Zhang X / Honig B / Fang Q / Zhou ZH | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2010 ジャーナル: J Mol Biol / 年: 2010タイトル: Backbone model of an aquareovirus virion by cryo-electron microscopy and bioinformatics. 著者: Lingpeng Cheng / Jiang Zhu / Wong Hoi Hui / Xiaokang Zhang / Barry Honig / Qin Fang / Z Hong Zhou /  要旨: Grass carp reovirus (GCRV) is a member of the aquareovirus genus in the Reoviridae family and has a capsid with two shells-a transcription-competent core surrounded by a coat. We report a near-atomic- ...Grass carp reovirus (GCRV) is a member of the aquareovirus genus in the Reoviridae family and has a capsid with two shells-a transcription-competent core surrounded by a coat. We report a near-atomic-resolution reconstruction of the GCRV virion by cryo-electron microscopy and single-particle reconstruction. A backbone model of the GCRV virion, including seven conformers of the five capsid proteins making up the 1500 molecules in both the core and the coat, was derived using cryo-electron microscopy density-map-constrained homology modeling and refinement. Our structure clearly showed that the amino-terminal segment of core protein VP3B forms an approximately 120-A-long alpha-helix-rich extension bridging across the icosahedral 2-fold-symmetry-related molecular interface. The presence of this unique structure across this interface and the lack of an external cementing molecule at this location in GCRV suggest a stabilizing role of this extended amino-terminal density. Moreover, part of this amino-terminal extension becomes invisible in the reconstruction of transcription-competent core particles, suggesting its involvement in endogenous viral RNA transcription. Our structure of the VP1 turret represents its open state, and comparison with its related structures at the closed state suggests hinge-like domain movements associated with the mRNA-capping machinery. Overall, this first backbone model of an aquareovirus virion provides a wealth of structural information for understanding the structural basis of GCRV assembly and transcription. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1653.map.gz emd_1653.map.gz | 753.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1653-v30.xml emd-1653-v30.xml emd-1653.xml emd-1653.xml | 7.9 KB 7.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  em-1653.png em-1653.png | 1023.3 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1653 http://ftp.pdbj.org/pub/emdb/structures/EMD-1653 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1653 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1653 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1653.map.gz / 形式: CCP4 / 大きさ: 1.5 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1653.map.gz / 形式: CCP4 / 大きさ: 1.5 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | VP1 protein | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 これらの図は立方格子座標系で作成されたものです | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.9716 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
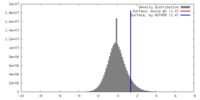
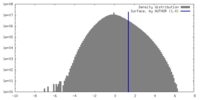
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Grass carp reovirus
| 全体 | 名称:   Grass carp reovirus (ウイルス) Grass carp reovirus (ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1000: Grass carp reovirus
| 超分子 | 名称: Grass carp reovirus / タイプ: sample / ID: 1000 / 詳細: The sample is Grass carp reovirus virion / Number unique components: 1 |
|---|
-超分子 #1: Grass carp reovirus
| 超分子 | 名称: Grass carp reovirus / タイプ: virus / ID: 1 / Name.synonym: GCRV / NCBI-ID: 128987 / 生物種: Grass carp reovirus / ウイルスタイプ: VIRION / ウイルス・単離状態: SEROTYPE / ウイルス・エンベロープ: No / ウイルス・中空状態: No / Syn species name: GCRV |
|---|---|
| 宿主 | 別称: VERTEBRATES |
| ウイルス殻 | Shell ID: 1 / 直径: 880 Å / T番号(三角分割数): 13 |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL |
|---|---|
| 緩衝液 | 詳細: PBS |
| 凍結 | 凍結剤: ETHANE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.3 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 93000 Bright-field microscopy / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.3 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 93000 |
| 試料ステージ | 試料ホルダー: FEI / 試料ホルダーモデル: PHILIPS ROTATION HOLDER |
| 撮影 | カテゴリ: CCD / フィルム・検出器のモデル: GENERIC CCD / 実像数: 4000 / 平均電子線量: 20 e/Å2 |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: Each micrograph |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: I (正20面体型対称 ) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 4.5 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: IMIRS / 使用した粒子像数: 15000 ) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 4.5 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: IMIRS / 使用した粒子像数: 15000 |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)