+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 5kem | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | EBOV sGP in complex with variable Fab domains of IgGs c13C6 and BDBV91 | ||||||||||||
 要素 要素 |
| ||||||||||||
 キーワード キーワード | VIRAL PROTEIN/IMMUNE SYSTEM / Ebola virus secreted glycoprotein / sGP / antibodies / VIRAL PROTEIN-IMMUNE SYSTEM complex | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報symbiont-mediated killing of host cell / host cell endoplasmic reticulum / viral budding from plasma membrane / clathrin-dependent endocytosis of virus by host cell / symbiont-mediated-mediated suppression of host tetherin activity / host cell cytoplasm / entry receptor-mediated virion attachment to host cell / symbiont-mediated suppression of host innate immune response / membrane raft / fusion of virus membrane with host endosome membrane ...symbiont-mediated killing of host cell / host cell endoplasmic reticulum / viral budding from plasma membrane / clathrin-dependent endocytosis of virus by host cell / symbiont-mediated-mediated suppression of host tetherin activity / host cell cytoplasm / entry receptor-mediated virion attachment to host cell / symbiont-mediated suppression of host innate immune response / membrane raft / fusion of virus membrane with host endosome membrane / lipid binding / viral envelope / symbiont entry into host cell / host cell plasma membrane / virion membrane / extracellular region / identical protein binding 類似検索 - 分子機能 | ||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 5.5 Å | ||||||||||||
 データ登録者 データ登録者 | Pallesen, J. / Murin, C.D. / de Val, N. / Cottrell, C.A. / Hastie, K.M. / Turner, H.L. / Fusco, M.L. / Flyak, A.I. / Zeitlin, L. / Crowe Jr., J.E. ...Pallesen, J. / Murin, C.D. / de Val, N. / Cottrell, C.A. / Hastie, K.M. / Turner, H.L. / Fusco, M.L. / Flyak, A.I. / Zeitlin, L. / Crowe Jr., J.E. / Andersen, K.G. / Saphire, E.O. / Ward, A.B. | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
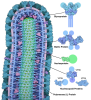
 引用 引用 |  ジャーナル: Nat Microbiol / 年: 2016 ジャーナル: Nat Microbiol / 年: 2016タイトル: Structures of Ebola virus GP and sGP in complex with therapeutic antibodies. 著者: Jesper Pallesen / Charles D Murin / Natalia de Val / Christopher A Cottrell / Kathryn M Hastie / Hannah L Turner / Marnie L Fusco / Andrew I Flyak / Larry Zeitlin / James E Crowe / Kristian G ...著者: Jesper Pallesen / Charles D Murin / Natalia de Val / Christopher A Cottrell / Kathryn M Hastie / Hannah L Turner / Marnie L Fusco / Andrew I Flyak / Larry Zeitlin / James E Crowe / Kristian G Andersen / Erica Ollmann Saphire / Andrew B Ward /  要旨: The Ebola virus (EBOV) GP gene encodes two glycoproteins. The major product is a soluble, dimeric glycoprotein (sGP) that is secreted abundantly. Despite the abundance of sGP during infection, little ...The Ebola virus (EBOV) GP gene encodes two glycoproteins. The major product is a soluble, dimeric glycoprotein (sGP) that is secreted abundantly. Despite the abundance of sGP during infection, little is known regarding its structure or functional role. A minor product, resulting from transcriptional editing, is the transmembrane-anchored, trimeric viral surface glycoprotein (GP). GP mediates attachment to and entry into host cells, and is the intended target of antibody therapeutics. Because large portions of sequence are shared between GP and sGP, it has been hypothesized that sGP may potentially subvert the immune response or may contribute to pathogenicity. In this study, we present cryo-electron microscopy structures of GP and sGP in complex with GP-specific and GP/sGP cross-reactive antibodies undergoing human clinical trials. The structure of the sGP dimer presented here, in complex with both an sGP-specific antibody and a GP/sGP cross-reactive antibody, permits us to unambiguously assign the oligomeric arrangement of sGP and compare its structure and epitope presentation to those of GP. We also provide biophysical evaluation of naturally occurring GP/sGP mutations that fall within the footprints identified by our high-resolution structures. Taken together, our data provide a detailed and more complete picture of the accessible Ebolavirus glycoprotein landscape and a structural basis to evaluate patient and vaccine antibody responses towards differently structured products of the GP gene. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  5kem.cif.gz 5kem.cif.gz | 269.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb5kem.ent.gz pdb5kem.ent.gz | 217.6 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  5kem.json.gz 5kem.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  5kem_validation.pdf.gz 5kem_validation.pdf.gz | 1 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  5kem_full_validation.pdf.gz 5kem_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  5kem_validation.xml.gz 5kem_validation.xml.gz | 47.6 KB | 表示 | |
| CIF形式データ |  5kem_validation.cif.gz 5kem_validation.cif.gz | 72 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ke/5kem https://data.pdbj.org/pub/pdb/validation_reports/ke/5kem ftp://data.pdbj.org/pub/pdb/validation_reports/ke/5kem ftp://data.pdbj.org/pub/pdb/validation_reports/ke/5kem | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: 抗体 | 分子量: 11578.873 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  #2: 抗体 | 分子量: 13652.312 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  Homo sapiens (ヒト) Homo sapiens (ヒト)#3: 抗体 | 分子量: 13169.679 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  #4: 抗体 | 分子量: 11611.877 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  #5: タンパク質 | 分子量: 25822.863 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  株: Mayinga-76 / 遺伝子: GP 発現宿主:  参照: UniProt: Q05320 Has protein modification | Y | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Ebola virus dimeric secreted glycoprotein in complex with IgG c13C6 and BDBV91 Fabs タイプ: COMPLEX / Entity ID: all / 由来: MULTIPLE SOURCES |
|---|---|
| 分子量 | 値: 0.27 MDa / 実験値: NO |
| 由来(天然) | 生物種:  |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.4 |
| 緩衝液成分 | 名称: 1xTBS |
| 試料 | 濃度: 4 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 400 divisions/in. / グリッドのタイプ: C-flat-2/2 4C |
| 急速凍結 | 装置: HOMEMADE PLUNGER / 凍結剤: ETHANE / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 22500 X / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1000 nm / Cs: 2.7 mm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER 最高温度: 77 K / 最低温度: 77 K |
| 撮影 | 平均露光時間: 10 sec. / 電子線照射量: 57 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 撮影したグリッド数: 1 / 実像数: 2048 |
| 画像スキャン | 動画フレーム数/画像: 50 / 利用したフレーム数/画像: 1-50 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C2 (2回回転対称) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 5.5 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 39000 / クラス平均像の数: 2 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: FLEXIBLE FIT / 空間: REAL / Target criteria: EMRinger 詳細: Model building and refinement were conducted using a combination of software programs. The refinement target was optimizing using the MolProbity score while maintaining a high (good) EMRinger score. |
 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj