| Entry | Database: PDB / ID: 5igo
|
|---|
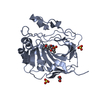
| Title | WD40 domain of Arabidopsis thaliana E3 Ubiquitin Ligase COP1 in complex with peptide from Trib1 |
|---|
 Components Components | - E3 ubiquitin-protein ligase COP1
- Tribbles homolog 1
|
|---|
 Keywords Keywords | Hydrolase/Peptide / WD40 domain E3 ligase / Hydrolase-Peptide Complex |
|---|
| Function / homology |  Function and homology information Function and homology information
ubiquitin-protein transferase regulator activity / positive regulation of eosinophil differentiation / anthocyanin-containing compound metabolic process / shade avoidance / positive regulation of flavonoid biosynthetic process / skotomorphogenesis / photoperiodism, flowering / red, far-red light phototransduction / regulation of MAP kinase activity / negative regulation of neutrophil differentiation ...ubiquitin-protein transferase regulator activity / positive regulation of eosinophil differentiation / anthocyanin-containing compound metabolic process / shade avoidance / positive regulation of flavonoid biosynthetic process / skotomorphogenesis / photoperiodism, flowering / red, far-red light phototransduction / regulation of MAP kinase activity / negative regulation of neutrophil differentiation / regulation of stomatal movement / photomorphogenesis / negative regulation of smooth muscle cell migration / positive regulation of macrophage differentiation / nuclear ubiquitin ligase complex / negative regulation of lipopolysaccharide-mediated signaling pathway / entrainment of circadian clock / NGF-stimulated transcription / mitogen-activated protein kinase kinase binding / response to UV-B / negative regulation of JNK cascade / Cul4-RING E3 ubiquitin ligase complex / protein kinase inhibitor activity / transcription regulator inhibitor activity / negative regulation of MAPK cascade / negative regulation of smooth muscle cell proliferation / RING-type E3 ubiquitin transferase / ubiquitin-protein transferase activity / ubiquitin protein ligase activity / positive regulation of proteasomal ubiquitin-dependent protein catabolic process / response to lipopolysaccharide / RNA polymerase II-specific DNA-binding transcription factor binding / proteasome-mediated ubiquitin-dependent protein catabolic process / nuclear body / protein ubiquitination / DNA repair / ubiquitin protein ligase binding / protein kinase binding / negative regulation of transcription by RNA polymerase II / zinc ion binding / identical protein binding / nucleus / cytoplasm / cytosolSimilarity search - Function Tribbles homologue 1 / Pseudokinase tribbles family/serine-threonine-protein kinase 40 / E3 ubiquitin-protein ligase COP1 / Zinc finger, C3HC4 type (RING finger) / Zinc finger, RING-type, conserved site / Zinc finger RING-type signature. / YVTN repeat-like/Quinoprotein amine dehydrogenase / Ring finger / 7 Propeller / Methylamine Dehydrogenase; Chain H ...Tribbles homologue 1 / Pseudokinase tribbles family/serine-threonine-protein kinase 40 / E3 ubiquitin-protein ligase COP1 / Zinc finger, C3HC4 type (RING finger) / Zinc finger, RING-type, conserved site / Zinc finger RING-type signature. / YVTN repeat-like/Quinoprotein amine dehydrogenase / Ring finger / 7 Propeller / Methylamine Dehydrogenase; Chain H / Zinc finger RING-type profile. / Zinc finger, RING-type / WD domain, G-beta repeat / Zinc finger, RING/FYVE/PHD-type / WD40 repeat, conserved site / Trp-Asp (WD) repeats signature. / Protein kinase domain / Trp-Asp (WD) repeats profile. / Trp-Asp (WD) repeats circular profile. / WD40 repeats / WD40 repeat / Serine/Threonine protein kinases, catalytic domain / WD40-repeat-containing domain superfamily / WD40/YVTN repeat-like-containing domain superfamily / Protein kinase domain profile. / Protein kinase domain / Protein kinase-like domain superfamily / Mainly BetaSimilarity search - Domain/homology |
|---|
| Biological species |   Arabidopsis thaliana (thale cress) Arabidopsis thaliana (thale cress)
 Homo sapiens (human) Homo sapiens (human) |
|---|
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.6 Å MOLECULAR REPLACEMENT / Resolution: 1.6 Å |
|---|
 Authors Authors | Uljon, S. / Blacklow, S.C. |
|---|
 Citation Citation |  Journal: Structure / Year: 2016 Journal: Structure / Year: 2016
Title: Structural Basis for Substrate Selectivity of the E3 Ligase COP1.
Authors: Uljon, S. / Xu, X. / Durzynska, I. / Stein, S. / Adelmant, G. / Marto, J.A. / Pear, W.S. / Blacklow, S.C. |
|---|
| History | | Deposition | Feb 28, 2016 | Deposition site: RCSB / Processing site: RCSB |
|---|
| Revision 1.0 | Apr 20, 2016 | Provider: repository / Type: Initial release |
|---|
| Revision 1.1 | May 11, 2016 | Group: Database references |
|---|
| Revision 1.2 | Jul 20, 2016 | Group: Data collection |
|---|
| Revision 1.3 | Nov 22, 2017 | Group: Derived calculations / Refinement description / Category: pdbx_struct_oper_list / software
Item: _pdbx_struct_oper_list.symmetry_operation / _software.classification |
|---|
| Revision 1.4 | Sep 27, 2023 | Group: Data collection / Database references / Refinement description
Category: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession |
|---|
|
|---|
 Yorodumi
Yorodumi Open data
Open data Basic information
Basic information Components
Components Keywords
Keywords Function and homology information
Function and homology information
 Homo sapiens (human)
Homo sapiens (human) X-RAY DIFFRACTION /
X-RAY DIFFRACTION /  SYNCHROTRON /
SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.6 Å
MOLECULAR REPLACEMENT / Resolution: 1.6 Å  Authors
Authors Citation
Citation Journal: Structure / Year: 2016
Journal: Structure / Year: 2016 Structure visualization
Structure visualization Molmil
Molmil Jmol/JSmol
Jmol/JSmol Downloads & links
Downloads & links Download
Download 5igo.cif.gz
5igo.cif.gz PDBx/mmCIF format
PDBx/mmCIF format pdb5igo.ent.gz
pdb5igo.ent.gz PDB format
PDB format 5igo.json.gz
5igo.json.gz PDBx/mmJSON format
PDBx/mmJSON format Other downloads
Other downloads https://data.pdbj.org/pub/pdb/validation_reports/ig/5igo
https://data.pdbj.org/pub/pdb/validation_reports/ig/5igo ftp://data.pdbj.org/pub/pdb/validation_reports/ig/5igo
ftp://data.pdbj.org/pub/pdb/validation_reports/ig/5igo

 Links
Links Assembly
Assembly




 Components
Components
 Trichoplusia ni (cabbage looper)
Trichoplusia ni (cabbage looper) Homo sapiens (human) / References: UniProt: Q96RU8
Homo sapiens (human) / References: UniProt: Q96RU8 X-RAY DIFFRACTION / Number of used crystals: 1
X-RAY DIFFRACTION / Number of used crystals: 1  Sample preparation
Sample preparation SYNCHROTRON / Site:
SYNCHROTRON / Site:  APS
APS  / Beamline: 24-ID-C / Wavelength: 0.97931 Å
/ Beamline: 24-ID-C / Wavelength: 0.97931 Å Processing
Processing MOLECULAR REPLACEMENT
MOLECULAR REPLACEMENT Movie
Movie Controller
Controller











 PDBj
PDBj




