| 登録情報 | データベース: PDB / ID: 5fhh
|
|---|
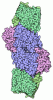
| タイトル | Structure of human Pif1 helicase domain residues 200-641 |
|---|
 要素 要素 | ATP-dependent DNA helicase PIF1 |
|---|
 キーワード キーワード | HYDROLASE / Pif1 helicase / SF1B 5'-3' DNA helicase |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
protein-DNA-RNA complex disassembly / 5'-3' DNA/RNA helicase activity / telomerase inhibitor activity / G-quadruplex DNA binding / : / DNA 5'-3' helicase / single-stranded DNA helicase activity / telomeric DNA binding / negative regulation of telomere maintenance via telomerase / mitochondrial nucleoid ...protein-DNA-RNA complex disassembly / 5'-3' DNA/RNA helicase activity / telomerase inhibitor activity / G-quadruplex DNA binding / : / DNA 5'-3' helicase / single-stranded DNA helicase activity / telomeric DNA binding / negative regulation of telomere maintenance via telomerase / mitochondrial nucleoid / Telomere Extension By Telomerase / telomere maintenance via telomerase / 5'-3' DNA helicase activity / DNA recombination / chromosome, telomeric region / DNA repair / magnesium ion binding / ATP hydrolysis activity / mitochondrion / nucleoplasm / ATP binding / nucleus類似検索 - 分子機能 : / Helicase / : / DNA helicase Pif1, 2B domain / : / LRR1 pleckstrin homology domain / DNA helicase Pif1-like / PIF1-like helicase / P-loop containing nucleoside triphosphate hydrolase類似検索 - ドメイン・相同性 ADENOSINE-5'-DIPHOSPHATE / TETRAFLUOROALUMINATE ION / ATP-dependent DNA helicase PIF1類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / 解像度: 3.6 Å シンクロトロン / 解像度: 3.6 Å |
|---|
 データ登録者 データ登録者 | Zhou, X. / Ren, W. / Bharath, S.R. / Song, H. |
|---|
 引用 引用 |  ジャーナル: Cell Rep / 年: 2016 ジャーナル: Cell Rep / 年: 2016
タイトル: Structural and Functional Insights into the Unwinding Mechanism of Bacteroides sp Pif1
著者: Zhou, X. / Ren, W. / Bharath, S.R. / Tang, X. / He, Y. / Chen, C. / Liu, Z. / Li, D. / Song, H. |
|---|
| 履歴 | | 登録 | 2015年12月22日 | 登録サイト: RCSB / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2016年3月30日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2024年11月20日 | Group: Data collection / Database references ...Data collection / Database references / Derived calculations / Structure summary
カテゴリ: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_entry_details / pdbx_modification_feature / pdbx_struct_oper_list
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession / _pdbx_struct_oper_list.symmetry_operation |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  シンクロトロン / 解像度: 3.6 Å
シンクロトロン / 解像度: 3.6 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Cell Rep / 年: 2016
ジャーナル: Cell Rep / 年: 2016 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 5fhh.cif.gz
5fhh.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb5fhh.ent.gz
pdb5fhh.ent.gz PDB形式
PDB形式 5fhh.json.gz
5fhh.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 5fhh_validation.pdf.gz
5fhh_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 5fhh_full_validation.pdf.gz
5fhh_full_validation.pdf.gz 5fhh_validation.xml.gz
5fhh_validation.xml.gz 5fhh_validation.cif.gz
5fhh_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/fh/5fhh
https://data.pdbj.org/pub/pdb/validation_reports/fh/5fhh ftp://data.pdbj.org/pub/pdb/validation_reports/fh/5fhh
ftp://data.pdbj.org/pub/pdb/validation_reports/fh/5fhh リンク
リンク 集合体
集合体


 要素
要素 Homo sapiens (ヒト) / 遺伝子: PIF1, C15orf20 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: PIF1, C15orf20 / 発現宿主: 
 X線回折
X線回折 試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  SSRF
SSRF  / ビームライン: BL17U / 波長: 1 Å
/ ビームライン: BL17U / 波長: 1 Å 解析
解析 ムービー
ムービー コントローラー
コントローラー

















 PDBj
PDBj