[English] 日本語
 Yorodumi
Yorodumi- PDB-4dgc: TRIMCyp cyclophilin domain from Macaca mulatta: cyclosporin A complex -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 4dgc | ||||||
|---|---|---|---|---|---|---|---|
| Title | TRIMCyp cyclophilin domain from Macaca mulatta: cyclosporin A complex | ||||||
 Components Components |
| ||||||
 Keywords Keywords | ISOMERASE/IMMUNOSUPPRESSANT / anti-viral protein / ISOMERASE-IMMUNOSUPPRESSANT complex | ||||||
| Function / homology |  Function and homology information Function and homology informationnegative regulation of protein K48-linked ubiquitination / regulation of apoptotic signaling pathway / cell adhesion molecule production / lipid droplet organization / negative regulation of viral life cycle / heparan sulfate binding / regulation of viral genome replication / leukocyte chemotaxis / negative regulation of stress-activated MAPK cascade / activation of protein kinase B activity ...negative regulation of protein K48-linked ubiquitination / regulation of apoptotic signaling pathway / cell adhesion molecule production / lipid droplet organization / negative regulation of viral life cycle / heparan sulfate binding / regulation of viral genome replication / leukocyte chemotaxis / negative regulation of stress-activated MAPK cascade / activation of protein kinase B activity / endothelial cell activation / protein peptidyl-prolyl isomerization / cyclosporin A binding / negative regulation of protein phosphorylation / negative regulation of protein kinase activity / negative regulation of oxidative stress-induced intrinsic apoptotic signaling pathway / positive regulation of viral genome replication / neutrophil chemotaxis / : / positive regulation of protein secretion / peptidylprolyl isomerase / peptidyl-prolyl cis-trans isomerase activity / platelet activation / RING-type E3 ubiquitin transferase / positive regulation of protein phosphorylation / platelet aggregation / integrin binding / autophagy / ubiquitin protein ligase activity / protein folding / cellular response to oxidative stress / defense response to virus / positive regulation of MAPK cascade / protein ubiquitination / innate immune response / apoptotic process / protein-containing complex / extracellular region / zinc ion binding / nucleus / cytoplasm / cytosol Similarity search - Function | ||||||
| Biological species |   Tolypocladium inflatum (fungus) Tolypocladium inflatum (fungus) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 2.65 Å MOLECULAR REPLACEMENT / Resolution: 2.65 Å | ||||||
 Authors Authors | Caines, M.E.C. / Bichel, K. / Price, A.J. / McEwan, W.A. / James, L.C. | ||||||
 Citation Citation |  Journal: Nat.Struct.Mol.Biol. / Year: 2012 Journal: Nat.Struct.Mol.Biol. / Year: 2012Title: Diverse HIV viruses are targeted by a conformationally dynamic antiviral. Authors: Caines, M.E. / Bichel, K. / Price, A.J. / McEwan, W.A. / Towers, G.J. / Willett, B.J. / Freund, S.M. / James, L.C. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  4dgc.cif.gz 4dgc.cif.gz | 332.8 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb4dgc.ent.gz pdb4dgc.ent.gz | 275.6 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  4dgc.json.gz 4dgc.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/dg/4dgc https://data.pdbj.org/pub/pdb/validation_reports/dg/4dgc ftp://data.pdbj.org/pub/pdb/validation_reports/dg/4dgc ftp://data.pdbj.org/pub/pdb/validation_reports/dg/4dgc | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  4dgaC  4dgbC  4dgdC  4dgeC  2wlwS C: citing same article ( S: Starting model for refinement |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unit cell |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Noncrystallographic symmetry (NCS) | NCS domain:
NCS domain segments: Ens-ID: 1 / Refine code: 4
|
- Components
Components
| #1: Protein | Mass: 18016.473 Da / Num. of mol.: 5 / Fragment: cyclophilin domain (UNP residues 304-468) Source method: isolated from a genetically manipulated source Source: (gene. exp.)   References: UniProt: B0LJC8, UniProt: P62940*PLUS, peptidylprolyl isomerase #2: Protein/peptide | 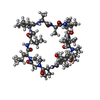  Type: Cyclic peptide / Class: Immunosuppressant / Mass: 1220.625 Da / Num. of mol.: 5 / Source method: obtained synthetically Type: Cyclic peptide / Class: Immunosuppressant / Mass: 1220.625 Da / Num. of mol.: 5 / Source method: obtained syntheticallyDetails: CYCLOSPORIN IS A CYCLIC UNDECAPEPTIDE. CYCLIZATION IS ACHIEVED BY LINKING THE N- AND THE C- TERMINI. Source: (synth.)  Tolypocladium inflatum (fungus) / References: NOR: NOR00033, Cyclosporin A Tolypocladium inflatum (fungus) / References: NOR: NOR00033, Cyclosporin A#3: Water | ChemComp-HOH / | Compound details | CYCLOSPORIN IS A CYCLIC UNDECAPEPTIDE. HERE, CYCLOSPORIN A IS REPRESENTED BY THE SEQUENCE (SEQRES) ...CYCLOSPORI | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 3.73 Å3/Da / Density % sol: 67.07 % |
|---|---|
| Crystal grow | Temperature: 290 K / Method: vapor diffusion, hanging drop / pH: 6.5 Details: 2.05 M ammonium sulfate, 10 MM magnesium sulfate, 0.1 M Bis-Tris, pH 6.5, VAPOR DIFFUSION, HANGING DROP, temperature 290K |
-Data collection
| Diffraction | Mean temperature: 100 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  ESRF ESRF  / Beamline: ID23-1 / Wavelength: 1.072 Å / Beamline: ID23-1 / Wavelength: 1.072 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: ADSC QUANTUM 315r / Detector: CCD / Date: Apr 24, 2010 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Monochromator: single crystal Si(111) / Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength | Wavelength: 1.072 Å / Relative weight: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 2.65→93.938 Å / Num. all: 41285 / Num. obs: 41285 / % possible obs: 94.9 % / Redundancy: 3.6 % / Biso Wilson estimate: 58.64 Å2 / Rsym value: 0.07 / Net I/σ(I): 12.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell | Diffraction-ID: 1
|
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: PDB ENTRY 2WLW Resolution: 2.65→93.938 Å / Cor.coef. Fo:Fc: 0.946 / Cor.coef. Fo:Fc free: 0.923 / WRfactor Rfree: 0.219 / WRfactor Rwork: 0.1836 / Occupancy max: 1 / Occupancy min: 1 / FOM work R set: 0.8853 / SU B: 12.683 / SU ML: 0.154 / SU R Cruickshank DPI: 0.3815 / SU Rfree: 0.2488 / Cross valid method: THROUGHOUT / σ(F): 0 / ESU R: 0.381 / ESU R Free: 0.249 / Stereochemistry target values: MAXIMUM LIKELIHOOD Details: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS U VALUES : WITH TLS ADDED
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Ion probe radii: 0.8 Å / Shrinkage radii: 0.8 Å / VDW probe radii: 1.2 Å / Solvent model: MASK | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 111.4 Å2 / Biso mean: 43.0877 Å2 / Biso min: 12.53 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 2.65→93.938 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints NCS | Dom-ID: 1 / Ens-ID: 1 / Number: 2032 / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 2.65→2.719 Å / Total num. of bins used: 20
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller











 PDBj
PDBj



