[English] 日本語
 Yorodumi
Yorodumi- PDB-3omz: Crystal structure of MICA-specific human gamma delta T cell receptor -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 3omz | ||||||
|---|---|---|---|---|---|---|---|
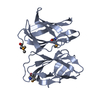
| Title | Crystal structure of MICA-specific human gamma delta T cell receptor | ||||||
 Components Components | human Vdelta1 gamma delta T cell receptor delta1A/B-3 | ||||||
 Keywords Keywords | IMMUNE SYSTEM / Immunoglobulin fold / Immune surveillance of cell stress protein MIC-A/B / MIC-A/B binding / Epithelium | ||||||
| Function / homology | Immunoglobulins / Immunoglobulin-like / Sandwich / Mainly Beta Function and homology information Function and homology information | ||||||
| Biological species |  Homo sapiens (human) Homo sapiens (human) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MAD / Resolution: 3.04 Å MAD / Resolution: 3.04 Å | ||||||
 Authors Authors | Xu, B. / Holmes, M.A. / Strong, R.K. | ||||||
 Citation Citation |  Journal: Proc.Natl.Acad.Sci.USA / Year: 2011 Journal: Proc.Natl.Acad.Sci.USA / Year: 2011Title: Crystal structure of a {gamma}{delta} T-cell receptor specific for the human MHC class I homolog MICA. Authors: Xu, B. / Pizarro, J.C. / Holmes, M.A. / McBeth, C. / Groh, V. / Spies, T. / Strong, R.K. #1:  Journal: Science / Year: 1998 Journal: Science / Year: 1998Title: Recognition of stress-induced MHC molecules by intestinal epithelial gamma delta T cells Authors: Groh, V. / Steinle, A. / Bauer, S. / Spies, T. #2:  Journal: Immunity / Year: 1999 Journal: Immunity / Year: 1999Title: Crystal structure of the MHC class I homolog MIC-A, a gammadelta T cell ligand Authors: Li, P. / Willie, S.T. / Bauer, S. / Morris, D.L. / Spies, T. / Strong, R.K. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  3omz.cif.gz 3omz.cif.gz | 233 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb3omz.ent.gz pdb3omz.ent.gz | 180.7 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  3omz.json.gz 3omz.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/om/3omz https://data.pdbj.org/pub/pdb/validation_reports/om/3omz ftp://data.pdbj.org/pub/pdb/validation_reports/om/3omz ftp://data.pdbj.org/pub/pdb/validation_reports/om/3omz | HTTPS FTP |
|---|
-Related structure data
| Similar structure data |
|---|
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 3 | 
| ||||||||
| 4 | 
| ||||||||
| Unit cell |
|
- Components
Components
| #1: Protein | Mass: 29232.941 Da / Num. of mol.: 4 Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Homo sapiens (human) / Plasmid: pET22b / Production host: Homo sapiens (human) / Plasmid: pET22b / Production host:  Has protein modification | Y | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.92 Å3/Da / Density % sol: 57.86 % |
|---|---|
| Crystal grow | Temperature: 295 K / Method: vapor diffusion, hanging drop / pH: 6.6 Details: 0.4M ammonium sulfate, 1.0M lithium sulfate, 0.1M sodium citrate, 0.03M glycyl-glycyl-glycine, pH 6.6, VAPOR DIFFUSION, HANGING DROP, temperature 295.0K |
-Data collection
| Diffraction | Mean temperature: 77 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  ALS ALS  / Beamline: 5.0.2 / Wavelength: 1 Å / Beamline: 5.0.2 / Wavelength: 1 Å |
| Detector | Type: ADSC QUANTUM 315r / Detector: CCD / Date: Oct 18, 2007 / Details: Dual crystal, Si(111) |
| Radiation | Monochromator: Dual crystal, Si(111) / Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 1 Å / Relative weight: 1 |
| Reflection | Resolution: 3.04→50 Å / Num. all: 25563 / Num. obs: 25563 / % possible obs: 99.8 % / Redundancy: 4.1 % / Rmerge(I) obs: 0.054 / Rsym value: 0.054 / Net I/σ(I): 48.4 |
| Reflection shell | Resolution: 3.04→3.16 Å / Redundancy: 4.1 % / Rmerge(I) obs: 0.365 / Mean I/σ(I) obs: 2.1 / % possible all: 99.1 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MAD / Resolution: 3.04→32.83 Å / Cor.coef. Fo:Fc: 0.888 / Cor.coef. Fo:Fc free: 0.849 / SU B: 39.567 / SU ML: 0.338 / Cross valid method: THROUGHOUT / ESU R: 0.849 / ESU R Free: 0.429 / Stereochemistry target values: MAXIMUM LIKELIHOOD / Details: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS MAD / Resolution: 3.04→32.83 Å / Cor.coef. Fo:Fc: 0.888 / Cor.coef. Fo:Fc free: 0.849 / SU B: 39.567 / SU ML: 0.338 / Cross valid method: THROUGHOUT / ESU R: 0.849 / ESU R Free: 0.429 / Stereochemistry target values: MAXIMUM LIKELIHOOD / Details: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Ion probe radii: 0.8 Å / Shrinkage radii: 0.8 Å / VDW probe radii: 1.4 Å / Solvent model: BABINET MODEL WITH MASK | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 90.023 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 3.04→32.83 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 3.037→3.115 Å / Total num. of bins used: 20
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller











 PDBj
PDBj