| 登録情報 | データベース: PDB / ID: 2lmg
|
|---|
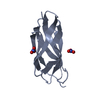
| タイトル | Solution Structure of The C-terminal Domain (537-610) of Human Heat Shock Protein 70 |
|---|
 要素 要素 | Heat shock 70 kDa protein 1A/1B |
|---|
 キーワード キーワード | CHAPERONE / HSP70 / Helix |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
: / positive regulation of endoribonuclease activity / denatured protein binding / cellular heat acclimation / death receptor agonist activity / negative regulation of inclusion body assembly / Viral RNP Complexes in the Host Cell Nucleus / positive regulation of nucleotide-binding oligomerization domain containing 2 signaling pathway / : / C3HC4-type RING finger domain binding ...: / positive regulation of endoribonuclease activity / denatured protein binding / cellular heat acclimation / death receptor agonist activity / negative regulation of inclusion body assembly / Viral RNP Complexes in the Host Cell Nucleus / positive regulation of nucleotide-binding oligomerization domain containing 2 signaling pathway / : / C3HC4-type RING finger domain binding / positive regulation of microtubule nucleation / ATP-dependent protein disaggregase activity / misfolded protein binding / regulation of mitotic spindle assembly / negative regulation of mitochondrial outer membrane permeabilization involved in apoptotic signaling pathway / positive regulation of tumor necrosis factor-mediated signaling pathway / transcription regulator inhibitor activity / aggresome / lysosomal transport / cellular response to steroid hormone stimulus / mRNA catabolic process / regulation of protein ubiquitination / chaperone cofactor-dependent protein refolding / HSF1-dependent transactivation / response to unfolded protein / negative regulation of extrinsic apoptotic signaling pathway in absence of ligand / chaperone-mediated protein complex assembly / Regulation of HSF1-mediated heat shock response / Attenuation phase / cellular response to unfolded protein / negative regulation of endoplasmic reticulum stress-induced intrinsic apoptotic signaling pathway / ATP metabolic process / protein folding chaperone / vesicle-mediated transport / inclusion body / negative regulation of protein ubiquitination / heat shock protein binding / HSP90 chaperone cycle for steroid hormone receptors (SHR) in the presence of ligand / centriole / positive regulation of RNA splicing / positive regulation of erythrocyte differentiation / AUF1 (hnRNP D0) binds and destabilizes mRNA / positive regulation of interleukin-8 production / G protein-coupled receptor binding / ATP-dependent protein folding chaperone / negative regulation of transforming growth factor beta receptor signaling pathway / PKR-mediated signaling / negative regulation of cell growth / histone deacetylase binding / transcription corepressor activity / disordered domain specific binding / unfolded protein binding / positive regulation of proteasomal ubiquitin-dependent protein catabolic process / virus receptor activity / positive regulation of NF-kappaB transcription factor activity / cellular response to heat / cellular response to oxidative stress / protein refolding / vesicle / ficolin-1-rich granule lumen / receptor ligand activity / blood microparticle / protein stabilization / nuclear speck / ribonucleoprotein complex / cadherin binding / negative regulation of cell population proliferation / focal adhesion / signaling receptor binding / centrosome / ubiquitin protein ligase binding / Neutrophil degranulation / positive regulation of gene expression / negative regulation of apoptotic process / perinuclear region of cytoplasm / enzyme binding / negative regulation of transcription by RNA polymerase II / endoplasmic reticulum / ATP hydrolysis activity / protein-containing complex / mitochondrion / RNA binding / extracellular space / extracellular exosome / extracellular region / nucleoplasm / ATP binding / nucleus / plasma membrane / cytoplasm / cytosol類似検索 - 分子機能 Substrate Binding Domain Of Dnak; Chain:A; Domain 2 - #10 / Heat shock hsp70 proteins family signature 2. / Heat shock hsp70 proteins family signature 1. / Heat shock hsp70 proteins family signature 3. / Heat shock protein 70, conserved site / Heat shock protein 70kD, peptide-binding domain superfamily / Heat shock protein 70 family / Hsp70 protein / Heat shock protein 70kD, C-terminal domain superfamily / Substrate Binding Domain Of Dnak; Chain:A; Domain 2 ...Substrate Binding Domain Of Dnak; Chain:A; Domain 2 - #10 / Heat shock hsp70 proteins family signature 2. / Heat shock hsp70 proteins family signature 1. / Heat shock hsp70 proteins family signature 3. / Heat shock protein 70, conserved site / Heat shock protein 70kD, peptide-binding domain superfamily / Heat shock protein 70 family / Hsp70 protein / Heat shock protein 70kD, C-terminal domain superfamily / Substrate Binding Domain Of Dnak; Chain:A; Domain 2 / ATPase, nucleotide binding domain / Up-down Bundle / Mainly Alpha類似検索 - ドメイン・相同性 Heat shock 70 kDa protein 1B / Heat shock 70 kDa protein 1A類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 | 溶液NMR / torsion angle dynamics |
|---|
| Model details | lowest energy, model 1 |
|---|
 データ登録者 データ登録者 | Zhou, C. / Gao, X. / Wu, M. / Hu, H. |
|---|
 引用 引用 |  ジャーナル: J.Biol.Chem. / 年: 2012 ジャーナル: J.Biol.Chem. / 年: 2012
タイトル: The C-terminal helices of heat shock protein 70 are essential for J-domain binding and ATPase activation.
著者: Gao, X.C. / Zhou, C.J. / Zhou, Z.R. / Wu, M. / Cao, C.Y. / Hu, H.Y. |
|---|
| 履歴 | | 登録 | 2011年12月1日 | 登録サイト: BMRB / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2012年1月11日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2019年12月25日 | Group: Data collection / Database references
カテゴリ: citation / citation_author ...citation / citation_author / pdbx_nmr_software / pdbx_nmr_spectrometer / struct_ref_seq_dif
Item: _citation.journal_volume / _citation.page_first ..._citation.journal_volume / _citation.page_first / _citation.page_last / _citation.pdbx_database_id_PubMed / _citation.title / _citation_author.name / _pdbx_nmr_software.name / _pdbx_nmr_spectrometer.model / _struct_ref_seq_dif.details |
|---|
| 改定 1.2 | 2023年6月14日 | Group: Database references / Other / カテゴリ: database_2 / pdbx_database_status
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession / _pdbx_database_status.status_code_nmr_data |
|---|
| 改定 1.3 | 2024年5月15日 | Group: Data collection / Database references / カテゴリ: chem_comp_atom / chem_comp_bond / database_2 / Item: _database_2.pdbx_DOI |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) データ登録者
データ登録者 引用
引用 ジャーナル: J.Biol.Chem. / 年: 2012
ジャーナル: J.Biol.Chem. / 年: 2012 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 2lmg.cif.gz
2lmg.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb2lmg.ent.gz
pdb2lmg.ent.gz PDB形式
PDB形式 2lmg.json.gz
2lmg.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 2lmg_validation.pdf.gz
2lmg_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 2lmg_full_validation.pdf.gz
2lmg_full_validation.pdf.gz 2lmg_validation.xml.gz
2lmg_validation.xml.gz 2lmg_validation.cif.gz
2lmg_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/lm/2lmg
https://data.pdbj.org/pub/pdb/validation_reports/lm/2lmg ftp://data.pdbj.org/pub/pdb/validation_reports/lm/2lmg
ftp://data.pdbj.org/pub/pdb/validation_reports/lm/2lmg リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 遺伝子: HSPA1A, HSPA1, HSPA1B / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: HSPA1A, HSPA1, HSPA1B / 発現宿主: 
 試料調製
試料調製 解析
解析 ムービー
ムービー コントローラー
コントローラー











 PDBj
PDBj








 HSQC
HSQC