+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1hcm | ||||||
|---|---|---|---|---|---|---|---|
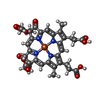
| タイトル | Cytochrome cd1 Nitrite Reductase, oxidised from from tetragonal crystals | ||||||
 要素 要素 | CYTOCHROME CD1 NITRITE REDUCTASE | ||||||
 キーワード キーワード | OXIDOREDUCTASE / ENZYME / NITRITE REDUCTASE | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報hydroxylamine reductase / hydroxylamine reductase activity / nitrite reductase (NO-forming) / nitrite reductase (NO-forming) activity / periplasmic space / electron transfer activity / heme binding / metal ion binding 類似検索 - 分子機能 | ||||||
| 生物種 |  PARACOCCUS PANTOTROPHUS (バクテリア) PARACOCCUS PANTOTROPHUS (バクテリア) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.5 Å 分子置換 / 解像度: 2.5 Å | ||||||
 データ登録者 データ登録者 | Sjogren, T. / Hajdu, J. | ||||||
 引用 引用 |  ジャーナル: J.Biol.Chem. / 年: 2001 ジャーナル: J.Biol.Chem. / 年: 2001タイトル: The Structure of an Alternative Form of Paracoccus Pantotrophus Cytochrome Cd1 Nitrite Reductase 著者: Sjogren, T. / Hajdu, J. #1:  ジャーナル: Nature / 年: 1997 ジャーナル: Nature / 年: 1997タイトル: Haem Ligand-Switching During Catalysis in Crystals of a Nitrogen Cycle Enzyme 著者: Williams, P.A. / Fulop, V. / Garman, E.F. / Saunders, N.F.W. / Ferguson, S.J. / Hajdu, J. #2:  ジャーナル: Cell(Cambridge,Mass.) / 年: 1995 ジャーナル: Cell(Cambridge,Mass.) / 年: 1995タイトル: The Anatomy of a Bifunctional Enzyme: Structural Basis for Reduction of Oxygen to Water and Synthesis of Nitric Oxide by Cytochrome Cd1 著者: Fulop, V. / Moir, J.W.B. / Saunders, N.F.W. / Ferguson, S.J. / Hajdu, J. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1hcm.cif.gz 1hcm.cif.gz | 226.4 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1hcm.ent.gz pdb1hcm.ent.gz | 181.6 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1hcm.json.gz 1hcm.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1hcm_validation.pdf.gz 1hcm_validation.pdf.gz | 1.8 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1hcm_full_validation.pdf.gz 1hcm_full_validation.pdf.gz | 1.8 MB | 表示 | |
| XML形式データ |  1hcm_validation.xml.gz 1hcm_validation.xml.gz | 44.5 KB | 表示 | |
| CIF形式データ |  1hcm_validation.cif.gz 1hcm_validation.cif.gz | 61.8 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/hc/1hcm https://data.pdbj.org/pub/pdb/validation_reports/hc/1hcm ftp://data.pdbj.org/pub/pdb/validation_reports/hc/1hcm ftp://data.pdbj.org/pub/pdb/validation_reports/hc/1hcm | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 62546.539 Da / 分子数: 2 / 由来タイプ: 天然 / 詳細: ORGANISM FORMERLY KNOWN AS THIOSPHAERA PANTOTROPHA / 由来: (天然)  PARACOCCUS PANTOTROPHUS (バクテリア) / 細胞内の位置: PERIPLASM / 参照: UniProt: Q9FCQ0, UniProt: P72181*PLUS PARACOCCUS PANTOTROPHUS (バクテリア) / 細胞内の位置: PERIPLASM / 参照: UniProt: Q9FCQ0, UniProt: P72181*PLUS#2: 化合物 | #3: 化合物 | #4: 化合物 | ChemComp-SO4 / #5: 水 | ChemComp-HOH / | Has protein modification | Y | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 4.3 Å3/Da / 溶媒含有率: 71.16 % | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 9 詳細: HANGING DROP USING 2.1 M AMMONIUM SULPHATE AND 100 MM CHES PH 7.0 1 MM ASCORBATE AND 2.5 UM PMS FROM REDUCTION OF PROTEIN WAS ALSO PRESENT IN CRYSTALLISATION. CRYSTALS WERE GROWN UNDER ...詳細: HANGING DROP USING 2.1 M AMMONIUM SULPHATE AND 100 MM CHES PH 7.0 1 MM ASCORBATE AND 2.5 UM PMS FROM REDUCTION OF PROTEIN WAS ALSO PRESENT IN CRYSTALLISATION. CRYSTALS WERE GROWN UNDER STRICTLY ANAEROBIC CONDITIONS. THE ENZYME WAS OXIDISED IN THE CRYSTAL BY ALLOWING AIR TO DIFFUSE INTO THE DROP | ||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 手法: 蒸気拡散法, ハンギングドロップ法 | ||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  MAX II MAX II  / ビームライン: I711 / 波長: 1.0252 / ビームライン: I711 / 波長: 1.0252 |
| 検出器 | タイプ: MARRESEARCH / 検出器: IMAGE PLATE / 日付: 2000年10月5日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1.0252 Å / 相対比: 1 |
| 反射 | 解像度: 2.5→30 Å / Num. obs: 74676 / % possible obs: 98.1 % / Observed criterion σ(I): 0 / 冗長度: 3.1 % / Biso Wilson estimate: 35.6 Å2 / Rmerge(I) obs: 0.062 / Rsym value: 0.062 / Net I/σ(I): 17.6 |
| 反射 シェル | 解像度: 2.5→2.59 Å / Rmerge(I) obs: 0.28 / Mean I/σ(I) obs: 3.9 / Rsym value: 0.28 / % possible all: 91.2 |
| 反射 | *PLUS 最低解像度: 30 Å |
| 反射 シェル | *PLUS % possible obs: 91.2 % / 冗長度: 2.8 % / Rmerge(I) obs: 0.28 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: PDB ENTRY 1H9X 解像度: 2.5→30 Å / SU B: 6.86 / 交差検証法: THROUGHOUT / σ(F): 0 詳細: IN SUBUNIT A RESIDUES A 1 - A 41 ARE DISORDERED STRUCTURE AND WERE NOT MODELLED. IN SUBUNIT B RESIDUES B 1 - B 38 ARE DISORDERED STRUCTURE AND WERE NOT MODELLED.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 39.7 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.5→30 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称: REFMAC / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS Rfactor obs: 0.226 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー


















 PDBj
PDBj