+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1fc2 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
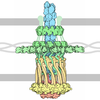
| タイトル | Crystallographic Refinement and Atomic Models of a Human FC Fragment and its Complex with Fragment B of Protein A from Staphylococcus Aureus at 2.9-and 2.8-Angstroms Resolution | ||||||||||||
 要素 要素 |
| ||||||||||||
 キーワード キーワード | IMMUNOGLOBULIN | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Fc-gamma receptor I complex binding / complement-dependent cytotoxicity / IgG immunoglobulin complex / antibody-dependent cellular cytotoxicity / IgG binding / immunoglobulin receptor binding / immunoglobulin complex, circulating / Classical antibody-mediated complement activation / Initial triggering of complement / FCGR activation ...Fc-gamma receptor I complex binding / complement-dependent cytotoxicity / IgG immunoglobulin complex / antibody-dependent cellular cytotoxicity / IgG binding / immunoglobulin receptor binding / immunoglobulin complex, circulating / Classical antibody-mediated complement activation / Initial triggering of complement / FCGR activation / complement activation, classical pathway / Role of phospholipids in phagocytosis / antigen binding / FCGR3A-mediated IL10 synthesis / Regulation of Complement cascade / B cell receptor signaling pathway / FCGR3A-mediated phagocytosis / Regulation of actin dynamics for phagocytic cup formation / antibacterial humoral response / Interleukin-4 and Interleukin-13 signaling / blood microparticle / adaptive immune response / extracellular space / extracellular exosome / extracellular region / plasma membrane 類似検索 - 分子機能 | ||||||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
| 手法 |  X線回折 / 解像度: 2.8 Å X線回折 / 解像度: 2.8 Å | ||||||||||||
 データ登録者 データ登録者 | Deisenhofer, J. | ||||||||||||
 引用 引用 |  ジャーナル: Biochemistry / 年: 1981 ジャーナル: Biochemistry / 年: 1981タイトル: Crystallographic refinement and atomic models of a human Fc fragment and its complex with fragment B of protein A from Staphylococcus aureus at 2.9- and 2.8-A resolution. 著者: Deisenhofer, J. #1:  ジャーナル: Hoppe-Seyler's Z.Physiol.Chem. / 年: 1978 ジャーナル: Hoppe-Seyler's Z.Physiol.Chem. / 年: 1978タイトル: Crystallization, Crystal Structure Analysis and Atomic Model of the Complex Formed by a Human Fc Fragment and Fragment B of Protein a from Staphylococcus Aureus 著者: Deisenhofer, J. / Jones, T.A. / Huber, R. / Sjodahl, J. / Sjoquist, J. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1fc2.cif.gz 1fc2.cif.gz | 66 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1fc2.ent.gz pdb1fc2.ent.gz | 46 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1fc2.json.gz 1fc2.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1fc2_validation.pdf.gz 1fc2_validation.pdf.gz | 508 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1fc2_full_validation.pdf.gz 1fc2_full_validation.pdf.gz | 515.5 KB | 表示 | |
| XML形式データ |  1fc2_validation.xml.gz 1fc2_validation.xml.gz | 8.5 KB | 表示 | |
| CIF形式データ |  1fc2_validation.cif.gz 1fc2_validation.cif.gz | 12.1 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/fc/1fc2 https://data.pdbj.org/pub/pdb/validation_reports/fc/1fc2 ftp://data.pdbj.org/pub/pdb/validation_reports/fc/1fc2 ftp://data.pdbj.org/pub/pdb/validation_reports/fc/1fc2 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 単位格子 |
| ||||||||
| Atom site foot note | 1: THESE ATOMS WERE NOT FOUND IN THE ELECTRON DENSITY MAP. THEIR COORDINATES WERE GENERATED USING STEREOCHEMICAL CRITERIA 2: RESIDUE PRO D 374 IS A CIS-PROLINE. | ||||||||
| 詳細 | THE CRYSTALLOGRAPHIC ASYMMETRIC UNIT, FOR WHICH COORDINATES ARE PRESENTED BELOW, CONSISTS OF ONE FRAGMENT B OF PROTEIN A (CHAIN INDICATOR C BELOW) AND ONE-HALF OF AN FC FRAGMENT (CHAIN INDICATOR D BELOW) TOGETHER WITH ITS POLYSACCHARIDE. THE FOLLOWING SYMMETRY OPERATION WHEN APPLIED TO THE COORDINATES OF THE ONE-HALF OF THE FC FRAGMENT GIVEN BELOW (CHAIN D) WILL GENERATE THE SECOND HALF OF THE FC FRAGMENT MOLECULE TRNSF1 1 -0.50000 -0.86603 0.00000 0.000 TRNSF2 1 -0.86603 0.50000 0.00000 0.000 TRNSF3 1 0.00000 0.00000 -1.00000 49.133 |
- 要素
要素
| #1: タンパク質 | 分子量: 6608.254 Da / 分子数: 1 / 由来タイプ: 組換発現 由来: (組換発現)  株: NCTC 8325 / 参照: UniProt: P02976, UniProt: P38507*PLUS |
|---|---|
| #2: タンパク質 | 分子量: 25236.615 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 参照: EMBL: Y14737, UniProt: P01857*PLUS Homo sapiens (ヒト) / 参照: EMBL: Y14737, UniProt: P01857*PLUS |
| #3: 多糖 | beta-D-galactopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose-(1-2)-alpha-D-mannopyranose- ...beta-D-galactopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose-(1-2)-alpha-D-mannopyranose-(1-6)-[2-acetamido-2-deoxy-beta-D-glucopyranose-(1-2)-alpha-D-mannopyranose-(1-3)]alpha-D-mannopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose-(1-4)-[alpha-L-fucopyranose-(1-6)]2-acetamido-2-deoxy-beta-D-glucopyranose |
| #4: 化合物 | ChemComp-SO4 / |
| Has protein modification | Y |
-実験情報
-実験
| 実験 | 手法:  X線回折 X線回折 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 3.33 Å3/Da / 溶媒含有率: 63.03 % | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | *PLUS pH: 6.8 / 手法: microdialysis / 詳細: took Deisenhofer et al., 1976a from original paper | ||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 放射 | 散乱光タイプ: x-ray |
|---|---|
| 放射波長 | 相対比: 1 |
| 反射 | *PLUS 最高解像度: 2.8 Å / Num. obs: 7002 / % possible obs: 62 % / Num. measured all: 25876 |
- 解析
解析
| 精密化 | 最高解像度: 2.8 Å | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化ステップ | サイクル: LAST / 最高解像度: 2.8 Å
| ||||||||||||
| 精密化 | *PLUS 最高解像度: 2.8 Å / 最低解像度: 7 Å / Num. reflection all: 6243 / Rfactor Rwork: 0.24 | ||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||
| 原子変位パラメータ | *PLUS |
 ムービー
ムービー コントローラー
コントローラー












 PDBj
PDBj