+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1bj3 | ||||||
|---|---|---|---|---|---|---|---|
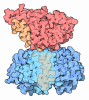
| タイトル | CRYSTAL STRUCTURE OF COAGULATION FACTOR IX-BINDING PROTEIN (IX-BP) FROM VENOM OF HABU SNAKE WITH A HETERODIMER OF C-TYPE LECTIN DOMAINS | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | COLLAGEN BINDING PROTEIN / COAGULATION FACTOR IX-BINDING / HETERODIMER / VENOM / HABU SNAKE / C-TYPE LECTIN SUPERFAMILY | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||
| 生物種 |  Trimeresurus flavoviridis (ハブ) Trimeresurus flavoviridis (ハブ) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  単一同系置換・異常分散 / 解像度: 2.6 Å 単一同系置換・異常分散 / 解像度: 2.6 Å | ||||||
 データ登録者 データ登録者 | Mizuno, H. / Fujimoto, Z. / Koizumi, M. / Kano, H. / Atoda, H. / Morita, T. | ||||||
 引用 引用 |  ジャーナル: J.Mol.Biol. / 年: 1999 ジャーナル: J.Mol.Biol. / 年: 1999タイトル: Crystal structure of coagulation factor IX-binding protein from habu snake venom at 2.6 A: implication of central loop swapping based on deletion in the linker region. 著者: Mizuno, H. / Fujimoto, Z. / Koizumi, M. / Kano, H. / Atoda, H. / Morita, T. #1:  ジャーナル: Nat.Struct.Biol. / 年: 1997 ジャーナル: Nat.Struct.Biol. / 年: 1997タイトル: Structure of Coagulation Factors Ix/X-Binding Protein, a Heterodimer of C-Type Lectin Domains 著者: Mizuno, H. / Fujimoto, Z. / Koizumi, M. / Kano, H. / Atoda, H. / Morita, T. #2:  ジャーナル: J.Biochem.(Tokyo) / 年: 1995 ジャーナル: J.Biochem.(Tokyo) / 年: 1995タイトル: Blood Coagulation Factor Ix-Binding Protein from the Venom of Trimeresurus Flavoviridis: Purification and Characterization 著者: Atoda, H. / Ishikawa, M. / Yoshihara, E. / Sekiya, F. / Morita, T. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1bj3.cif.gz 1bj3.cif.gz | 65.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1bj3.ent.gz pdb1bj3.ent.gz | 48.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1bj3.json.gz 1bj3.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/bj/1bj3 https://data.pdbj.org/pub/pdb/validation_reports/bj/1bj3 ftp://data.pdbj.org/pub/pdb/validation_reports/bj/1bj3 ftp://data.pdbj.org/pub/pdb/validation_reports/bj/1bj3 | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 14655.184 Da / 分子数: 1 / 断片: C-TYPE LECTIN CRD DOMAIN / 由来タイプ: 天然 詳細: DISULPHIDE DIMER BETWEEN A CYS79 AND B CYS75, PROTEIN COMPOSED OF HOMOLOGOUS SUBUNITS TO THE CARBOHYDRATE RECOGNITION DOMAIN OF C-TYPE LECTIN 由来: (天然)  Trimeresurus flavoviridis (ハブ) / Secretion: VENOM / 参照: PIR: JC4329, UniProt: Q7LZ71*PLUS Trimeresurus flavoviridis (ハブ) / Secretion: VENOM / 参照: PIR: JC4329, UniProt: Q7LZ71*PLUS | ||||||
|---|---|---|---|---|---|---|---|
| #2: タンパク質 | 分子量: 14455.071 Da / 分子数: 1 / 断片: C-TYPE LECTIN CRD DOMAIN / 由来タイプ: 天然 詳細: DISULPHIDE DIMER BETWEEN A CYS79 AND B CYS75, PROTEIN COMPOSED OF HOMOLOGOUS SUBUNITS TO THE CARBOHYDRATE RECOGNITION DOMAIN OF C-TYPE LECTIN 由来: (天然)  Trimeresurus flavoviridis (ハブ) / Secretion: VENOM / 参照: UniProt: P23807 Trimeresurus flavoviridis (ハブ) / Secretion: VENOM / 参照: UniProt: P23807 | ||||||
| #3: 化合物 | | #4: 水 | ChemComp-HOH / | Has protein modification | Y | 配列の詳細 | REFERENCE: MATURE PROTEIN LACKS INITIAL 23 RESIDUES, B CHAIN OF IX-BINDING PROTEIN IS THE SAME AS ...REFERENCE: MATURE PROTEIN LACKS INITIAL 23 RESIDUES, B CHAIN OF IX-BINDING PROTEIN IS THE SAME AS THAT OF FACTOR IX/FACTOR X-BINDING ANTICOAGUL | |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 2 X線回折 / 使用した結晶の数: 2 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.3 Å3/Da / 溶媒含有率: 47 % | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | pH: 7.8 詳細: PROTEIN WAS CRYSTALLIZED BY MIXING WITH EQUAL VOLUME OF 60% AMMONIUM SULPHATE IN 20 MM TRI-HCL BUFFER AT PH 7.8 CONTAINING AND AT ROOM TEMPERATURE | ||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 20 ℃ / 手法: 蒸気拡散法, ハンギングドロップ法 | ||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 298 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  Photon Factory Photon Factory  / ビームライン: BL-6A / 波長: 1 / ビームライン: BL-6A / 波長: 1 |
| 検出器 | タイプ: RIGAKU / 検出器: IMAGE PLATE / 日付: 1995年6月15日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1 Å / 相対比: 1 |
| 反射 | 解像度: 2.6→100 Å / Num. obs: 7253 / % possible obs: 90 % / Observed criterion σ(I): 3 / 冗長度: 4.1 % / Biso Wilson estimate: 25.1 Å2 / Rmerge(I) obs: 0.102 / Net I/σ(I): 12 |
| 反射 シェル | 解像度: 2.6→2.72 Å / 冗長度: 2.3 % / Rmerge(I) obs: 0.145 / Mean I/σ(I) obs: 8.6 / % possible all: 74 |
| 反射 | *PLUS Num. measured all: 21947 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  単一同系置換・異常分散 / 解像度: 2.6→6 Å / Rfactor Rfree error: 0.014 / Data cutoff high absF: 10000000 / Data cutoff low absF: 0.001 / Isotropic thermal model: RESTRAINED / 交差検証法: THROUGHOUT / σ(F): 2 単一同系置換・異常分散 / 解像度: 2.6→6 Å / Rfactor Rfree error: 0.014 / Data cutoff high absF: 10000000 / Data cutoff low absF: 0.001 / Isotropic thermal model: RESTRAINED / 交差検証法: THROUGHOUT / σ(F): 2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 17.3 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.6→6 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | 解像度: 2.6→2.75 Å / Rfactor Rfree error: 0.045 / Total num. of bins used: 6
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xplor file |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称:  X-PLOR / バージョン: 2.1 / 分類: refinement X-PLOR / バージョン: 2.1 / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS 最高解像度: 2.6 Å / % reflection Rfree: 5.6 % | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS Biso mean: 17.3 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | *PLUS Rfactor Rfree: 0.33 / % reflection Rfree: 5.9 % / Rfactor Rwork: 0.234 |
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj