+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8015 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
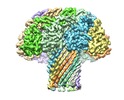
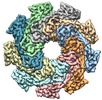
| タイトル | Cryo-EM structure of the Lysenin Pore | |||||||||
 マップデータ マップデータ | None | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Pore forming protein / aerolysin / toxin | |||||||||
| 機能・相同性 | other organism cell membrane / monoatomic ion transport / toxin activity / killing of cells of another organism / defense response to bacterium / extracellular region / Lysenin 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Savva CG / Bokori-Brown M | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2016 ジャーナル: Nat Commun / 年: 2016タイトル: Cryo-EM structure of lysenin pore elucidates membrane insertion by an aerolysin family protein. 著者: Monika Bokori-Brown / Thomas G Martin / Claire E Naylor / Ajit K Basak / Richard W Titball / Christos G Savva /  要旨: Lysenin from the coelomic fluid of the earthworm Eisenia fetida belongs to the aerolysin family of small β-pore-forming toxins (β-PFTs), some members of which are pathogenic to humans and animals. ...Lysenin from the coelomic fluid of the earthworm Eisenia fetida belongs to the aerolysin family of small β-pore-forming toxins (β-PFTs), some members of which are pathogenic to humans and animals. Despite efforts, a high-resolution structure of a channel for this family of proteins has been elusive and therefore the mechanism of activation and membrane insertion remains unclear. Here we determine the pore structure of lysenin by single particle cryo-EM, to 3.1 Å resolution. The nonameric assembly reveals a long β-barrel channel spanning the length of the complex that, unexpectedly, includes the two pre-insertion strands flanking the hypothetical membrane-insertion loop. Examination of other members of the aerolysin family reveals high structural preservation in this region, indicating that the membrane-insertion pathway in this family is conserved. For some toxins, proteolytic activation and pro-peptide removal will facilitate unfolding of the pre-insertion strands, allowing them to form the β-barrel of the channel. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8015.map.gz emd_8015.map.gz | 3.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8015-v30.xml emd-8015-v30.xml emd-8015.xml emd-8015.xml | 16.4 KB 16.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8015_1.png emd_8015_1.png emd_8015_2.png emd_8015_2.png | 202.3 KB 252.9 KB | ||
| Filedesc metadata |  emd-8015.cif.gz emd-8015.cif.gz | 6.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8015 http://ftp.pdbj.org/pub/emdb/structures/EMD-8015 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8015 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8015 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8015.map.gz / 形式: CCP4 / 大きさ: 42.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8015.map.gz / 形式: CCP4 / 大きさ: 42.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | None | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.43 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
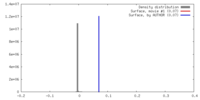
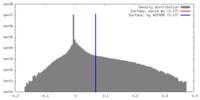
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Membrane-inserted form of the nonameric pore forming protein Lysenin
| 全体 | 名称: Membrane-inserted form of the nonameric pore forming protein Lysenin |
|---|---|
| 要素 |
|
-超分子 #1: Membrane-inserted form of the nonameric pore forming protein Lysenin
| 超分子 | 名称: Membrane-inserted form of the nonameric pore forming protein Lysenin タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 315 KDa |
-分子 #1: Lysenin
| 分子 | 名称: Lysenin / タイプ: protein_or_peptide / ID: 1 / コピー数: 9 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 34.977246 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSAKAAEGYE QIEVDVVAVW KEGYVYENRG STSVDQKITI TKGMKNVNSE TRTVTATHSI GSTISTGDAF EIGSVEVSYS HSHEESQVS MTETEVYESK VIEHTITIPP TSKFTRWQLN ADVGGADIEY MYLIDEVTPI GGTQSIPQVI TSRAKIIVGR Q IILGKTEI ...文字列: MSAKAAEGYE QIEVDVVAVW KEGYVYENRG STSVDQKITI TKGMKNVNSE TRTVTATHSI GSTISTGDAF EIGSVEVSYS HSHEESQVS MTETEVYESK VIEHTITIPP TSKFTRWQLN ADVGGADIEY MYLIDEVTPI GGTQSIPQVI TSRAKIIVGR Q IILGKTEI RIKHAERKEY MTVVSRKSWP AATLGHSKLF KFVLYEDWGG FRIKTLNTMY SGYEYAYSSD QGGIYFDQGT DN PKQRWAI NKSLPLRHGD VVTFMNKYFT RSGLCYDDGP ATNVYCLDKR EDKWILEVVG LVPRGSGHHH HHH UniProtKB: Lysenin |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.2 mg/mL | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
| ||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: GRAPHENE / 支持フィルム - トポロジー: CONTINUOUS 詳細: Grids were glow-discharged prior to deposition of Graphene-oxide.No further treatment was performed after graphene-oxide deposition. | ||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 277 K |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 85.0 K / 最高: 85.0 K |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum エネルギーフィルター - エネルギー下限: 0 eV エネルギーフィルター - エネルギー上限: 20 eV |
| 詳細 | Direct alignments: Beam tilt pivot points, Beam shift, Comma Free. C2 aperture centering, C2 lens astigmatism correction. Objective aperture centering and objective lens astigmatism correction. Energy filter Tuning and occasional ZLP centering. |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - サイズ - 横: 3710 pixel / デジタル化 - サイズ - 縦: 3710 pixel / デジタル化 - 画像ごとのフレーム数: 0-20 / 撮影したグリッド数: 1 / 実像数: 280 / 平均露光時間: 18.0 sec. / 平均電子線量: 47.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 4.7 µm 最小 デフォーカス(補正後): 0.7000000000000001 µm 倍率(補正後): 34965 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A / Chain - Residue range: 150-297 / Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | Initial docking of C-terminal region of lysenin monomer to EM map was performed using UCSF Chimera followed by model N-terminal extension in COOT. |
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
| 得られたモデル |  PDB-5gaq: |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)