+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-5752 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryogenic electron microscopy of cardiac actin:tropomyosin | |||||||||
 マップデータ マップデータ | Reconstruction of rabbit skeletal F-actin and bovine cardiac (striated) tropomyosin. The map is filtered at 15 Angstrom resolution. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | coiled-coil / actin-binding protein / cytoskeleton | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cardiac myofibril / cytoskeletal motor activator activity / myofibril / tropomyosin binding / myosin heavy chain binding / mesenchyme migration / troponin I binding / filamentous actin / actin filament bundle / skeletal muscle thin filament assembly ...cardiac myofibril / cytoskeletal motor activator activity / myofibril / tropomyosin binding / myosin heavy chain binding / mesenchyme migration / troponin I binding / filamentous actin / actin filament bundle / skeletal muscle thin filament assembly / actin filament bundle assembly / striated muscle thin filament / skeletal muscle myofibril / actin monomer binding / skeletal muscle fiber development / stress fiber / cardiac muscle contraction / muscle contraction / titin binding / actin filament polymerization / sarcomere / actin filament organization / filopodium / actin filament / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / calcium-dependent protein binding / disordered domain specific binding / actin filament binding / actin cytoskeleton / lamellipodium / actin binding / cell body / hydrolase activity / protein heterodimerization activity / protein domain specific binding / calcium ion binding / positive regulation of gene expression / magnesium ion binding / protein homodimerization activity / ATP binding / identical protein binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |   | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 15.0 Å | |||||||||
 データ登録者 データ登録者 | Sousa DR / Stagg SM / Stroupe ME | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2013 ジャーナル: J Mol Biol / 年: 2013タイトル: Cryo-EM structures of the actin:tropomyosin filament reveal the mechanism for the transition from C- to M-state. 著者: Duncan R Sousa / Scott M Stagg / M Elizabeth Stroupe /  要旨: Tropomyosin (Tm) is a key factor in the molecular mechanisms that regulate the binding of myosin motors to actin filaments (F-Actins) in most eukaryotic cells. This regulation is achieved by the ...Tropomyosin (Tm) is a key factor in the molecular mechanisms that regulate the binding of myosin motors to actin filaments (F-Actins) in most eukaryotic cells. This regulation is achieved by the azimuthal repositioning of Tm along the actin (Ac):Tm:troponin (Tn) thin filament to block or expose myosin binding sites on Ac. In striated muscle, including involuntary cardiac muscle, Tm regulates muscle contraction by coupling Ca(2+) binding to Tn with myosin binding to the thin filament. In smooth muscle, the switch is the posttranslational modification of the myosin. Depending on the activation state of Tn and the binding state of myosin, Tm can occupy the blocked, closed, or open position on Ac. Using native cryogenic 3DEM (three-dimensional electron microscopy), we have directly resolved and visualized cardiac and gizzard muscle Tm on filamentous Ac in the position that corresponds to the closed state. From the 8-Å-resolution structure of the reconstituted Ac:Tm filament formed with gizzard-derived Tm, we discuss two possible mechanisms for the transition from closed to open state and describe the role Tm plays in blocking myosin tight binding in the closed-state position. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_5752.map.gz emd_5752.map.gz | 211.3 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-5752-v30.xml emd-5752-v30.xml emd-5752.xml emd-5752.xml | 11.7 KB 11.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_5752_1.jpg emd_5752_1.jpg | 53.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-5752 http://ftp.pdbj.org/pub/emdb/structures/EMD-5752 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5752 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5752 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_5752_validation.pdf.gz emd_5752_validation.pdf.gz | 78.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_5752_full_validation.pdf.gz emd_5752_full_validation.pdf.gz | 77.7 KB | 表示 | |
| XML形式データ |  emd_5752_validation.xml.gz emd_5752_validation.xml.gz | 495 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5752 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5752 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5752 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5752 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_5752.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_5752.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of rabbit skeletal F-actin and bovine cardiac (striated) tropomyosin. The map is filtered at 15 Angstrom resolution. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.477 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
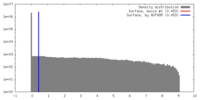
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : rabbit skeletal F-actin bound to bovine cardiac tropomyosin
| 全体 | 名称: rabbit skeletal F-actin bound to bovine cardiac tropomyosin |
|---|---|
| 要素 |
|
-超分子 #1000: rabbit skeletal F-actin bound to bovine cardiac tropomyosin
| 超分子 | 名称: rabbit skeletal F-actin bound to bovine cardiac tropomyosin タイプ: sample / ID: 1000 集合状態: fourteen actin monomers bind to two tropomyosin coiled-coils Number unique components: 2 |
|---|
-分子 #1: Actin, alpha skeletal muscle
| 分子 | 名称: Actin, alpha skeletal muscle / タイプ: protein_or_peptide / ID: 1 / Name.synonym: Alpha-actin-1 詳細: F-actin filaments were formed and tropomyosin was bound to the filaments. 集合状態: filament / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 728 KDa |
| 配列 | UniProtKB: Actin, alpha skeletal muscle / GO: skeletal muscle thin filament assembly / InterPro: Actin family |
-分子 #2: Tropomyosin alpha-1
| 分子 | 名称: Tropomyosin alpha-1 / タイプ: protein_or_peptide / ID: 2 / Name.synonym: Alpha-tropomyosin, Tropomyosin-1 詳細: F-actin filaments were formed and tropomyosin was bound to the filaments. 集合状態: filament / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 728 KDa |
| 配列 | UniProtKB: Tropomyosin alpha-1 chain / GO: actin binding / InterPro: Tropomyosin |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.1 詳細: 70 mM NaCl, 3 mM MgCl2, 0.2 mM EGTA, 5 mM NaH2PO4, 5 mM PIPES buffer |
| グリッド | 詳細: Quantifoil 1.2/1.3 sized holes |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 120 K / 装置: FEI VITROBOT MARK IV 手法: Blot with calcium-free filter paper for 2.5 seconds before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 日付 | 2010年3月25日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 実像数: 500 / 平均電子線量: 30 e/Å2 詳細: Images are recorded on a Gatan Ultrascan 4000 CCD and are available upon request to MES (mestroupe@bio.fsu.edu) |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 101555 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 1.5 µm / 倍率(公称値): 59000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | Filaments were selected by hand via points along each filament and then boxed at even intervals. |
|---|---|
| CTF補正 | 詳細: Micrograph |
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 27.5 Å 想定した対称性 - らせんパラメータ - ΔΦ: 166.6 ° 想定した対称性 - らせんパラメータ - 軸対称性: C1 (非対称) アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 15.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: Matlab, SPIDER, EMAN / 使用した粒子像数: 49318 |
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - #0 - Chain ID: B / Chain - #1 - Chain ID: H |
|---|---|
| ソフトウェア | 名称: Chimera Fit-in-Map |
| 詳細 | The F-actin and tropomyosin were fitted separately. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: Cross correlation |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)