+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4127 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM reconstruction of the Bacterial proteasome interactor (Bpa) bound to the 20S proteasome of M. tuberculosis. | |||||||||
 マップデータ マップデータ | bacterial proteasome activator bound to bacterial proteasome reconstructed without applied symmetry | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報symbiont-mediated perturbation of host defenses / zymogen binding / proteasome accessory complex / positive regulation of proteasomal protein catabolic process / proteasome binding / proteasome endopeptidase complex / proteasome core complex, beta-subunit complex / threonine-type endopeptidase activity / proteasome core complex, alpha-subunit complex / proteasomal protein catabolic process ...symbiont-mediated perturbation of host defenses / zymogen binding / proteasome accessory complex / positive regulation of proteasomal protein catabolic process / proteasome binding / proteasome endopeptidase complex / proteasome core complex, beta-subunit complex / threonine-type endopeptidase activity / proteasome core complex, alpha-subunit complex / proteasomal protein catabolic process / peptidoglycan-based cell wall / : / protein homooligomerization / modification-dependent protein catabolic process / proteasome-mediated ubiquitin-dependent protein catabolic process / extracellular region / plasma membrane / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Mycobacterium tuberculosis H37Rv (結核菌) Mycobacterium tuberculosis H37Rv (結核菌) | |||||||||
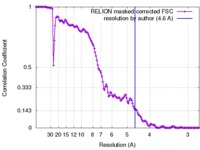
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.6 Å | |||||||||
 データ登録者 データ登録者 | Bolten M / Delley CL / Leibundgut M / Boehringer D / Ban N / Weber-Ban E | |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2016 ジャーナル: Structure / 年: 2016タイトル: Structural Analysis of the Bacterial Proteasome Activator Bpa in Complex with the 20S Proteasome. 著者: Marcel Bolten / Cyrille L Delley / Marc Leibundgut / Daniel Boehringer / Nenad Ban / Eilika Weber-Ban /  要旨: Mycobacterium tuberculosis harbors proteasomes that recruit substrates for degradation through an ubiquitin-like modification pathway. Recently, a non-ATPase activator termed Bpa (bacterial ...Mycobacterium tuberculosis harbors proteasomes that recruit substrates for degradation through an ubiquitin-like modification pathway. Recently, a non-ATPase activator termed Bpa (bacterial proteasome activator) was shown to support an alternate proteasomal degradation pathway. Here, we present the cryo-electron microscopy (cryo-EM) structure of Bpa in complex with the 20S core particle (CP). For docking into the cryo-EM density, we solved the X-ray structure of Bpa, showing that it forms tight four-helix bundles arranged into a 12-membered ring with a 40 Å wide central pore and the C-terminal helix of each protomer protruding from the ring. The Bpa model was fitted into the cryo-EM map of the Bpa-CP complex, revealing its architecture and striking symmetry mismatch. The Bpa-CP interface was resolved to 3.5 Å, showing the interactions between the C-terminal GQYL motif of Bpa and the proteasome α-rings. This docking mode is related to the one observed for eukaryotic activators with features specific to the bacterial complex. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4127.map.gz emd_4127.map.gz | 200.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4127-v30.xml emd-4127-v30.xml emd-4127.xml emd-4127.xml | 12.5 KB 12.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_4127_fsc.xml emd_4127_fsc.xml | 13.3 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4127.png emd_4127.png | 153 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4127 http://ftp.pdbj.org/pub/emdb/structures/EMD-4127 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4127 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4127 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4127.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4127.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | bacterial proteasome activator bound to bacterial proteasome reconstructed without applied symmetry | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.4 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : proteasome in complex with bacterial proteasome activator
| 全体 | 名称: proteasome in complex with bacterial proteasome activator |
|---|---|
| 要素 |
|
-超分子 #1: proteasome in complex with bacterial proteasome activator
| 超分子 | 名称: proteasome in complex with bacterial proteasome activator タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#7 |
|---|---|
| 由来(天然) | 生物種:  Mycobacterium tuberculosis H37Rv (結核菌) Mycobacterium tuberculosis H37Rv (結核菌) |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 930 KDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.102 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: OTHER 詳細: Quantifoil R 2/2 with an additional thin carbon layer | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 280.5 K / 装置: FEI VITROBOT MARK I |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON II (4k x 4k) 検出モード: INTEGRATING / デジタル化 - サンプリング間隔: 14.0 µm / 撮影したグリッド数: 1 / 平均電子線量: 25.0 e/Å2 詳細: Drift corrected in post-processing. 4 images per hole. |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 100000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.6 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 59000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)