+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Partially closed falcilysin, from free falcilysin dataset | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | falcilysin partially closed conformation / HYDROLASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報hemoglobin catabolic process / apicoplast / food vacuole / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; その他のペプチターゼ / vacuolar membrane / protein processing / metalloendopeptidase activity / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
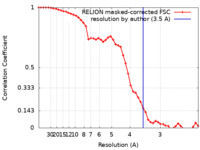
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.5 Å | |||||||||
 データ登録者 データ登録者 | Lin JQ / Yan XF / Lescar J | |||||||||
| 資金援助 |  シンガポール, 1件 シンガポール, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2024 ジャーナル: Commun Biol / 年: 2024タイトル: Inhibition of falcilysin from Plasmodium falciparum by interference with its closed-to-open dynamic transition. 著者: Jianqing Lin / Xinfu Yan / Zara Chung / Chong Wai Liew / Abbas El Sahili / Evgeniya V Pechnikova / Peter R Preiser / Zbynek Bozdech / Yong-Gui Gao / Julien Lescar /   要旨: In the absence of an efficacious vaccine, chemotherapy remains crucial to prevent and treat malaria. Given its key role in haemoglobin degradation, falcilysin constitutes an attractive target. Here, ...In the absence of an efficacious vaccine, chemotherapy remains crucial to prevent and treat malaria. Given its key role in haemoglobin degradation, falcilysin constitutes an attractive target. Here, we reveal the mechanism of enzymatic inhibition of falcilysin by MK-4815, an investigational new drug with potent antimalarial activity. Using X-ray crystallography, we determine two binary complexes of falcilysin in a closed state, bound with peptide substrates from the haemoglobin α and β chains respectively. An antiparallel β-sheet is formed between the substrate and enzyme, accounting for sequence-independent recognition at positions P2 and P1. In contrast, numerous contacts favor tyrosine and phenylalanine at the P1' position of the substrate. Cryo-EM studies reveal a majority of unbound falcilysin molecules adopting an open conformation. Addition of MK-4815 shifts about two-thirds of falcilysin molecules to a closed state. These structures give atomic level pictures of the proteolytic cycle, in which falcilysin interconverts between a closed state conducive to proteolysis, and an open conformation amenable to substrate diffusion and products release. MK-4815 and quinolines bind to an allosteric pocket next to a hinge region of falcilysin and hinders this dynamic transition. These data should inform the design of potent inhibitors of falcilysin to combat malaria. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_37940.map.gz emd_37940.map.gz | 6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-37940-v30.xml emd-37940-v30.xml emd-37940.xml emd-37940.xml | 18.8 KB 18.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_37940_fsc.xml emd_37940_fsc.xml | 4.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_37940.png emd_37940.png | 20.4 KB | ||
| マスクデータ |  emd_37940_msk_1.map emd_37940_msk_1.map | 8 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-37940.cif.gz emd-37940.cif.gz | 6.1 KB | ||
| その他 |  emd_37940_additional_1.map.gz emd_37940_additional_1.map.gz emd_37940_additional_2.map.gz emd_37940_additional_2.map.gz emd_37940_half_map_1.map.gz emd_37940_half_map_1.map.gz emd_37940_half_map_2.map.gz emd_37940_half_map_2.map.gz | 1.2 MB 7.5 MB 6 MB 6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-37940 http://ftp.pdbj.org/pub/emdb/structures/EMD-37940 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37940 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37940 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_37940.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_37940.map.gz / 形式: CCP4 / 大きさ: 8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.146 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_37940_msk_1.map emd_37940_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
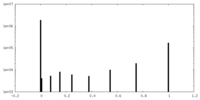
| 密度ヒストグラム |
-追加マップ: #2
| ファイル | emd_37940_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
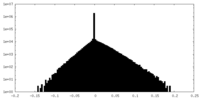
| 密度ヒストグラム |
-追加マップ: #1
| ファイル | emd_37940_additional_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
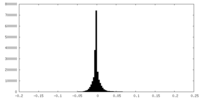
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_37940_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
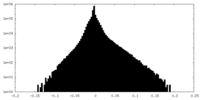
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_37940_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Falcilysin
| 全体 | 名称: Falcilysin |
|---|---|
| 要素 |
|
-超分子 #1: Falcilysin
| 超分子 | 名称: Falcilysin / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Falcilysin
| 分子 | 名称: Falcilysin / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 132.220375 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: EWIHEKSPKH NSYDIIEKRY NEEFKMTYTV YQHKKAKTQV ISLGTNDPLD VEQAFAFYVK TLTHSGKGIP HILEHSVLSG SKNYNYKNS IGLLEKGTLH THLNAYTFND RTVYMAGSMN NKDFFNIMGV YMDSVFQPNV LENKYIFETE GWTYEVEKLK E DEKGKAEI ...文字列: EWIHEKSPKH NSYDIIEKRY NEEFKMTYTV YQHKKAKTQV ISLGTNDPLD VEQAFAFYVK TLTHSGKGIP HILEHSVLSG SKNYNYKNS IGLLEKGTLH THLNAYTFND RTVYMAGSMN NKDFFNIMGV YMDSVFQPNV LENKYIFETE GWTYEVEKLK E DEKGKAEI PQMKDYKVSF NGIVYNEMKG ALSSPLEDLY HEEMKYMFPD NVHSNNSGGD PKEITNLTYE EFKEFYYKNY NP KKVKVFF FSKNNPTELL NFVDQYLGQL DYSKYRDDAV ESVEYQTYKK GPFYIKKKYG DHSEEKENLV SVAWLLNPKV DKT NNHNNN HSNNQSSENN GYSNGSHSSD LSLENPTDYF VLLIINNLLI HTPESVLYKA LTDCGLGNNV IDRGLNDSLV QYIF SIGLK GIKRNNEKIK NFDKVHYEVE DVIMNALKKV VKEGFNKSAV EASINNIEFI LKEANLKTSK SIDFVFEMTS KLNYN RDPL LIFEFEKYLN IVKNKIKNEP MYLEKFVEKH FINNAHRSVI LLEGDENYAQ EQENLEKQEL KKRIENFNEQ EKEQVI KNF EELSKYKNAE ESPEHLNKFP IISISDLNKK TLEVPVNVYF TNINENNNIM ETYNKLKTNE HMLKDNMDVF LKKYVLK ND KHNTNNNNNN NNNMDYSFTE TKYEGNVPIL VYEMPTTGIV YLQFVFSLDH LTVDELAYLN LFKTLILENK TNKRSSED F VILREKNIGS MSANVALYSK DDHLNVTDKY NAQALFNLEM HVLSHKCNDA LNIALEAVKE SDFSNKKKVI DILKRKING MKTTFSEKGY AILMKYVKAH LNSKHYAHNI IYGYENYLKL QEQLELAEND FKTLENILVR IRNKIFNKKN LMVSVTSDYG ALKHLFVNS NESLKNLVSY FEENDKYIND MQNKVNDPTV MGWNEEIKSK KLFDEEKVKK EFFVLPTFVN SVSMSGILFK P GEYLDPSF TVIVAALKNS YLWDTVRGLN GAYGVFADIE YDGSVVFLSA RDPNLEKTLA TFRESAKGLR KMADTMTEND LL RYIINTI GTIDKPRRGI ELSKLSFLRL ISNESEQDRV EFRKRIMNTK KEDFYKFADL LESKVNEFEK NIVIITTKEK ANE YIANVD GEFKKVLI UniProtKB: Falcilysin |
-分子 #2: ZINC ION
| 分子 | 名称: ZINC ION / タイプ: ligand / ID: 2 / コピー数: 1 / 式: ZN |
|---|---|
| 分子量 | 理論値: 65.409 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 20 mM Na HEPES, 300 mM NaCl, 0.5 mM TCEP, pH 7.5 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)