+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3450 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of the K+ transporter KtrAB from Vibrio alginolyticus in the ADP-bound state | |||||||||
 マップデータ マップデータ | KtrB2-KtrA8-KtrB2 complex | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Vibrio alginolyticus (バクテリア) Vibrio alginolyticus (バクテリア) | |||||||||
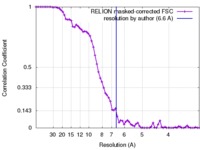
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.6 Å | |||||||||
 データ登録者 データ登録者 | Diskowski M / Mills DJ / Baerland N / Haenelt I / Vonck J | |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2017 ジャーナル: Elife / 年: 2017タイトル: Helical jackknives control the gates of the double-pore K uptake system KtrAB. 著者: Marina Diskowski / Ahmad Reza Mehdipour / Dorith Wunnicke / Deryck J Mills / Vedrana Mikusevic / Natalie Bärland / Jan Hoffmann / Nina Morgner / Heinz-Jürgen Steinhoff / Gerhard Hummer / ...著者: Marina Diskowski / Ahmad Reza Mehdipour / Dorith Wunnicke / Deryck J Mills / Vedrana Mikusevic / Natalie Bärland / Jan Hoffmann / Nina Morgner / Heinz-Jürgen Steinhoff / Gerhard Hummer / Janet Vonck / Inga Hänelt /  要旨: Ion channel gating is essential for cellular homeostasis and is tightly controlled. In some eukaryotic and most bacterial ligand-gated K channels, RCK domains regulate ion fluxes. Until now, a single ...Ion channel gating is essential for cellular homeostasis and is tightly controlled. In some eukaryotic and most bacterial ligand-gated K channels, RCK domains regulate ion fluxes. Until now, a single regulatory mechanism has been proposed for all RCK-regulated channels, involving signal transduction from the RCK domain to the gating area. Here, we present an inactive ADP-bound structure of KtrAB from , determined by cryo-electron microscopy, which, combined with EPR spectroscopy and molecular dynamics simulations, uncovers a novel regulatory mechanism for ligand-induced action at a distance. Exchange of activating ATP to inactivating ADP triggers short helical segments in the K-translocating KtrB dimer to organize into two long helices that penetrate deeply into the regulatory RCK domains, thus connecting nucleotide-binding sites and ion gates. As KtrAB and its homolog TrkAH have been implicated as bacterial pathogenicity factors, the discovery of this functionally relevant inactive conformation may advance structure-guided drug development. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3450.map.gz emd_3450.map.gz | 25.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3450-v30.xml emd-3450-v30.xml emd-3450.xml emd-3450.xml | 15.6 KB 15.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_3450_fsc.xml emd_3450_fsc.xml | 6.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_3450.png emd_3450.png | 131.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3450 http://ftp.pdbj.org/pub/emdb/structures/EMD-3450 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3450 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3450 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3450_validation.pdf.gz emd_3450_validation.pdf.gz | 284.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3450_full_validation.pdf.gz emd_3450_full_validation.pdf.gz | 283.4 KB | 表示 | |
| XML形式データ |  emd_3450_validation.xml.gz emd_3450_validation.xml.gz | 9.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3450 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3450 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3450 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3450 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3450.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3450.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | KtrB2-KtrA8-KtrB2 complex | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.67 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : KtrAB
| 全体 | 名称: KtrAB |
|---|---|
| 要素 |
|
-超分子 #1: KtrAB
| 超分子 | 名称: KtrAB / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: complex of KtrB2A8 with another KtrB transporter dimer attached to the symmetric A8 regulatory domain |
|---|---|
| 由来(天然) | 生物種:  Vibrio alginolyticus (バクテリア) Vibrio alginolyticus (バクテリア) |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 340 KDa |
-分子 #1: KtrB
| 分子 | 名称: KtrB / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Vibrio alginolyticus (バクテリア) Vibrio alginolyticus (バクテリア) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTQFHQRGVF YVPDGKRDKA KGGEPRIILL SFLGVLLPSA VLLTLPVFSV SGLSITDALF TATSAISVT GLGVVDTGQH FTLAGKILLM CLMQIGGLGQ MTLSAVLLYM FGVRLSLRQQ A LAKEALGQ ERQVNLRRLV KKIVTFALVA EAIGFVFLSY RWVPEMGWQT ...文字列: MTQFHQRGVF YVPDGKRDKA KGGEPRIILL SFLGVLLPSA VLLTLPVFSV SGLSITDALF TATSAISVT GLGVVDTGQH FTLAGKILLM CLMQIGGLGQ MTLSAVLLYM FGVRLSLRQQ A LAKEALGQ ERQVNLRRLV KKIVTFALVA EAIGFVFLSY RWVPEMGWQT GMFYALFHSI SA FNNAGFA LFSDSMMSFV NDPLVSFTLA GLFIFGGLGF TVIGDVWRHW RKGFHFLHIH TKI MLIATP LLLLVGTVLF WLLERHNPNT MGSLTTGGQW LAAFFQSASA RTAGFNSVDL TQFT QPALL IMIVLMLIGA GSTSTGGGIK VSTFAVAFMA TWTFLRQKKH VVMFKRTVNW PTVTK SLAI IVVSGAILTT AMFLLMLTEK ASFDKVMFET ISAFATVGLT AGLTAELSEP GKYIMI VVM IIGRIGPLTL AYMLARPEPT LIKYPEDTVL TG |
-分子 #2: KtrA
| 分子 | 名称: KtrA / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Vibrio alginolyticus (バクテリア) Vibrio alginolyticus (バクテリア) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKTGDKQFAV IGLGRFGLAV CKELQDSGSQ VLAVDINEDR VKEAAGFVSQ AIVANCTHEE TVAELKLDD YDMVMIAIGA DVNASILATL IAKEAGVKSV WVKANDRFQA RVLQKIGADH I IMPERDMG IRVARKMLDK RVLEFHPLGS GLAMTEFVVG SRLMGKTLSD ...文字列: MKTGDKQFAV IGLGRFGLAV CKELQDSGSQ VLAVDINEDR VKEAAGFVSQ AIVANCTHEE TVAELKLDD YDMVMIAIGA DVNASILATL IAKEAGVKSV WVKANDRFQA RVLQKIGADH I IMPERDMG IRVARKMLDK RVLEFHPLGS GLAMTEFVVG SRLMGKTLSD LALCKVEGVQ VL GYKRGPE IIKAPDMSTT LEIGDLIIVV GPQDKLANKL KSL |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||||||||
| グリッド | モデル: C-flat CF-MH-4C / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 70 % / チャンバー内温度: 283 K / 装置: FEI VITROBOT MARK IV / 詳細: The sample was blotted for 10 seconds. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 3200FSC |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: In-column Omega Filter |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - 画像ごとのフレーム数: 2-40 / 実像数: 800 / 平均露光時間: 8.0 sec. / 平均電子線量: 27.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 2.5 µm / 最小 デフォーカス(補正後): 1.5 µm / 倍率(補正後): 30675 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 4.2 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.5 µm / 倍率(公称値): 20000 |
| 試料ステージ | 試料ホルダーモデル: JEOL 3200FSC CRYOHOLDER / ホルダー冷却材: NITROGEN |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)