+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Co-structure of the Human Metapneunomovirus RNA-dependent RNA polymerase with MRK-1 | |||||||||
 マップデータ マップデータ | Sharpened map used for model refinement | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | RNA-BINDING PROTEIN / HMPV / RDRP / RNA-DEPENDENT RNA POLYMERASE / PRNTASE / POLYRIBONUCLEOTIDYL TRANSFERASE / RNA CAPPING / VIRAL REPLICATION / VIRAL PROTEIN / REPLICATION | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報GDP polyribonucleotidyltransferase / 加水分解酵素; 酸無水物に作用; リン含有酸無水物に作用 / virion component / host cell cytoplasm / mRNA 5'-cap (guanine-N7-)-methyltransferase activity / RNA-directed RNA polymerase / RNA-directed RNA polymerase activity / GTPase activity / ATP binding / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Human metapneumovirus CAN97-83 (ウイルス) / Human metapneumovirus CAN97-83 (ウイルス) /  Human metapneumovirus (ウイルス) Human metapneumovirus (ウイルス) | |||||||||
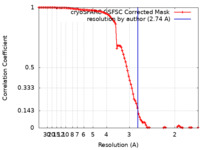
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.74 Å | |||||||||
 データ登録者 データ登録者 | Fischmann TO | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2023 ジャーナル: Commun Biol / 年: 2023タイトル: Conserved allosteric inhibitory site on the respiratory syncytial virus and human metapneumovirus RNA-dependent RNA polymerases. 著者: Victoria A Kleiner / Thierry O Fischmann / John A Howe / Douglas C Beshore / Michael J Eddins / Yan Hou / Todd Mayhood / Daniel Klein / Debbie D Nahas / Bob J Lucas / He Xi / Edward Murray / ...著者: Victoria A Kleiner / Thierry O Fischmann / John A Howe / Douglas C Beshore / Michael J Eddins / Yan Hou / Todd Mayhood / Daniel Klein / Debbie D Nahas / Bob J Lucas / He Xi / Edward Murray / Daphne Y Ma / Krista Getty / Rachel Fearns /  要旨: Respiratory syncytial virus (RSV) and human metapneumovirus (HMPV) are related RNA viruses responsible for severe respiratory infections and resulting disease in infants, elderly, and ...Respiratory syncytial virus (RSV) and human metapneumovirus (HMPV) are related RNA viruses responsible for severe respiratory infections and resulting disease in infants, elderly, and immunocompromised adults. Therapeutic small molecule inhibitors that bind to the RSV polymerase and inhibit viral replication are being developed, but their binding sites and molecular mechanisms of action remain largely unknown. Here we report a conserved allosteric inhibitory site identified on the L polymerase proteins of RSV and HMPV that can be targeted by a dual-specificity, non-nucleoside inhibitor, termed MRK-1. Cryo-EM structures of the inhibitor in complexes with truncated RSV and full-length HMPV polymerase proteins provide a structural understanding of how MRK-1 is active against both viruses. Functional analyses indicate that MRK-1 inhibits conformational changes necessary for the polymerase to engage in RNA synthesis initiation and to transition into an elongation mode. Competition studies reveal that the MRK-1 binding pocket is distinct from that of a capping inhibitor with an overlapping resistance profile, suggesting that the polymerase conformation bound by MRK-1 may be distinct from that involved in mRNA capping. These findings should facilitate optimization of dual RSV and HMPV replication inhibitors and provide insights into the molecular mechanisms underlying their polymerase activities. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29366.map.gz emd_29366.map.gz | 97.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29366-v30.xml emd-29366-v30.xml emd-29366.xml emd-29366.xml | 21.1 KB 21.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_29366_fsc.xml emd_29366_fsc.xml | 9.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_29366.png emd_29366.png | 150.5 KB | ||
| Filedesc metadata |  emd-29366.cif.gz emd-29366.cif.gz | 7.8 KB | ||
| その他 |  emd_29366_half_map_1.map.gz emd_29366_half_map_1.map.gz emd_29366_half_map_2.map.gz emd_29366_half_map_2.map.gz | 95.2 MB 95.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29366 http://ftp.pdbj.org/pub/emdb/structures/EMD-29366 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29366 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29366 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8fpjMC  8fpiC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29366.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29366.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Sharpened map used for model refinement | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.84 Å | ||||||||||||||||||||||||||||||||||||
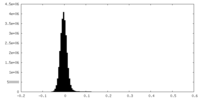
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Unsharpened half-map
| ファイル | emd_29366_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened half-map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
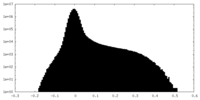
| 密度ヒストグラム |
-ハーフマップ: Unsharpened half-map
| ファイル | emd_29366_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened half-map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : HUMAN METAPNEUMOVIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAME...
| 全体 | 名称: HUMAN METAPNEUMOVIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAMERIC PHOSPHOPROTEIN (P) AND COMPLEXED WITH MRK-1 |
|---|---|
| 要素 |
|
-超分子 #1: HUMAN METAPNEUMOVIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAME...
| 超分子 | 名称: HUMAN METAPNEUMOVIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAMERIC PHOSPHOPROTEIN (P) AND COMPLEXED WITH MRK-1 タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #2 |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus CAN97-83 (ウイルス) Human metapneumovirus CAN97-83 (ウイルス) |
-分子 #1: RNA-directed RNA polymerase L
| 分子 | 名称: RNA-directed RNA polymerase L / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: RNA-directed RNA polymerase |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (ウイルス) Human metapneumovirus (ウイルス) |
| 分子量 | 理論値: 235.226891 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSDYKDHDG DYKDHDIDYK DDDDKGSGSL EVLFQGPMDP LNESTVNVYL PDSYLKGVIS FSETNAIGSC LLKRPYLKND NTAKVAIEN PVIEHVRLKN AVNSKMKISD YKVVEPVNMQ HEIMKNVHSC ELTLLKQFLT RSKNISTLKL NMICDWLQLK S TSDDTSIL ...文字列: MGSDYKDHDG DYKDHDIDYK DDDDKGSGSL EVLFQGPMDP LNESTVNVYL PDSYLKGVIS FSETNAIGSC LLKRPYLKND NTAKVAIEN PVIEHVRLKN AVNSKMKISD YKVVEPVNMQ HEIMKNVHSC ELTLLKQFLT RSKNISTLKL NMICDWLQLK S TSDDTSIL SFIDVEFIPS WVSNWFSNWY NLNKLILEFR REEVIRTGSI LCRSLGKLVF IVSSYGCIVK SNKSKRVSFF TY NQLLTWK DVMLSRFNAN FCIWVSNSLN ENQEGLGLRS NLQGMLTNKL YETVDYMLSL CCNEGFSLVK EFEGFIMSEI LRI TEHAQF STRFRNTLLN GLTDQLTKLK NKNRLRVHST VLENNDYPMY EVVLKLLGDT LRCIKLLINK NLENAAELYY IFRI FGHPM VDERDAMDAV KLNNEITKIL RLESLTELRG AFILRIIKGF VDNNKRWPKI KNLKVLSKRW TMYFKAKNYP SQLEL SEQD FLELAAIQFE QEFSVPEKTN LEMVLNDKAI SPPKRLIWSV YPKNYLPETI KNRYLEETFN ASDSLKTRRV LEYYLK DNK FDQKELKSYV VRQEYLNDKE HIVSLTGKER ELSVGRMFAM QPGKQRQIQI LAEKLLADNI VPFFPETLTK YGDLDLQ RI MEIKSELSSI KTRRNDSYNN YIARASIVTD LSKFNQAFRY ETTAICADVA DELHGTQSLF CWLHLIVPMT TMICAYRH A PPETKGEYDI DKIEEQSGLY RYHMGGIEGW CQKLWTMEAI SLLDVVSVKT RCQMTSLLNG DNQSIDVSKP VKLSEGLDE VKADYRLAVK MLKEIRDAYR NIGHKLKEGE TYISRDLQFI SKVIQSEGVM HPTPIKKVLR VGPWINTILD DIKTSAESIG SLCQELEFR GESIIVSLIL RNFWLYNLYM HESKQHPLAG KQLFKQLNKT LTSVQRFFEI KRENEVVDLW MNIPMQFGGG D PVVFYRSF YRRTPDFLTE AISHVDILLK ISANIKNETK VSFFKALLSI EKNERATLTT LMRDPQAVGS ERQAKVTSDI NR TAVTSIL SLSPNQLFSD SAIHYSRNEE EVGIIAENIT PVYPHGLRVL YESLPFHKAE KVVNMISGTK SITNLLQRTS AIN GEDIDR AVSMMLENLG LLSRILSVVV DSIEIPIKSN GRLICCQISR TLRETSWNNM EIVGVTSPSI TTCMDVIYAT SSHL KGIII EKFSTDRTTR GQRGPKSPWV GSSTQEKKLV PVYNRQILSK QQREQLEAIG KMRWVYKGTP GLRRLLNKIC LGSLG ISYK CVKPLLPRFM SVNFLHRLSV SSRPMEFPAS VPAYRTTNYH FDTSPINQAL SERFGNEDIN LVFQNAISCG ISIMSV VEQ LTGRSPKQLV LIPQLEEIDI MPPPVFQGKF NYKLVDKITS DQHIFSPDKI DMLTLGKMLM PTIKGQKTDQ FLNKREN YF HGNNLIESLS AALACHWCGI LTEQCIENNI FKKDWGDGFI SDHAFMDFKI FLCVFKTKLL CSWGSQGKNI KDEDIVDE S IDKLLRIDNT FWRMFSKVMF EPKVKKRIML YDVKFLSLVG YIGFKNWFIE QLRSAELHEI PWIVNAEGDL VEIKSIKIY LQLIEQSLFL RITVLNYTDM AHALTRLIRK KLMCDNALLT PISSPMVNLT QVIDPTTQLD YFPKITFERL KNYDTSSNYA KGKLTRNYM ILLPWQHVNR YNFVFSSTGC KVSLKTCIGK LMKDLNPKVL YFIGEGAGNW MARTACEYPD IKFVYRSLKD D LDHHYPLE YQRVIGELSR IIDSGEGLSM ETTDATQKTH WDLIHRVSKD ALLITLCDAE FKDRDDFFKM VILWRKHVLS CR ICTTYGT DLYLFAKYHA KDCNVKLPFF VRSVATFIMQ GSKLSGSECY ILLTLGHHNS LPCHGEIQNS KMKIAVCNDF YAA KKLDNK SIEANCKSLL SGLRIPINKK ELDRQRRLLT LQSNHSSVAT VGGSKIIESK WLTNKASTII DWLEHILNSP KGEL NYDFF EALENTYPNM IKLIDNLGNA EIKKLIKVTG YMLVSKK UniProtKB: RNA-directed RNA polymerase L |
-分子 #2: Phosphoprotein
| 分子 | 名称: Phosphoprotein / タイプ: protein_or_peptide / ID: 2 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Human metapneumovirus (ウイルス) Human metapneumovirus (ウイルス) |
| 分子量 | 理論値: 34.814141 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSFPEGKDIL FMGNEAAKLA EAFQKSLRKP SHKRSQSIIG EKVNTVSETL ELPTISRPTK PTILSEPKLA WTDKGGAIKT EAKQTIKVM DPIEEEEFTE KRVLPSSDGK TPAEKKLKPS TNTKKKVSFT PNEPGKYTKL EKDALDLLSD NEEEDAESSI L TFEERDTS ...文字列: MSFPEGKDIL FMGNEAAKLA EAFQKSLRKP SHKRSQSIIG EKVNTVSETL ELPTISRPTK PTILSEPKLA WTDKGGAIKT EAKQTIKVM DPIEEEEFTE KRVLPSSDGK TPAEKKLKPS TNTKKKVSFT PNEPGKYTKL EKDALDLLSD NEEEDAESSI L TFEERDTS SLSIEARLES IEEKLSMILG LLRTLNIATA GPTAARDGIR DAMIGIREEL IADIIKEAKG KAAEMMEEEM NQ RTKIGNG SVKLTEKAKE LNKIVEDEST SGESEEEEEL KDTQENNQED DIYQLIMKGE NKYFQGHHHH HHH UniProtKB: Phosphoprotein |
-分子 #3: 4-(2-aminopropan-2-yl)-N'-[4-(cyclopropyloxy)-3-methoxybenzoyl]-6...
| 分子 | 名称: 4-(2-aminopropan-2-yl)-N'-[4-(cyclopropyloxy)-3-methoxybenzoyl]-6-(4-fluorophenyl)pyridine-2-carbohydrazide タイプ: ligand / ID: 3 / コピー数: 1 / 式: Y6L |
|---|---|
| 分子量 | 理論値: 478.515 Da |
| Chemical component information | 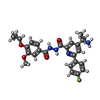 ChemComp-Y6L: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.6 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 検出モード: COUNTING / 平均電子線量: 45.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL |
|---|---|
| 得られたモデル |  PDB-8fpj: |
 ムービー
ムービー コントローラー
コントローラー






 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)