+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2225 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Negative stain microscopy of two Actin-related protein 8 (Arp8) molecules from S. cerevisiae bound to a mono-nucleosome. | |||||||||
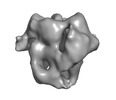
 マップデータ マップデータ | Reconstruction of a yeast mono-nucleosome in complex with two molecules of yeast Arp8. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Chromatin remodelling / INO80 complex / Actin related protein / Arp8 / Nucleosome / Nucleosome binding | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 21.0 Å | |||||||||
 データ登録者 データ登録者 | Bose DA / Saravanan M / Wuerges J / McCormack EA / Cook NJ / Zhang X / Wigley DB | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2012 ジャーナル: Proc Natl Acad Sci U S A / 年: 2012タイトル: Interactions between the nucleosome histone core and Arp8 in the INO80 chromatin remodeling complex. 著者: Matheshwaran Saravanan / Jochen Wuerges / Daniel Bose / Elizabeth A McCormack / Nicola J Cook / Xiaodong Zhang / Dale B Wigley /  要旨: Actin-related protein Arp8 is a component of the INO80 chromatin remodeling complex. Yeast Arp8 (yArp8) comprises two domains: a 25-KDa N-terminal domain, found only in yeast, and a 75-KDa C-terminal ...Actin-related protein Arp8 is a component of the INO80 chromatin remodeling complex. Yeast Arp8 (yArp8) comprises two domains: a 25-KDa N-terminal domain, found only in yeast, and a 75-KDa C-terminal domain (yArp8CTD) that contains the actin fold and is conserved across other species. The crystal structure shows that yArp8CTD contains three insertions within the actin core. Using a combination of biochemistry and EM, we show that Arp8 forms a complex with nucleosomes, and that the principal interactions are via the H3 and H4 histones, mediated through one of the yArp8 insertions. We show that recombinant yArp8 exists in monomeric and dimeric states, but the dimer is the biologically relevant form required for stable interactions with histones that exploits the twofold symmetry of the nucleosome core. Taken together, these data provide unique insight into the stoichiometry, architecture, and molecular interactions between components of the INO80 remodeling complex and nucleosomes, providing a first step toward building up the structure of the complex. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2225.map.gz emd_2225.map.gz | 619.6 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2225-v30.xml emd-2225-v30.xml emd-2225.xml emd-2225.xml | 11.1 KB 11.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_2225.tif emd_2225.tif | 656 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2225 http://ftp.pdbj.org/pub/emdb/structures/EMD-2225 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2225 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2225 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2225_validation.pdf.gz emd_2225_validation.pdf.gz | 189 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2225_full_validation.pdf.gz emd_2225_full_validation.pdf.gz | 188.1 KB | 表示 | |
| XML形式データ |  emd_2225_validation.xml.gz emd_2225_validation.xml.gz | 5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2225 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2225 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2225 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2225 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2225.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2225.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of a yeast mono-nucleosome in complex with two molecules of yeast Arp8. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.52 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Complex of yeast Actin Related Protein 8 (Arp8) C-terminal domain...
| 全体 | 名称: Complex of yeast Actin Related Protein 8 (Arp8) C-terminal domain bound to a yeast mono-nucleosome. |
|---|---|
| 要素 |
|
-超分子 #1000: Complex of yeast Actin Related Protein 8 (Arp8) C-terminal domain...
| 超分子 | 名称: Complex of yeast Actin Related Protein 8 (Arp8) C-terminal domain bound to a yeast mono-nucleosome. タイプ: sample / ID: 1000 集合状態: Two molecules of Arp8 bind a single nucleosome. Number unique components: 2 |
|---|---|
| 分子量 | 理論値: 400 KDa |
-分子 #1: Actin-like protein ARP8
| 分子 | 名称: Actin-like protein ARP8 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 集合状態: dimer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 100 KDa |
| 組換発現 | 生物種:  |
-分子 #2: nucleosome
| 分子 | 名称: nucleosome / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 集合状態: 1 / 組換発現: No |
|---|---|
| 由来(天然) | 生物種:  |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.02 mg/mL |
|---|---|
| 染色 | タイプ: NEGATIVE 詳細: 2 ul of ~0.02mg/ml Arp8CTD/nucleosome complex was applied to glow-discharged continuous carbon grids (TAAB). Sample was adsorbed for 20s, then stained with 2% w/v uranyl acetate for 40s ...詳細: 2 ul of ~0.02mg/ml Arp8CTD/nucleosome complex was applied to glow-discharged continuous carbon grids (TAAB). Sample was adsorbed for 20s, then stained with 2% w/v uranyl acetate for 40s before blotting and air drying. |
| グリッド | 詳細: Copper 300 mesh continuous carbon grids (TAAB) |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM200FEG |
|---|---|
| 日付 | 2010年3月23日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: TVIPS TEMCAM-F415 (4k x 4k) 平均電子線量: 10 e/Å2 詳細: Data collected on a 4k x 4k CCD camera at 50000x magnification. Sampling interval was 1.76A/pixel. ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.1 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダー: single tilt / 試料ホルダーモデル: SIDE ENTRY, EUCENTRIC |
- 画像解析
画像解析
| CTF補正 | 詳細: Each particle |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C2 (2回回転対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 21.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: IMAGIC, V, TIGRIS, EMAN / 使用した粒子像数: 4165 |
| 最終 角度割当 | 詳細: Imagic |
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称: Chimera, CNS, Situs |
| 詳細 | Protocol: Rigid body. The Arp8 crystal structure was positioned interactively in Chimera, then the fit was refined using Situs and CNS. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
-原子モデル構築 2
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称: Chimera, CNS, Situs |
| 詳細 | Protocol: Rigid body. The Arp8 crystal structure was positioned interactively in Chimera, then the fit was refined using Situs and CNS. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















