+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2059 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of HBV T=4 pgRNA-filled Cp183 capsid | |||||||||
 マップデータ マップデータ | Cryo-EM structure of HBV T=4 pgRNA-filled Cp183 capsid (Cp183RNA-SSS) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | HBV / Cp183 / pgRNA | |||||||||
| 生物種 |   Hepatitis B virus (B 型肝炎ウイルス) Hepatitis B virus (B 型肝炎ウイルス) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 8.0 Å | |||||||||
 データ登録者 データ登録者 | Wang JC-Y / Dhasan RS / Zlotnick A | |||||||||
 引用 引用 |  ジャーナル: PLoS Pathog / 年: 2012 ジャーナル: PLoS Pathog / 年: 2012タイトル: Structural organization of pregenomic RNA and the carboxy-terminal domain of the capsid protein of hepatitis B virus. 著者: Joseph C-Y Wang / Mary S Dhason / Adam Zlotnick /  要旨: The Hepatitis B Virus (HBV) double-stranded DNA genome is reverse transcribed from its RNA pregenome (pgRNA) within the virus core (or capsid). Phosphorylation of the arginine-rich carboxy-terminal ...The Hepatitis B Virus (HBV) double-stranded DNA genome is reverse transcribed from its RNA pregenome (pgRNA) within the virus core (or capsid). Phosphorylation of the arginine-rich carboxy-terminal domain (CTD) of the HBV capsid protein (Cp183) is essential for pgRNA encapsidation and reverse transcription. However, the structure of the CTD remains poorly defined. Here we report sub-nanometer resolution cryo-EM structures of in vitro assembled empty and pgRNA-filled Cp183 capsids in unphosphorylated and phosphorylation-mimic states. In empty capsids, we found unexpected evidence of surface accessible CTD density partially occluding pores in the capsid surface. We also observed that CTD organization changed substantively as a function of phosphorylation. In RNA-filled capsids, unphosphorylated CTDs favored thick ropes of RNA, while the phosphorylation-mimic favored a mesh of thin, high-density strands suggestive of single stranded RNA. These results demonstrate that the CTD can regulate nucleic acid structure, supporting the hypothesis that the HBV capsid has a functional role as a nucleic acid chaperone. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2059.map.gz emd_2059.map.gz | 41.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2059-v30.xml emd-2059-v30.xml emd-2059.xml emd-2059.xml | 10.7 KB 10.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  EMD-2059.jpg EMD-2059.jpg | 266.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2059 http://ftp.pdbj.org/pub/emdb/structures/EMD-2059 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2059 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2059 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2059_validation.pdf.gz emd_2059_validation.pdf.gz | 225.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2059_full_validation.pdf.gz emd_2059_full_validation.pdf.gz | 224.2 KB | 表示 | |
| XML形式データ |  emd_2059_validation.xml.gz emd_2059_validation.xml.gz | 7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2059 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2059 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2059 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2059 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2059.map.gz / 形式: CCP4 / 大きさ: 101.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2059.map.gz / 形式: CCP4 / 大きさ: 101.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cryo-EM structure of HBV T=4 pgRNA-filled Cp183 capsid (Cp183RNA-SSS) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.4836 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
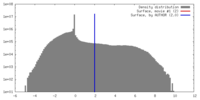
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : HBV T=4 pgRNA-filled Cp183 capsid
| 全体 | 名称: HBV T=4 pgRNA-filled Cp183 capsid |
|---|---|
| 要素 |
|
-超分子 #1000: HBV T=4 pgRNA-filled Cp183 capsid
| 超分子 | 名称: HBV T=4 pgRNA-filled Cp183 capsid / タイプ: sample / ID: 1000 / Number unique components: 1 |
|---|
-超分子 #1: Hepatitis B virus
| 超分子 | 名称: Hepatitis B virus / タイプ: virus / ID: 1 / Name.synonym: HBV Cp183 詳細: Reassembled the purified Cp183 dimers with in vitro transcribed HBV pgRNA at a molar ratio of protein dimer to RNA polymer = 120:1 NCBI-ID: 10407 / 生物種: Hepatitis B virus / ウイルスタイプ: VIRUS-LIKE PARTICLE / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: Yes / ウイルス・中空状態: Yes / Syn species name: HBV Cp183 |
|---|---|
| 宿主 | 生物種:  Homo sapiens (ヒト) / 別称: VERTEBRATES Homo sapiens (ヒト) / 別称: VERTEBRATES |
| ウイルス殻 | Shell ID: 1 / 名称: Cp183 / T番号(三角分割数): 4 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 / 詳細: 150 mM NaCl, 50 mM HEPES, 2 mM DTT |
|---|---|
| グリッド | 詳細: Quantifoil R 2/2 holey carbon 200 mesh copper grids |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 93 K / 装置: FEI VITROBOT MARK III / 手法: Blot for 4 seconds before plunging |
- 電子顕微鏡法 #1
電子顕微鏡法 #1
| Microscopy ID | 1 |
|---|---|
| 顕微鏡 | JEOL 3200FS |
| 温度 | 平均: 97 K |
| アライメント法 | Legacy - 非点収差: objective lens astigmatism was corrected at 80,000 times magnification |
| 特殊光学系 | エネルギーフィルター - 名称: Omega filter |
| 日付 | 2010年4月27日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 実像数: 193 / 平均電子線量: 14 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 1.1 mm / 最大 デフォーカス(公称値): 3.8 µm / 最小 デフォーカス(公称値): 0.27 µm / 倍率(公称値): 40000 |
| 試料ステージ | 試料ホルダー: Side entry liquid nitrogen-cooled cryo specimen holder 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 電子顕微鏡法 #2
電子顕微鏡法 #2
| Microscopy ID | 2 |
|---|---|
| 顕微鏡 | JEOL 3200FS |
| 温度 | 平均: 97 K |
| アライメント法 | Legacy - 非点収差: objective lens astigmatism was corrected at 80,000 times magnification |
| 特殊光学系 | エネルギーフィルター - 名称: Omega filter |
| 日付 | 2010年5月4日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 実像数: 193 / 平均電子線量: 14 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 1.1 mm / 最大 デフォーカス(公称値): 3.8 µm / 最小 デフォーカス(公称値): 0.27 µm / 倍率(公称値): 40000 |
| 試料ステージ | 試料ホルダー: Side entry liquid nitrogen-cooled cryo specimen holder 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| CTF補正 | 詳細: Each particle phase-flipping |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: I (正20面体型対称) / 解像度のタイプ: BY AUTHOR / 解像度: 8.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: Auto3dem / 使用した粒子像数: 7201 |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)