+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Mouse teneurin-3 non-compact subunit - A0B1 isoform | |||||||||
 マップデータ マップデータ | Map of mouse teneurin-3 A0B1 isoform ectodomain non-compact subunit | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Synaptic cell adhesion molecule / Homodimer / Cis-synaptic / CELL ADHESION | |||||||||
| 生物種 |  | |||||||||
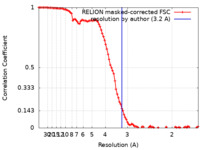
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.2 Å | |||||||||
 データ登録者 データ登録者 | Gogou C / Meijer DH | |||||||||
| 資金援助 |  オランダ, 1件 オランダ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Alternative splicing controls teneurin-3 compact dimer formation for neuronal recognition. 著者: Christos Gogou / J Wouter Beugelink / Cátia P Frias / Leanid Kresik / Natalia Jaroszynska / Uwe Drescher / Bert J C Janssen / Robert Hindges / Dimphna H Meijer /   要旨: Neuronal network formation is facilitated by recognition between synaptic cell adhesion molecules at the cell surface. Alternative splicing of cell adhesion molecules provides additional specificity ...Neuronal network formation is facilitated by recognition between synaptic cell adhesion molecules at the cell surface. Alternative splicing of cell adhesion molecules provides additional specificity in forming neuronal connections. For the teneurin family of cell adhesion molecules, alternative splicing of the EGF-repeats and NHL domain controls synaptic protein-protein interactions. Here we present cryo-EM structures of the compact dimeric ectodomain of two teneurin-3 isoforms that harbour the splice insert in the EGF-repeats. This dimer is stabilised by an EGF8-ABD contact between subunits. Cryo-EM reconstructions of all four splice variants, together with SAXS and negative stain EM, reveal compacted dimers for each, with variant-specific dimeric arrangements. This results in specific trans-cellular interactions, as tested in cell clustering and stripe assays. The compact conformations provide a structural basis for teneurin homo- and heterophilic interactions. Altogether, our findings demonstrate how alternative splicing results in rearrangements of the dimeric subunits, influencing neuronal recognition and likely circuit wiring. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_18900.map.gz emd_18900.map.gz | 78.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-18900-v30.xml emd-18900-v30.xml emd-18900.xml emd-18900.xml | 14.5 KB 14.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_18900_fsc.xml emd_18900_fsc.xml | 10 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_18900.png emd_18900.png | 108.6 KB | ||
| Filedesc metadata |  emd-18900.cif.gz emd-18900.cif.gz | 4.1 KB | ||
| その他 |  emd_18900_half_map_1.map.gz emd_18900_half_map_1.map.gz emd_18900_half_map_2.map.gz emd_18900_half_map_2.map.gz | 65.5 MB 65.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-18900 http://ftp.pdbj.org/pub/emdb/structures/EMD-18900 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18900 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18900 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_18900_validation.pdf.gz emd_18900_validation.pdf.gz | 1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_18900_full_validation.pdf.gz emd_18900_full_validation.pdf.gz | 1 MB | 表示 | |
| XML形式データ |  emd_18900_validation.xml.gz emd_18900_validation.xml.gz | 17.1 KB | 表示 | |
| CIF形式データ |  emd_18900_validation.cif.gz emd_18900_validation.cif.gz | 22.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18900 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18900 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18900 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18900 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_18900.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_18900.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map of mouse teneurin-3 A0B1 isoform ectodomain non-compact subunit | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.836 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map of mouse teneurin-3 A0B1 isoform ectodomain...
| ファイル | emd_18900_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map of mouse teneurin-3 A0B1 isoform ectodomain non-compact subunit | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map of mouse teneurin-3 A0B1 isoform ectodomain...
| ファイル | emd_18900_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map of mouse teneurin-3 A0B1 isoform ectodomain non-compact subunit | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : mouse teneurin-3 A1B1 isoform ectodomain subunit
| 全体 | 名称: mouse teneurin-3 A1B1 isoform ectodomain subunit |
|---|---|
| 要素 |
|
-超分子 #1: mouse teneurin-3 A1B1 isoform ectodomain subunit
| 超分子 | 名称: mouse teneurin-3 A1B1 isoform ectodomain subunit / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 536.96 KDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.8 / 詳細: 20 mM HEPES, 150 mM NaCl, 2mM CaCl2 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)