+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | ApdP-SRC with P-tRNA only | |||||||||
 マップデータ マップデータ | Main map, post-processed | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Stalling / nascent chain / translation arrest / regulation / RIBOSOME | |||||||||
| 生物種 |  Sinorhizobium medicae (根粒菌) Sinorhizobium medicae (根粒菌) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Morici M / Wilson DN | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: RAPP-containing arrest peptides induce translational stalling by short circuiting the ribosomal peptidyltransferase activity. 著者: Martino Morici / Sara Gabrielli / Keigo Fujiwara / Helge Paternoga / Bertrand Beckert / Lars V Bock / Shinobu Chiba / Daniel N Wilson /   要旨: Arrest peptides containing RAPP (ArgAlaProPro) motifs have been discovered in both Gram-positive and Gram-negative bacteria, where they are thought to regulate expression of important protein ...Arrest peptides containing RAPP (ArgAlaProPro) motifs have been discovered in both Gram-positive and Gram-negative bacteria, where they are thought to regulate expression of important protein localization machinery components. Here we determine cryo-EM structures of ribosomes stalled on RAPP arrest motifs in both Bacillus subtilis and Escherichia coli. Together with molecular dynamics simulations, our structures reveal that the RAPP motifs allow full accommodation of the A-site tRNA, but prevent the subsequent peptide bond from forming. Our data support a model where the RAP in the P-site interacts and stabilizes a single hydrogen atom on the Pro-tRNA in the A-site, thereby preventing an optimal geometry for the nucleophilic attack required for peptide bond formation to occur. This mechanism to short circuit the ribosomal peptidyltransferase activity is likely to operate for the majority of other RAPP-like arrest peptides found across diverse bacterial phylogenies. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_18340.map.gz emd_18340.map.gz | 47.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-18340-v30.xml emd-18340-v30.xml emd-18340.xml emd-18340.xml | 21.3 KB 21.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_18340.png emd_18340.png | 69.6 KB | ||
| Filedesc metadata |  emd-18340.cif.gz emd-18340.cif.gz | 4.2 KB | ||
| その他 |  emd_18340_additional_1.map.gz emd_18340_additional_1.map.gz emd_18340_half_map_1.map.gz emd_18340_half_map_1.map.gz emd_18340_half_map_2.map.gz emd_18340_half_map_2.map.gz | 141 MB 141.4 MB 141.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-18340 http://ftp.pdbj.org/pub/emdb/structures/EMD-18340 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18340 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18340 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_18340_validation.pdf.gz emd_18340_validation.pdf.gz | 1.2 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_18340_full_validation.pdf.gz emd_18340_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  emd_18340_validation.xml.gz emd_18340_validation.xml.gz | 14.8 KB | 表示 | |
| CIF形式データ |  emd_18340_validation.cif.gz emd_18340_validation.cif.gz | 17.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18340 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18340 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18340 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18340 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_18340.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_18340.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Main map, post-processed | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.82 Å | ||||||||||||||||||||||||||||||||||||
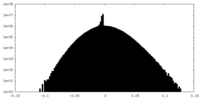
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: Preprocessed nao
| ファイル | emd_18340_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Preprocessed nao | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
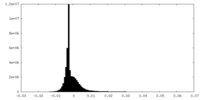
| 密度ヒストグラム |
-ハーフマップ: Half-map 1
| ファイル | emd_18340_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
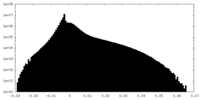
| 密度ヒストグラム |
-ハーフマップ: Half-map 2
| ファイル | emd_18340_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
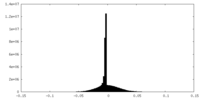
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : E. coli ApdP-stalled ribosomal complex
| 全体 | 名称: E. coli ApdP-stalled ribosomal complex |
|---|---|
| 要素 |
|
-超分子 #1: E. coli ApdP-stalled ribosomal complex
| 超分子 | 名称: E. coli ApdP-stalled ribosomal complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#51 |
|---|---|
| 由来(天然) | 生物種:  Sinorhizobium medicae (根粒菌) Sinorhizobium medicae (根粒菌) |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE-PROPANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 75.6 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 0.6 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER 詳細: Exprimental unpublished map from our lab from an analogous ample, previously low-pass filtered |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 17657 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)