+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Chimaera of AP2 with FCHO2 linker domain as a fusion on Cmu2 subunit | |||||||||
 マップデータ マップデータ | Local resolution filtered overall map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | adaptor complex / AP2 / trafficking / clathrin / CCP / PROTEIN TRANSPORT | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Gap junction degradation / Formation of annular gap junctions / LDL clearance / WNT5A-dependent internalization of FZD2, FZD5 and ROR2 / WNT5A-dependent internalization of FZD2, FZD5 and ROR2 / LDL clearance / WNT5A-dependent internalization of FZD4 / Retrograde neurotrophin signalling / VLDLR internalisation and degradation / Nef Mediated CD8 Down-regulation ...Gap junction degradation / Formation of annular gap junctions / LDL clearance / WNT5A-dependent internalization of FZD2, FZD5 and ROR2 / WNT5A-dependent internalization of FZD2, FZD5 and ROR2 / LDL clearance / WNT5A-dependent internalization of FZD4 / Retrograde neurotrophin signalling / VLDLR internalisation and degradation / Nef Mediated CD8 Down-regulation / Trafficking of GluR2-containing AMPA receptors / Retrograde neurotrophin signalling / clathrin adaptor complex / WNT5A-dependent internalization of FZD4 / WNT5A-dependent internalization of FZD2, FZD5 and ROR2 / Trafficking of GluR2-containing AMPA receptors / extrinsic component of presynaptic endocytic zone membrane / VLDLR internalisation and degradation / WNT5A-dependent internalization of FZD4 / MHC class II antigen presentation / Recycling pathway of L1 / AP-2 adaptor complex / regulation of vesicle size / postsynaptic neurotransmitter receptor internalization / Recycling pathway of L1 / LDL clearance / Cargo recognition for clathrin-mediated endocytosis / Retrograde neurotrophin signalling / Cargo recognition for clathrin-mediated endocytosis / clathrin-coated endocytic vesicle / Clathrin-mediated endocytosis / clathrin adaptor activity / Clathrin-mediated endocytosis / positive regulation of synaptic vesicle endocytosis / membrane coat / vesicle budding from membrane / clathrin-dependent endocytosis / coronary vasculature development / MHC class II antigen presentation / endolysosome membrane / signal sequence binding / Nef Mediated CD4 Down-regulation / aorta development / ventricular septum development / low-density lipoprotein particle receptor binding / Neutrophil degranulation / clathrin binding / positive regulation of receptor internalization / Trafficking of GluR2-containing AMPA receptors / Recycling pathway of L1 / synaptic vesicle endocytosis / EPH-ephrin mediated repulsion of cells / negative regulation of protein localization to plasma membrane / protein serine/threonine kinase binding / clathrin-coated pit / vesicle-mediated transport / MHC class II antigen presentation / VLDLR internalisation and degradation / phosphatidylinositol binding / kidney development / intracellular protein transport / clathrin-coated endocytic vesicle membrane / kinase binding / terminal bouton / receptor internalization / cytoplasmic side of plasma membrane / disordered domain specific binding / endocytic vesicle membrane / Cargo recognition for clathrin-mediated endocytosis / synaptic vesicle / Clathrin-mediated endocytosis / presynapse / cytoplasmic vesicle / protein-containing complex assembly / postsynapse / transmembrane transporter binding / Potential therapeutics for SARS / protein domain specific binding / intracellular membrane-bounded organelle / lipid binding / glutamatergic synapse / synapse / protein-containing complex binding / protein kinase binding / membrane / plasma membrane / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |    Homo sapiens (ヒト) / Homo sapiens (ヒト) /  | |||||||||
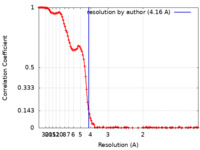
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.16 Å | |||||||||
 データ登録者 データ登録者 | Kane Dickson V / Qu K / Owen DJ / Briggs JA / Zaccai NR | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2022 ジャーナル: Sci Adv / 年: 2022タイトル: FCHO controls AP2's initiating role in endocytosis through a PtdIns(4,5)P-dependent switch. 著者: Nathan R Zaccai / Zuzana Kadlecova / Veronica Kane Dickson / Kseniya Korobchevskaya / Jan Kamenicky / Oleksiy Kovtun / Perunthottathu K Umasankar / Antoni G Wrobel / Jonathan G G Kaufman / ...著者: Nathan R Zaccai / Zuzana Kadlecova / Veronica Kane Dickson / Kseniya Korobchevskaya / Jan Kamenicky / Oleksiy Kovtun / Perunthottathu K Umasankar / Antoni G Wrobel / Jonathan G G Kaufman / Sally R Gray / Kun Qu / Philip R Evans / Marco Fritzsche / Filip Sroubek / Stefan Höning / John A G Briggs / Bernard T Kelly / David J Owen / Linton M Traub /      要旨: Clathrin-mediated endocytosis (CME) is the main mechanism by which mammalian cells control their cell surface proteome. Proper operation of the pivotal CME cargo adaptor AP2 requires membrane- ...Clathrin-mediated endocytosis (CME) is the main mechanism by which mammalian cells control their cell surface proteome. Proper operation of the pivotal CME cargo adaptor AP2 requires membrane-localized Fer/Cip4 homology domain-only proteins (FCHO). Here, live-cell enhanced total internal reflection fluorescence-structured illumination microscopy shows that FCHO marks sites of clathrin-coated pit (CCP) initiation, which mature into uniform-sized CCPs comprising a central patch of AP2 and clathrin corralled by an FCHO/Epidermal growth factor potential receptor substrate number 15 (Eps15) ring. We dissect the network of interactions between the FCHO interdomain linker and AP2, which concentrates, orients, tethers, and partially destabilizes closed AP2 at the plasma membrane. AP2's subsequent membrane deposition drives its opening, which triggers FCHO displacement through steric competition with phosphatidylinositol 4,5-bisphosphate, clathrin, cargo, and CME accessory factors. FCHO can now relocate toward a CCP's outer edge to engage and activate further AP2s to drive CCP growth/maturation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_14517.map.gz emd_14517.map.gz | 11 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-14517-v30.xml emd-14517-v30.xml emd-14517.xml emd-14517.xml | 20 KB 20 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_14517_fsc.xml emd_14517_fsc.xml | 15.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_14517.png emd_14517.png | 125.6 KB | ||
| Filedesc metadata |  emd-14517.cif.gz emd-14517.cif.gz | 7 KB | ||
| その他 |  emd_14517_half_map_1.map.gz emd_14517_half_map_1.map.gz emd_14517_half_map_2.map.gz emd_14517_half_map_2.map.gz | 139 MB 139 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-14517 http://ftp.pdbj.org/pub/emdb/structures/EMD-14517 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14517 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-14517 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_14517_validation.pdf.gz emd_14517_validation.pdf.gz | 895.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_14517_full_validation.pdf.gz emd_14517_full_validation.pdf.gz | 894.9 KB | 表示 | |
| XML形式データ |  emd_14517_validation.xml.gz emd_14517_validation.xml.gz | 19.3 KB | 表示 | |
| CIF形式データ |  emd_14517_validation.cif.gz emd_14517_validation.cif.gz | 25.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14517 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14517 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14517 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-14517 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7z5cMC  7ofpC  7og1C  7ohiC  7ohoC  7ohzC  7oi5C  7oiqC  7oitC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_14517.map.gz / 形式: CCP4 / 大きさ: 149.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_14517.map.gz / 形式: CCP4 / 大きさ: 149.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Local resolution filtered overall map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.652 Å | ||||||||||||||||||||||||||||||||||||
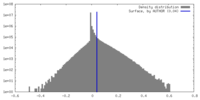
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map A
| ファイル | emd_14517_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
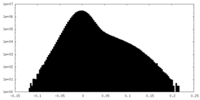
| 投影像・断面図 |
| ||||||||||||
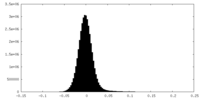
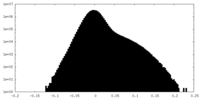
| 密度ヒストグラム |
-ハーフマップ: Half map B
| ファイル | emd_14517_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
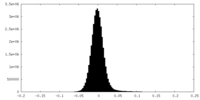
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : AP2 core complex
| 全体 | 名称: AP2 core complex |
|---|---|
| 要素 |
|
-超分子 #1: AP2 core complex
| 超分子 | 名称: AP2 core complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Ternary complex of AP2 core expressed as part of a chimaera with FCHO2 linker (not modelled) |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 203 KDa |
-分子 #1: AP-2 complex subunit alpha-2
| 分子 | 名称: AP-2 complex subunit alpha-2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 69.656297 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MPAVSKGEGM RGLAVFISDI RNCKSKEAEI KRINKELANI RSKFKGDKAL DGYSKKKYVC KLLFIFLLGH DIDFGHMEAV NLLSSNRYT EKQIGYLFIS VLVNSNSELI RLINNAIKND LASRNPTFMG LALHCIANVG SREMAEAFAG EIPKILVAGD T MDSVKQSA ...文字列: MPAVSKGEGM RGLAVFISDI RNCKSKEAEI KRINKELANI RSKFKGDKAL DGYSKKKYVC KLLFIFLLGH DIDFGHMEAV NLLSSNRYT EKQIGYLFIS VLVNSNSELI RLINNAIKND LASRNPTFMG LALHCIANVG SREMAEAFAG EIPKILVAGD T MDSVKQSA ALCLLRLYRT SPDLVPMGDW TSRVVHLLND QHLGVVTAAT SLITTLAQKN PEEFKTSVSL AVSRLSRIVT SA STDLQDY TYYFVPAPWL SVKLLRLLQC YPPPEDPAVR GRLTECLETI LNKAQEPPKS KKVQHSNAKN AVLFEAISLI IHH DSEPNL LVRACNQLGQ FLQHRETNLR YLALESMCTL ASSEFSHEAV KTHIETVINA LKTERDVSVR QRAVDLLYAM CDRS NAQQI VAEMLSYLET ADYSIREEIV LKVAILAEKY AVDYTWYVDT ILNLIRIAGD YVSEEVWYRV IQIVINRDDV QGYAA KTVF EALQAPACHE NLVKVGGYIL GEFGNLIAGD PRSSPLIQFN LLHSKFHLCS VPTRALLLST YIKFVNLFPE VKATIQ DVL RSDSQLKNAD VELQQRAVEY LRLSTVASTD ILATVLEEMP PFPERESSIL AKLKKKKG UniProtKB: AP-2 complex subunit alpha-2 |
-分子 #2: AP-2 complex subunit beta
| 分子 | 名称: AP-2 complex subunit beta / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 66.953195 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTDSKYFTTN KKGEIFELKA ELNNEKKEKR KEAVKKVIAA MTVGKDVSSL FPDVVNCMQT DNLELKKLVY LYLMNYAKSQ PDMAIMAVN SFVKDCEDPN PLIRALAVRT MGCIRVDKIT EYLCEPLRKC LKDEDPYVRK TAAVCVAKLH DINAQMVEDQ G FLDSLRDL ...文字列: MTDSKYFTTN KKGEIFELKA ELNNEKKEKR KEAVKKVIAA MTVGKDVSSL FPDVVNCMQT DNLELKKLVY LYLMNYAKSQ PDMAIMAVN SFVKDCEDPN PLIRALAVRT MGCIRVDKIT EYLCEPLRKC LKDEDPYVRK TAAVCVAKLH DINAQMVEDQ G FLDSLRDL IADSNPMVVA NAVAALSEIS ESHPNSNLLD LNPQNINKLL TALNECTEWG QIFILDCLSN YNPKDDREAQ SI CERVTPR LSHANSAVVL SAVKVLMKFL ELLPKDSDYY NMLLKKLAPP LVTLLSGEPE VQYVALRNIN LIVQKRPEIL KQE IKVFFV KYNDPIYVKL EKLDIMIRLA SQANIAQVLA ELKEYATEVD VDFVRKAVRA IGRCAIKVEQ SAERCVSTLL DLIQ TKVNY VVQEAIVVIR DIFRKYPNKY ESIIATLCEN LDSLDEPDAR AAMIWIVGEY AERIDNADEL LESFLEGFHD ESTQV QLTL LTAIVKLFLK KPSETQELVQ QVLSLATQDS DNPDLRDRGY IYWRLLSTDP VTAKEVVLSE KPLISEETDL IEPTLL DEL ICHIGSLASV YHKPPNAFVE GSHGIHRK UniProtKB: AP-2 complex subunit beta |
-分子 #3: AP-2 complex subunit mu
| 分子 | 名称: AP-2 complex subunit mu / タイプ: protein_or_peptide / ID: 3 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 49.726641 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MIGGLFIYNH KGEVLISRVY RDDIGRNAVD AFRVNVIHAR QQVRSPVTNI ARTSFFHVKR SNIWLAAVTK QNVNAAMVFE FLYKMCDVM AAYFGKISEE NIKNNFVLIY ELLDEILDFG YPQNSETGAL KTFITQQGIK SQHQTKEEQS QITSQVTGQI G WRREGIKY ...文字列: MIGGLFIYNH KGEVLISRVY RDDIGRNAVD AFRVNVIHAR QQVRSPVTNI ARTSFFHVKR SNIWLAAVTK QNVNAAMVFE FLYKMCDVM AAYFGKISEE NIKNNFVLIY ELLDEILDFG YPQNSETGAL KTFITQQGIK SQHQTKEEQS QITSQVTGQI G WRREGIKY RRNELFLDVL ESVNLLMSPQ GQVLSAHVSG RVVMKSYLSG MPECKFGMND KIVIEKQGKG TADETSKSGK QS IAIDDCT FHQCVRLSKF DSERSISFIP PDGEFELMRY RTTKDIILPF RVIPLVREVG RTKLEVKVVI KSNFKPSLLA QKI EVRIPT PLNTSGVQVI CMKGKAKYKA SENAIVWKIK RMAGMKESQI SAEIELLPTN DKKKWARPPI SMNFEVPFAP SGLK VRYLK VFEPKLNYSD HDVIKWVRYI GRSGIYETRC UniProtKB: AP-2 complex subunit mu |
-分子 #4: AP-2 complex subunit sigma
| 分子 | 名称: AP-2 complex subunit sigma / タイプ: protein_or_peptide / ID: 4 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 17.038688 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MIRFILIQNR AGKTRLAKWY MQFDDDEKQK LIEEVHAVVT VRDAKHTNFV EFRNFKIIYR RYAGLYFCIC VDVNDNNLAY LEAIHNFVE VLNEYFHNVC ELDLVFNFYK VYTVVDEMFL AGEIRETSQT KVLKQLLMLQ SLE UniProtKB: AP-2 complex subunit sigma |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.4 mg/mL |
|---|---|
| 緩衝液 | pH: 7.6 詳細: 50% HKT buffer (10mM Hepes, 10mM Tris 120mM potassium acetate pH 7.2) and 50% Core buffer (10mM Tris, 250mM NaCl, pH 8) |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
| 詳細 | This sample was monodisperse. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 47.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.9 µm / 最小 デフォーカス(公称値): 0.9 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


































 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)