+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-12583 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of Nipah virus nucleocapsid 1.5 helical turn spiral assembly | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative stranded viral RNA transcription / negative stranded viral RNA replication / helical viral capsid / viral nucleocapsid / molecular adaptor activity / host cell cytoplasm / ribonucleoprotein complex / structural molecule activity / RNA binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Nipah henipavirus (ウイルス) Nipah henipavirus (ウイルス) | |||||||||
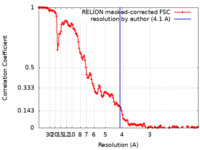
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.1 Å | |||||||||
 データ登録者 データ登録者 | Ker DS / Jenkins HT / Greive SJ / Antson AA | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: PLoS Pathog / 年: 2021 ジャーナル: PLoS Pathog / 年: 2021タイトル: CryoEM structure of the Nipah virus nucleocapsid assembly. 著者: De-Sheng Ker / Huw T Jenkins / Sandra J Greive / Alfred A Antson /  要旨: Nipah and its close relative Hendra are highly pathogenic zoonotic viruses, storing their ssRNA genome in a helical nucleocapsid assembly formed by the N protein, a major viral immunogen. Here, we ...Nipah and its close relative Hendra are highly pathogenic zoonotic viruses, storing their ssRNA genome in a helical nucleocapsid assembly formed by the N protein, a major viral immunogen. Here, we report the first cryoEM structure for a Henipavirus RNA-bound nucleocapsid assembly, at 3.5 Å resolution. The helical assembly is stabilised by previously undefined N- and C-terminal segments, contributing to subunit-subunit interactions. RNA is wrapped around the nucleocapsid protein assembly with a periodicity of six nucleotides per protomer, in the "3-bases-in, 3-bases-out" conformation, with protein plasticity enabling non-sequence specific interactions. The structure reveals commonalities in RNA binding pockets and in the conformation of bound RNA, not only with members of the Paramyxoviridae family, but also with the evolutionarily distant Filoviridae Ebola virus. Significant structural differences with other Paramyxoviridae members are also observed, particularly in the position and length of the exposed α-helix, residues 123-139, which may serve as a valuable epitope for surveillance and diagnostics. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12583.map.gz emd_12583.map.gz | 49 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12583-v30.xml emd-12583-v30.xml emd-12583.xml emd-12583.xml | 15.7 KB 15.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_12583_fsc.xml emd_12583_fsc.xml | 13.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_12583.png emd_12583.png | 93.8 KB | ||
| マスクデータ |  emd_12583_msk_1.map emd_12583_msk_1.map | 52.7 MB |  マスクマップ マスクマップ | |
| その他 |  emd_12583_half_map_1.map.gz emd_12583_half_map_1.map.gz emd_12583_half_map_2.map.gz emd_12583_half_map_2.map.gz | 48.9 MB 48.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12583 http://ftp.pdbj.org/pub/emdb/structures/EMD-12583 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12583 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12583 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_12583_validation.pdf.gz emd_12583_validation.pdf.gz | 680.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_12583_full_validation.pdf.gz emd_12583_full_validation.pdf.gz | 679.4 KB | 表示 | |
| XML形式データ |  emd_12583_validation.xml.gz emd_12583_validation.xml.gz | 17.5 KB | 表示 | |
| CIF形式データ |  emd_12583_validation.cif.gz emd_12583_validation.cif.gz | 22.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12583 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12583 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12583 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12583 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12583.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12583.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.048 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
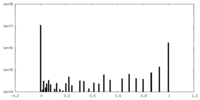
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_12583_msk_1.map emd_12583_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
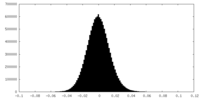
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_12583_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
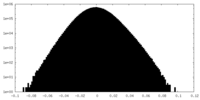
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_12583_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
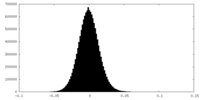
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Nipah virus nucleocapsid Protein-RNA complex
| 全体 | 名称: Nipah virus nucleocapsid Protein-RNA complex |
|---|---|
| 要素 |
|
-超分子 #1: Nipah virus nucleocapsid Protein-RNA complex
| 超分子 | 名称: Nipah virus nucleocapsid Protein-RNA complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Nipah henipavirus (ウイルス) Nipah henipavirus (ウイルス) |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 1 MDa |
-分子 #1: Nucleocapsid protein
| 分子 | 名称: Nucleocapsid protein / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Nipah henipavirus (ウイルス) Nipah henipavirus (ウイルス) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSSHHHHHH SSGLEVLFQG PAMSDIFEEA ASFRSYQSKL GRDGRASAAT ATLTTKIRI FVPATNSPEL RWELTLFALD VIRSPSAAES MKVGAAFTLI S MYSERPGA LIRSLLNDPD IEAVIIDVGS MVNGIPVMER RGDKAQEEME GL MRILKTA RDSSKGKTPF ...文字列: MGSSHHHHHH SSGLEVLFQG PAMSDIFEEA ASFRSYQSKL GRDGRASAAT ATLTTKIRI FVPATNSPEL RWELTLFALD VIRSPSAAES MKVGAAFTLI S MYSERPGA LIRSLLNDPD IEAVIIDVGS MVNGIPVMER RGDKAQEEME GL MRILKTA RDSSKGKTPF VDSRAYGLRI TDMSTLVSAV ITIEAQIWIL IAK AVTAPD TAEESETRRW AKYVQQKRVN PFFALTQQWL TEMRNLLSQS LSVR KFMVE ILIEVKKGGS AKGRAVEIIS DIGNYVEETG MAGFFATIRF GLETR YPAL ALNEFQSDLN TIKSLMLLYR EIGPRAPYMV LLEESIQTKF APGGYP LLW SFAMGVATTI DRSMGALNIN RGYLEPMYFR LGQKSARHHA GGIDQNM AN RLGLSSDQVA ELAAAVQETS AGRQESNVQA REAKFAAGGV LIGGSDQD I DEGEEPIEQS GRQSVTFKRE MSISSLANSV PSSSVSTSGG TRLTNSLLN LRSRLAAKAA KEAASSNATD DPAISNRTQG ESEKKNNQDL KPAQNDLDFV RADV |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.4 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 平均電子線量: 41.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.1 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)