+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6qti | ||||||
|---|---|---|---|---|---|---|---|
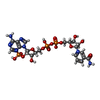
| タイトル | Structure of ovine transhydrogenase in the presence of NADP+ in a "double face-down" conformation | ||||||
 要素 要素 | Nicotinamide nucleotide transhydrogenase | ||||||
 キーワード キーワード | MEMBRANE PROTEIN / mitochondrial / proton-translocating / nicotinamide nucleotide transhydrogenase | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報: / proton-translocating NAD(P)+ transhydrogenase / NADPH regeneration / proton transmembrane transport / NADP binding / mitochondrial inner membrane / identical protein binding 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | ||||||
 データ登録者 データ登録者 | Kampjut, D. / Sazanov, L.A. | ||||||
| 資金援助 |  オーストリア, 1件 オーストリア, 1件
| ||||||
 引用 引用 |  ジャーナル: Nature / 年: 2019 ジャーナル: Nature / 年: 2019タイトル: Structure and mechanism of mitochondrial proton-translocating transhydrogenase. 著者: Domen Kampjut / Leonid A Sazanov /  要旨: Proton-translocating transhydrogenase (also known as nicotinamide nucleotide transhydrogenase (NNT)) is found in the plasma membranes of bacteria and the inner mitochondrial membranes of eukaryotes. ...Proton-translocating transhydrogenase (also known as nicotinamide nucleotide transhydrogenase (NNT)) is found in the plasma membranes of bacteria and the inner mitochondrial membranes of eukaryotes. NNT catalyses the transfer of a hydride between NADH and NADP, coupled to the translocation of one proton across the membrane. Its main physiological function is the generation of NADPH, which is a substrate in anabolic reactions and a regulator of oxidative status; however, NNT may also fine-tune the Krebs cycle. NNT deficiency causes familial glucocorticoid deficiency in humans and metabolic abnormalities in mice, similar to those observed in type II diabetes. The catalytic mechanism of NNT has been proposed to involve a rotation of around 180° of the entire NADP(H)-binding domain that alternately participates in hydride transfer and proton-channel gating. However, owing to the lack of high-resolution structures of intact NNT, the details of this process remain unclear. Here we present the cryo-electron microscopy structure of intact mammalian NNT in different conformational states. We show how the NADP(H)-binding domain opens the proton channel to the opposite sides of the membrane, and we provide structures of these two states. We also describe the catalytically important interfaces and linkers between the membrane and the soluble domains and their roles in nucleotide exchange. These structures enable us to propose a revised mechanism for a coupling process in NNT that is consistent with a large body of previous biochemical work. Our results are relevant to the development of currently unavailable NNT inhibitors, which may have therapeutic potential in ischaemia reperfusion injury, metabolic syndrome and some cancers. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6qti.cif.gz 6qti.cif.gz | 412.8 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6qti.ent.gz pdb6qti.ent.gz | 328.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6qti.json.gz 6qti.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  6qti_validation.pdf.gz 6qti_validation.pdf.gz | 1.7 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  6qti_full_validation.pdf.gz 6qti_full_validation.pdf.gz | 1.7 MB | 表示 | |
| XML形式データ |  6qti_validation.xml.gz 6qti_validation.xml.gz | 63.5 KB | 表示 | |
| CIF形式データ |  6qti_validation.cif.gz 6qti_validation.cif.gz | 94.6 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/qt/6qti https://data.pdbj.org/pub/pdb/validation_reports/qt/6qti ftp://data.pdbj.org/pub/pdb/validation_reports/qt/6qti ftp://data.pdbj.org/pub/pdb/validation_reports/qt/6qti | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
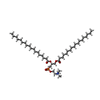
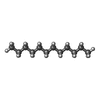
| #1: タンパク質 | 分子量: 114010.305 Da / 分子数: 2 / 由来タイプ: 天然 / 由来: (天然)  #2: 化合物 | #3: 化合物 | #4: 化合物 | ChemComp-PC1 / #5: 化合物 | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Nicotinamide nucleotide transhydrogenase in the presence of NADP+ タイプ: COMPLEX / Entity ID: #1 / 由来: NATURAL | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 値: 0.22 MDa / 実験値: NO | ||||||||||||||||||||
| 由来(天然) | 生物種:  | ||||||||||||||||||||
| 緩衝液 | pH: 7.4 | ||||||||||||||||||||
| 緩衝液成分 |
| ||||||||||||||||||||
| 試料 | 濃度: 5 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES 詳細: Sample was purified in LMNG (final conc. 0.06%) and contained 0.05% CHAPS as a secondary detergent as well as 5 mM NADP+. | ||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R0.6/1 | ||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K / 詳細: 4-6 s blotting time |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 10 sec. / 電子線照射量: 72 e/Å2 / 検出モード: SUPER-RESOLUTION フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 撮影したグリッド数: 1 / 実像数: 2160 |
| 画像スキャン | 動画フレーム数/画像: 40 |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.12_2829: / 分類: 精密化 | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 1076677 | ||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 98294 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||
| 原子モデル構築 | B value: 75.7 / プロトコル: AB INITIO MODEL / 空間: REAL / Target criteria: Correlation coefficient, EMRinger score | ||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 1D4O Accession code: 1D4O / Source name: PDB / タイプ: experimental model |
 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj