+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-7085 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | cryo-EM structure of TRPM4 in ATP bound state with long coiled coil at 3.3 angstrom resolution | ||||||||||||
 マップデータ マップデータ | Structure of TRPM4 in ATP bound state at 3.3A | ||||||||||||
 試料 試料 |
| ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報positive regulation of atrial cardiac muscle cell action potential / positive regulation of regulation of vascular associated smooth muscle cell membrane depolarization / sodium channel complex / regulation of T cell cytokine production / membrane depolarization during AV node cell action potential / membrane depolarization during bundle of His cell action potential / membrane depolarization during Purkinje myocyte cell action potential / negative regulation of bone mineralization / ligand-gated calcium channel activity / TRP channels ...positive regulation of atrial cardiac muscle cell action potential / positive regulation of regulation of vascular associated smooth muscle cell membrane depolarization / sodium channel complex / regulation of T cell cytokine production / membrane depolarization during AV node cell action potential / membrane depolarization during bundle of His cell action potential / membrane depolarization during Purkinje myocyte cell action potential / negative regulation of bone mineralization / ligand-gated calcium channel activity / TRP channels / voltage-gated monoatomic ion channel activity / regulation of ventricular cardiac muscle cell action potential / sodium ion import across plasma membrane / calcium-activated cation channel activity / inorganic cation transmembrane transport / dendritic cell chemotaxis / cellular response to ATP / positive regulation of heart rate / regulation of heart rate by cardiac conduction / positive regulation of insulin secretion involved in cellular response to glucose stimulus / protein sumoylation / positive regulation of fat cell differentiation / negative regulation of osteoblast differentiation / long-term memory / positive regulation of vasoconstriction / positive regulation of adipose tissue development / regulation of membrane potential / calcium ion transmembrane transport / calcium channel activity / calcium ion transport / positive regulation of canonical Wnt signaling pathway / positive regulation of cytosolic calcium ion concentration / protein homotetramerization / adaptive immune response / calmodulin binding / neuronal cell body / calcium ion binding / positive regulation of cell population proliferation / Golgi apparatus / endoplasmic reticulum / nucleoplasm / ATP binding / membrane / plasma membrane / cytosol 類似検索 - 分子機能 | ||||||||||||
| 生物種 |  | ||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.25 Å | ||||||||||||
 データ登録者 データ登録者 | Guo J / She J / Chen Q / Bai X / Jiang Y | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2017 ジャーナル: Nature / 年: 2017タイトル: Structures of the calcium-activated, non-selective cation channel TRPM4. 著者: Jiangtao Guo / Ji She / Weizhong Zeng / Qingfeng Chen / Xiao-Chen Bai / Youxing Jiang /  要旨: TRPM4 is a calcium-activated, phosphatidylinositol-4,5-bisphosphate (PtdIns(4,5)P) -modulated, non-selective cation channel that belongs to the family of melastatin-related transient receptor ...TRPM4 is a calcium-activated, phosphatidylinositol-4,5-bisphosphate (PtdIns(4,5)P) -modulated, non-selective cation channel that belongs to the family of melastatin-related transient receptor potential (TRPM) channels. Here we present the electron cryo-microscopy structures of the mouse TRPM4 channel with and without ATP. TRPM4 consists of multiple transmembrane and cytosolic domains, which assemble into a three-tiered architecture. The N-terminal nucleotide-binding domain and the C-terminal coiled-coil participate in the tetrameric assembly of the channel; ATP binds at the nucleotide-binding domain and inhibits channel activity. TRPM4 has an exceptionally wide filter but is only permeable to monovalent cations; filter residue Gln973 is essential in defining monovalent selectivity. The S1-S4 domain and the post-S6 TRP domain form the central gating apparatus that probably houses the Ca- and PtdIns(4,5)P-binding sites. These structures provide an essential starting point for elucidating the complex gating mechanisms of TRPM4 and reveal the molecular architecture of the TRPM family. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_7085.map.gz emd_7085.map.gz | 60.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-7085-v30.xml emd-7085-v30.xml emd-7085.xml emd-7085.xml | 16.4 KB 16.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_7085.png emd_7085.png | 204.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-7085 http://ftp.pdbj.org/pub/emdb/structures/EMD-7085 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7085 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7085 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_7085_validation.pdf.gz emd_7085_validation.pdf.gz | 541.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_7085_full_validation.pdf.gz emd_7085_full_validation.pdf.gz | 541.2 KB | 表示 | |
| XML形式データ |  emd_7085_validation.xml.gz emd_7085_validation.xml.gz | 5.9 KB | 表示 | |
| CIF形式データ |  emd_7085_validation.cif.gz emd_7085_validation.cif.gz | 6.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7085 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7085 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7085 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7085 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_7085.map.gz / 形式: CCP4 / 大きさ: 65.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_7085.map.gz / 形式: CCP4 / 大きさ: 65.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Structure of TRPM4 in ATP bound state at 3.3A | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
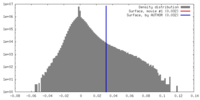
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : homotetramer of mouse TRPM4
| 全体 | 名称: homotetramer of mouse TRPM4 |
|---|---|
| 要素 |
|
-超分子 #1: homotetramer of mouse TRPM4
| 超分子 | 名称: homotetramer of mouse TRPM4 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Transient receptor potential cation channel subfamily M member 4
| 分子 | 名称: Transient receptor potential cation channel subfamily M member 4 タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 140.922875 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MVGPEKEQSW IPKIFRKKVC TTFIVDLSDD AGGTLCQCGQ PRDAHPSVAV EDAFGAAVVT EWNSDEHTTE KPTDAYGDLD FTYSGRKHS NFLRLSDRTD PATVYSLVTR SWGFRAPNLV VSVLGGSGGP VLQTWLQDLL RRGLVRAAQS TGAWIVTGGL H TGIGRHVG ...文字列: MVGPEKEQSW IPKIFRKKVC TTFIVDLSDD AGGTLCQCGQ PRDAHPSVAV EDAFGAAVVT EWNSDEHTTE KPTDAYGDLD FTYSGRKHS NFLRLSDRTD PATVYSLVTR SWGFRAPNLV VSVLGGSGGP VLQTWLQDLL RRGLVRAAQS TGAWIVTGGL H TGIGRHVG VAVRDHQTAS TGSSKVVAMG VAPWGVVRNR DMLINPKGSF PARYRWRGDP EDGVEFPLDY NYSAFFLVDD GT YGRLGGE NRFRLRFESY VAQQKTGVGG TGIDIPVLLL LIDGDEKMLK RIEDATQAQL PCLLVAGSGG AADCLVETLE DTL APGSGG LRRGEARDRI RRYFPKGDPE VLQAQVERIM TRKELLTVYS SEDGSEEFET IVLRALVKAC GSSEASAYLD ELRL AVAWN RVDIAQSELF RGDIQWRSFH LEASLMDALL NDRPEFVRLL ISHGLSLGHF LTPVRLAQLY SAVSPNSLIR NLLDQ ASHA SSSKSPPVNG TVELRPPNVG QVLRTLLGET CAPRYPARNT RDSYLGQDHR ENDSLLMDWA NKQPSTDASF EQAPWS DLL IWALLLNRAQ MAIYFWEKGS NSVASALGAC LLLRVMARLE SEAEEAARRK DLAATFESMS VDLFGECYHN SEERAAR LL LRRCPLWGEA TCLQLAMQAD ARAFFAQDGV QSLLTQKWWG EMDSTTPIWA LLLAFFCPPL IYTNLIVFRK SEEEPTQK D LDFDMDSSIN GAGPPGTVEP SAKVALERRQ RRRPGRALCC GKFSKRWSDF WGAPVTAFLG NVVSYLLFLL LFAHVLLVD FQPTKPSVSE LLLYFWAFTL LCEELRQGLG GGWGSLASGG RGPDRAPLRH RLHLYLSDTW NQCDLLALTC FLLGVGCRLT PGLFDLGRT VLCLDFMIFT LRLLHIFTVN KQLGPKIVIV SKMMKDVFFF LFFLCVWLVA YGVATEGILR PQDRSLPSIL R RVFYRPYL QIFGQIPQEE MDVALMIPGN CSMERGSWAH PEGPVAGSCV SQYANWLVVL LLIVFLLVAN ILLLNLLIAM FS YTFSKVH GNSDLYWKAQ RYSLIREFHS RPALAPPLII ISHVRLLIKW LRRCRRCRRA NLPASPVFEH FRVCLSKEAE RKL LTWESV HKENFLLAQA RDKRDSDSER LKRTSQKVDT ALKQLGQIRE YDRRLRGLER EVQHCSRVLT WMAEALSHSA LLPP GAPPP PSPTGSKDRN SKAYVDELTS RGRLEVLFQG PDYKDDDDKH HHHHHHHHH |
-分子 #2: ADENOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 4 / 式: ATP |
|---|---|
| 分子量 | 理論値: 507.181 Da |
| Chemical component information |  ChemComp-ATP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
| 詳細 | protein samples are reconstituted into nanodiscs |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS エネルギーフィルター - エネルギー下限: -10 eV エネルギーフィルター - エネルギー上限: 10 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 3000 / 平均露光時間: 15.0 sec. / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 46730 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)