+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4194 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
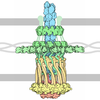
| タイトル | Thermus thermophilus PilF ATPase (AMPPNP-bound form) | |||||||||
 マップデータ マップデータ | Thermus thermophilus PilF ATPase (AMPPNP-bound form) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | type IV pilus / type II secretion / macromolecular machine / MOTOR PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Thermus thermophilus HB8 (バクテリア) / Thermus thermophilus HB8 (バクテリア) /   Thermus thermophilus (strain HB8 / ATCC 27634 / DSM 579) (バクテリア) Thermus thermophilus (strain HB8 / ATCC 27634 / DSM 579) (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 8.0 Å | |||||||||
 データ登録者 データ登録者 | Derrick JP / Collins RF | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Sci Rep / 年: 2018 ジャーナル: Sci Rep / 年: 2018タイトル: Structural cycle of the Thermus thermophilus PilF ATPase: the powering of type IVa pilus assembly. 著者: Richard Collins / Vijaykumar Karuppiah / C Alistair Siebert / Rana Dajani / Angela Thistlethwaite / Jeremy P Derrick /  要旨: Type IV pili are responsible for a diverse range of functions, including twitching motility and cell adhesion. Assembly of the pilus fiber is driven by a cytoplasmic ATPase: it interacts with an ...Type IV pili are responsible for a diverse range of functions, including twitching motility and cell adhesion. Assembly of the pilus fiber is driven by a cytoplasmic ATPase: it interacts with an inner membrane complex of biogenesis proteins which, in turn, bind to nascent pilin subunits and mediate fiber assembly. Here we report the structural characterization of the PilF TFP assembly ATPase from Thermus thermophilus. The crystal structure of a recombinant C-terminal fragment of PilF revealed bound, unhydrolysed ATP, although the full length complex was enzymatically active. 3D reconstructions were carried out by single particle cryoelectron microscopy for full length apoprotein PilF and in complex with AMPPNP. The structure forms an hourglass-like shape, with the ATPase domains in one half and the N1 domains in the second half which, we propose, interact with the other pilus biogenesis components. Molecular models for both forms were generated: binding of AMPPNP causes an upward shift of the N1 domains towards the ATPase domains of ~8 Å. We advocate a model in which ATP hydrolysis is linked to displacement of the N1 domains which is associated with lifting pilin subunits out of the inner membrane, and provide the activation energy needed to form the pilus fiber. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4194.map.gz emd_4194.map.gz | 5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4194-v30.xml emd-4194-v30.xml emd-4194.xml emd-4194.xml | 11.4 KB 11.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_4194.png emd_4194.png | 90.1 KB | ||
| Filedesc metadata |  emd-4194.cif.gz emd-4194.cif.gz | 5.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4194 http://ftp.pdbj.org/pub/emdb/structures/EMD-4194 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4194 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4194 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4194.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4194.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Thermus thermophilus PilF ATPase (AMPPNP-bound form) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.78 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Thermus thermophilus PilF ATPase (AMPPNP-bound form)
| 全体 | 名称: Thermus thermophilus PilF ATPase (AMPPNP-bound form) |
|---|---|
| 要素 |
|
-超分子 #1: Thermus thermophilus PilF ATPase (AMPPNP-bound form)
| 超分子 | 名称: Thermus thermophilus PilF ATPase (AMPPNP-bound form) タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:   Thermus thermophilus HB8 (バクテリア) Thermus thermophilus HB8 (バクテリア) |
-分子 #1: Type IV pilus assembly protein PilF
| 分子 | 名称: Type IV pilus assembly protein PilF / タイプ: protein_or_peptide / ID: 1 / コピー数: 18 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Thermus thermophilus (strain HB8 / ATCC 27634 / DSM 579) (バクテリア) Thermus thermophilus (strain HB8 / ATCC 27634 / DSM 579) (バクテリア)株: HB8 / ATCC 27634 / DSM 579 |
| 分子量 | 理論値: 101.021289 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSVLTIGDKR LGAALLDAGL LTDEELQRAL ERHREVGGSL AEVLVDMGLL SERRIAQTIE DRFGIPLVEL HRVEIPPKVK ALLPAEKAK ELKAIPFALD EEAGVVRVAF LNPLDTLSLE EVEDLTGLVV EPYQTTKSAF LYALAKHYPE LGLPVPPPPS G EGQKDLKL ...文字列: MSVLTIGDKR LGAALLDAGL LTDEELQRAL ERHREVGGSL AEVLVDMGLL SERRIAQTIE DRFGIPLVEL HRVEIPPKVK ALLPAEKAK ELKAIPFALD EEAGVVRVAF LNPLDTLSLE EVEDLTGLVV EPYQTTKSAF LYALAKHYPE LGLPVPPPPS G EGQKDLKL GELLLQKGWI SREALEEALV EQEKTGDLLG RILVRKGLPE EALYRALAEQ KGLEFLESTE GIVPDPSAAL LL LRSDALR YGAVPIGFQN GEVEVVLSDP RHKEAVAQLL NRPARFYLAL PQAWEELFRR AYPQKNRLGE VLVQEGKLSR EAL KEALEV QKGLPRAKPL GEILVELGLA RPEDVEEALQ KQRRGGGRLE DTLVQSGKLR PEALAQAVAT QLGYPYVDPE EDPP DPGAP LLLPEDLCRR YGVFPHRLEG NRLVLLMKDP RNILALDDVR LALKRKGLNY EVAPAVATEA AITKLIERFY GKAEL SEIA KEFAKKQAEE EVPSPLELDE SAAQKFVKQV IREAFLQDAS DIHIEPRQND VQVRLRIDGA LRPYSTLPKG ALNAVI SVV KIMGGLNIAE KRLPQDGRVR YREGAIDVDL RLSTLPTVYG EKAVMRLLKK ASDIPEIEDL GFAPGVFERF KEVISKP YG IFLITGPTGS GKSFTTFSIL KRIATPDKNT QTIEDPVEYE IPGINQTQVN PQAGLTFARA LRAFLRQDPD IIMVGEIR D SETAKIATEA ALTGHLVIAT LHTNDAAQAI TRLDEMGVEP FNISAALIGV LSQRLVRRVC EHCKVEVKPD PETLRRLGL SEAEIQGARL YKGMGCERCG GTGYKGRYAI HELLVVDDEI RHAIVAGKSA TEIKEIARRK GMKTLREDGL YKALQGITTL EEVLARTIE AAAELALVPR GSSAHHHHHH HHHH UniProtKB: Type IV pilus assembly ATPase PilB |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.2 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 25 mM HEPES pH 7.5, 150 mM NaCl, 5 mM MgCl2 and 5 % glycerol (v/v) |
| 凍結 | 凍結剤: ETHANE |
| 詳細 | Monodisperse |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: k2 エネルギーフィルター - エネルギー下限: 20 eV エネルギーフィルター - エネルギー上限: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 BASE (4k x 4k) 平均電子線量: 45.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 4.5 µm / 最小 デフォーカス(補正後): 1.0 µm / 照射モード: OTHER / 撮影モード: OTHER / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.5 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 8.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: RELION / 使用した粒子像数: 450000 |
| 初期 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: EMAN |
| 最終 角度割当 | タイプ: PROJECTION MATCHING |
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





















