+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the p300 catalytic core bound to the H4K12acK16ac nucleosome, class 1 (3.2 angstrom resolution) | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Acetyl taransferase / Complex / Nucleosome / TRANSFERASE / TRANSFERASE-DNA complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報behavioral defense response / peptidyl-lysine propionylation / histone lactyltransferase (CoA-dependent) activity / peptidyl-lysine crotonylation / peptidyl-lysine butyrylation / histone butyryltransferase activity / histone H3K122 acetyltransferase activity / swimming / peptide butyryltransferase activity / histone H2B acetyltransferase activity ...behavioral defense response / peptidyl-lysine propionylation / histone lactyltransferase (CoA-dependent) activity / peptidyl-lysine crotonylation / peptidyl-lysine butyrylation / histone butyryltransferase activity / histone H3K122 acetyltransferase activity / swimming / peptide butyryltransferase activity / histone H2B acetyltransferase activity / thigmotaxis / peptide 2-hydroxyisobutyryltransferase activity / histone crotonyltransferase activity / protein propionyltransferase activity / NOTCH2 intracellular domain regulates transcription / peptidyl-lysine acetylation / lysine N-acetyltransferase activity, acting on acetyl phosphate as donor / histone H4 acetyltransferase activity / internal peptidyl-lysine acetylation / cellular response to L-leucine / histone H3 acetyltransferase activity / NFE2L2 regulating ER-stress associated genes / peptide N-acetyltransferase activity / acetylation-dependent protein binding / Activation of the TFAP2 (AP-2) family of transcription factors / NFE2L2 regulating inflammation associated genes / NGF-stimulated transcription / STAT3 nuclear events downstream of ALK signaling / histone H3K18 acetyltransferase activity / N-terminal peptidyl-lysine acetylation / histone H3K27 acetyltransferase activity / LRR FLII-interacting protein 1 (LRRFIP1) activates type I IFN production / NFE2L2 regulates pentose phosphate pathway genes / TGFBR3 expression / Polo-like kinase mediated events / NFE2L2 regulating MDR associated enzymes / regulation of androgen receptor signaling pathway / regulation of mitochondrion organization / positive regulation by host of viral transcription / face morphogenesis / Regulation of FOXO transcriptional activity by acetylation / Regulation of gene expression in late stage (branching morphogenesis) pancreatic bud precursor cells / regulation of glycolytic process / RUNX3 regulates NOTCH signaling / Regulation of gene expression by Hypoxia-inducible Factor / Nuclear events mediated by NFE2L2 / NOTCH4 Intracellular Domain Regulates Transcription / FOXO-mediated transcription of cell death genes / Regulation of NFE2L2 gene expression / NOTCH3 Intracellular Domain Regulates Transcription / platelet formation / TRAF6 mediated IRF7 activation / peptide-lysine-N-acetyltransferase activity / megakaryocyte development / NFE2L2 regulating tumorigenic genes / NFE2L2 regulating anti-oxidant/detoxification enzymes / macrophage derived foam cell differentiation / regulation of tubulin deacetylation / nuclear androgen receptor binding / STAT family protein binding / protein acetylation / acyltransferase activity / internal protein amino acid acetylation / fat cell differentiation / positive regulation of transforming growth factor beta receptor signaling pathway / Formation of paraxial mesoderm / stimulatory C-type lectin receptor signaling pathway / RUNX1 interacts with co-factors whose precise effect on RUNX1 targets is not known / PI5P Regulates TP53 Acetylation / acetyltransferase activity / Zygotic genome activation (ZGA) / RUNX3 regulates p14-ARF / NF-kappaB binding / histone acetyltransferase complex / negative regulation of tumor necrosis factor-mediated signaling pathway / Attenuation phase / intrinsic apoptotic signaling pathway in response to DNA damage by p53 class mediator / somitogenesis / negative regulation of protein-containing complex assembly / negative regulation of gluconeogenesis / cellular response to nutrient levels / protein localization to CENP-A containing chromatin / canonical NF-kappaB signal transduction / Chromatin modifying enzymes / Replacement of protamines by nucleosomes in the male pronucleus / CENP-A containing nucleosome / positive regulation of T-helper 17 cell lineage commitment / pre-mRNA intronic binding / histone acetyltransferase activity / SARS-CoV-1 targets host intracellular signalling and regulatory pathways / Packaging Of Telomere Ends / regulation of cellular response to heat / histone acetyltransferase / Recognition and association of DNA glycosylase with site containing an affected purine / Cleavage of the damaged purine / skeletal muscle tissue development / NR1H3 & NR1H2 regulate gene expression linked to cholesterol transport and efflux / Deposition of new CENPA-containing nucleosomes at the centromere / Regulation of TP53 Activity through Acetylation / nucleosomal DNA binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
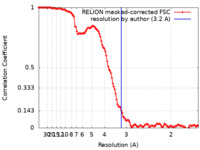
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.2 Å | |||||||||
 データ登録者 データ登録者 | Kikuchi M / Morita S / Wakamori M / Shin S / Uchikubo-Kamo T / Shirouzu M / Umehara T | |||||||||
| 資金援助 |  日本, 1件 日本, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Epigenetic mechanisms to propagate histone acetylation by p300/CBP. 著者: Masaki Kikuchi / Satoshi Morita / Masatoshi Wakamori / Shin Sato / Tomomi Uchikubo-Kamo / Takehiro Suzuki / Naoshi Dohmae / Mikako Shirouzu / Takashi Umehara /  要旨: Histone acetylation is important for the activation of gene transcription but little is known about its direct read/write mechanisms. Here, we report cryogenic electron microscopy structures in which ...Histone acetylation is important for the activation of gene transcription but little is known about its direct read/write mechanisms. Here, we report cryogenic electron microscopy structures in which a p300/CREB-binding protein (CBP) multidomain monomer recognizes histone H4 N-terminal tail (NT) acetylation (ac) in a nucleosome and acetylates non-H4 histone NTs within the same nucleosome. p300/CBP not only recognized H4NTac via the bromodomain pocket responsible for reading, but also interacted with the DNA minor grooves via the outside of that pocket. This directed the catalytic center of p300/CBP to one of the non-H4 histone NTs. The primary target that p300 writes by reading H4NTac was H2BNT, and H2BNTac promoted H2A-H2B dissociation from the nucleosome. We propose a model in which p300/CBP replicates histone N-terminal tail acetylation within the H3-H4 tetramer to inherit epigenetic storage, and transcribes it from the H3-H4 tetramer to the H2B-H2A dimers to activate context-dependent gene transcription through local nucleosome destabilization. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_34588.map.gz emd_34588.map.gz | 140.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-34588-v30.xml emd-34588-v30.xml emd-34588.xml emd-34588.xml | 20.3 KB 20.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_34588_fsc.xml emd_34588_fsc.xml | 12 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_34588.png emd_34588.png | 82.8 KB | ||
| マスクデータ |  emd_34588_msk_1.map emd_34588_msk_1.map | 149.9 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-34588.cif.gz emd-34588.cif.gz | 6.8 KB | ||
| その他 |  emd_34588_half_map_1.map.gz emd_34588_half_map_1.map.gz emd_34588_half_map_2.map.gz emd_34588_half_map_2.map.gz | 118.4 MB 118.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-34588 http://ftp.pdbj.org/pub/emdb/structures/EMD-34588 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34588 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34588 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_34588_validation.pdf.gz emd_34588_validation.pdf.gz | 932.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_34588_full_validation.pdf.gz emd_34588_full_validation.pdf.gz | 932.5 KB | 表示 | |
| XML形式データ |  emd_34588_validation.xml.gz emd_34588_validation.xml.gz | 19.3 KB | 表示 | |
| CIF形式データ |  emd_34588_validation.cif.gz emd_34588_validation.cif.gz | 25.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34588 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34588 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34588 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34588 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8hagMC  8hahC  8haiC  8hajC  8hakC  8halC  8hamC  8hanC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_34588.map.gz / 形式: CCP4 / 大きさ: 149.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_34588.map.gz / 形式: CCP4 / 大きさ: 149.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.829 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_34588_msk_1.map emd_34588_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_34588_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_34588_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : the p300 catalytic core bound to the H4K12acK16ac nucleosome
| 全体 | 名称: the p300 catalytic core bound to the H4K12acK16ac nucleosome |
|---|---|
| 要素 |
|
-超分子 #1: the p300 catalytic core bound to the H4K12acK16ac nucleosome
| 超分子 | 名称: the p300 catalytic core bound to the H4K12acK16ac nucleosome タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: p300 was expressed in insect cells. |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Histone H3.1
| 分子 | 名称: Histone H3.1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 15.305969 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: ARTKQTARKS TGGKAPRKQL ATKAARKSAP ATGGVKKPHR YRPGTVALRE IRRYQKSTEL LIRKLPFQRL VREIAQDFKT DLRFQSSAV MALQEACEAY LVGLFEDTNL CAIHAKRVTI MPKDIQLARR IRGERA UniProtKB: Histone H3.1 |
-分子 #2: Histone H4
| 分子 | 名称: Histone H4 / タイプ: protein_or_peptide / ID: 2 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 11.345289 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SGRGKGGKGL G(ALY)GGA(ALY)RHRK VLRDNIQGIT KPAIRRLARR GGVKRISGLI YEETRGVLKV FLENVIRDAV TY TEHAKRK TVTAMDVVYA LKRQGRTLYG FGG |
-分子 #3: Histone H2A type 1-B/E
| 分子 | 名称: Histone H2A type 1-B/E / タイプ: protein_or_peptide / ID: 3 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 14.034355 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SGRGKQGGKA RAKAKTRSSR AGLQFPVGRV HRLLRKGNYS ERVGAGAPVY LAAVLEYLTA EILELAGNAA RDNKKTRIIP RHLQLAIRN DEELNKLLGR VTIAQGGVLP NIQAVLLPKK TESHHKAKGK UniProtKB: Histone H2A type 1-B/E |
-分子 #4: Histone H2B type 1-J
| 分子 | 名称: Histone H2B type 1-J / タイプ: protein_or_peptide / ID: 4 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 13.935239 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MPEPAKSAPA PKKGSKKAVT KAQKKDGKKR KRSRKESYSI YVYKVLKQVH PDTGISSKAM GIMNSFVNDI FERIAGEASR LAHYNKRST ITSREIQTAV RLLLPGELAK HAVSEGTKAV TKYTSAK UniProtKB: Histone H2B type 1-J |
-分子 #5: Histone acetyltransferase p300
| 分子 | 名称: Histone acetyltransferase p300 / タイプ: protein_or_peptide / ID: 5 / コピー数: 1 / 光学異性体: LEVO / EC番号: histone acetyltransferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 92.314391 KDa |
| 組換発現 | 生物種:  Trichoplusia ni (イラクサキンウワバ) Trichoplusia ni (イラクサキンウワバ) |
| 配列 | 文字列: GSSGSSGIFK PEELRQALMP TLEALYRQDP ESLPFRQPVD PQLLGIPDYF DIVKSPMDLS TIKRKLDTGQ YQEPWQYVDD IWLMFNNAW LYNRKTSRVY KYCSKLSEVF EQEIDPVMQS LGYCCGRKLE FSPQTLCCYG KQLCTIPRDA TYYSYQNRYH F CEKCFNEI ...文字列: GSSGSSGIFK PEELRQALMP TLEALYRQDP ESLPFRQPVD PQLLGIPDYF DIVKSPMDLS TIKRKLDTGQ YQEPWQYVDD IWLMFNNAW LYNRKTSRVY KYCSKLSEVF EQEIDPVMQS LGYCCGRKLE FSPQTLCCYG KQLCTIPRDA TYYSYQNRYH F CEKCFNEI QGESVSLGDD PSQPQTTINK EQFSKRKNDT LDPELFVECT ECGRKMHQIC VLHHEIIWPA GFVCDGCLKK SA RTRKENK FSAKRLPSTR LGTFLENRVN DFLRRQNHPE SGEVTVRVVH ASDKTVEVKP GMKARFVDSG EMAESFPYRT KAL FAFEEI DGVDLCFFGM HVQEYGSDCP PPNQRRVYIS YLDSVHFFRP KCLRTAVYHE ILIGYLEYVK KLGYTTGHIW ACPP SEGDD YIFHCHPPDQ KIPKPKRLQE WYKKMLDKAV SERIVHDYKD IFKQATEDRL TSAKELPYFE GDFWPNVLEE SIKEL EQEE EERKREENTS NESTDVTKGD SKNAKKKNNK KTSKNKSSLS RGNKKKPGMP NVSNDLSQKL YATMEKHKEV FFVIRL IAG PAANSLPPIV DPDPLIPCDL MDGRDAFLTL ARDKHLEFSS LRRAQWSTMC MLVELHTQSQ DRFVYTCNEC KHHVETR WH CTVCEDYDLC ITCYNTKNHD HKMEKLGLGL DDESNNQQAA ATQSPGDSRR LSIQRCIQSL VHACQCRNAN CSLPSCQK M KRVVQHTKGC KRKTNGGCPI CKQLIALCCY HAKHCQENKC PVPFCLNIKQ KLRQQQLQHR LQQAQMLRRR MASMQ UniProtKB: Histone acetyltransferase p300 |
-分子 #6: DNA (180-mer)
| 分子 | 名称: DNA (180-mer) / タイプ: dna / ID: 6 / コピー数: 2 / 分類: DNA |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 55.560527 KDa |
| 配列 | 文字列: (DA)(DT)(DC)(DC)(DG)(DT)(DC)(DC)(DG)(DT) (DT)(DA)(DC)(DC)(DG)(DC)(DC)(DA)(DT)(DC) (DA)(DA)(DT)(DA)(DT)(DC)(DC)(DA)(DC) (DC)(DT)(DG)(DC)(DA)(DG)(DA)(DT)(DT)(DC) (DT) (DA)(DC)(DC)(DA)(DA) ...文字列: (DA)(DT)(DC)(DC)(DG)(DT)(DC)(DC)(DG)(DT) (DT)(DA)(DC)(DC)(DG)(DC)(DC)(DA)(DT)(DC) (DA)(DA)(DT)(DA)(DT)(DC)(DC)(DA)(DC) (DC)(DT)(DG)(DC)(DA)(DG)(DA)(DT)(DT)(DC) (DT) (DA)(DC)(DC)(DA)(DA)(DA)(DA)(DG) (DT)(DG)(DT)(DA)(DT)(DT)(DT)(DG)(DG)(DA) (DA)(DA) (DC)(DT)(DG)(DC)(DT)(DC)(DC) (DA)(DT)(DC)(DA)(DA)(DA)(DA)(DG)(DG)(DC) (DA)(DT)(DG) (DT)(DT)(DC)(DA)(DG)(DC) (DT)(DG)(DA)(DA)(DT)(DT)(DC)(DA)(DG)(DC) (DT)(DG)(DA)(DA) (DC)(DA)(DT)(DG)(DC) (DC)(DT)(DT)(DT)(DT)(DG)(DA)(DT)(DG)(DG) (DA)(DG)(DC)(DA)(DG) (DT)(DT)(DT)(DC) (DC)(DA)(DA)(DA)(DT)(DA)(DC)(DA)(DC)(DT) (DT)(DT)(DT)(DG)(DG)(DT) (DA)(DG)(DA) (DA)(DT)(DC)(DT)(DG)(DC)(DA)(DG)(DG)(DT) (DG)(DG)(DA)(DT)(DA)(DT)(DT) (DG)(DA) (DT)(DG)(DG)(DC)(DG)(DG)(DT)(DA)(DA)(DC) (DG)(DG)(DA)(DC)(DG)(DG)(DA)(DT) |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.2 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー









































 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)