+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-22807 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | The Cryo-EM Structure of Alcohol Dehyrogenase from Yeast in complex with NAD+ and Trifluoro Ethanol (TFE) | |||||||||
 マップデータ マップデータ | Cryo-EM Structure of Alcohol Dehyrogenase from Yeast in complex with NAD+ and Pyrazole | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Alcohol dehydrogenase / holo-enzyme complex / OXIDOREDUCTASE | |||||||||
| 機能・相同性 | :  機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.77 Å | |||||||||
 データ登録者 データ登録者 | Subramanian R / Chang L / Guntupalli SR | |||||||||
 引用 引用 |  ジャーナル: Biochemistry / 年: 2014 ジャーナル: Biochemistry / 年: 2014タイトル: Yeast alcohol dehydrogenase structure and catalysis. 著者: Savarimuthu Baskar Raj / S Ramaswamy / Bryce V Plapp /  要旨: Yeast (Saccharomyces cerevisiae) alcohol dehydrogenase I (ADH1) is the constitutive enzyme that reduces acetaldehyde to ethanol during the fermentation of glucose. ADH1 is a homotetramer of subunits ...Yeast (Saccharomyces cerevisiae) alcohol dehydrogenase I (ADH1) is the constitutive enzyme that reduces acetaldehyde to ethanol during the fermentation of glucose. ADH1 is a homotetramer of subunits with 347 amino acid residues. A structure for ADH1 was determined by X-ray crystallography at 2.4 Å resolution. The asymmetric unit contains four different subunits, arranged as similar dimers named AB and CD. The unit cell contains two different tetramers made up of "back-to-back" dimers, AB:AB and CD:CD. The A and C subunits in each dimer are structurally similar, with a closed conformation, bound coenzyme, and the oxygen of 2,2,2-trifluoroethanol ligated to the catalytic zinc in the classical tetrahedral coordination with Cys-43, Cys-153, and His-66. In contrast, the B and D subunits have an open conformation with no bound coenzyme, and the catalytic zinc has an alternative, inverted coordination with Cys-43, Cys-153, His-66, and the carboxylate of Glu-67. The asymmetry in the dimeric subunits of the tetramer provides two structures that appear to be relevant for the catalytic mechanism. The alternative coordination of the zinc may represent an intermediate in the mechanism of displacement of the zinc-bound water with alcohol or aldehyde substrates. Substitution of Glu-67 with Gln-67 decreases the catalytic efficiency by 100-fold. Previous studies of structural modeling, evolutionary relationships, substrate specificity, chemical modification, and site-directed mutagenesis are interpreted more fully with the three-dimensional structure. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_22807.map.gz emd_22807.map.gz | 20.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-22807-v30.xml emd-22807-v30.xml emd-22807.xml emd-22807.xml | 13.6 KB 13.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_22807.png emd_22807.png | 235 KB | ||
| Filedesc metadata |  emd-22807.cif.gz emd-22807.cif.gz | 5.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-22807 http://ftp.pdbj.org/pub/emdb/structures/EMD-22807 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22807 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22807 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_22807_validation.pdf.gz emd_22807_validation.pdf.gz | 539.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_22807_full_validation.pdf.gz emd_22807_full_validation.pdf.gz | 539 KB | 表示 | |
| XML形式データ |  emd_22807_validation.xml.gz emd_22807_validation.xml.gz | 5.9 KB | 表示 | |
| CIF形式データ |  emd_22807_validation.cif.gz emd_22807_validation.cif.gz | 6.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22807 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22807 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22807 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22807 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_22807.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_22807.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cryo-EM Structure of Alcohol Dehyrogenase from Yeast in complex with NAD+ and Pyrazole | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.05 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Alcohol Dehydrogenase NAD+ Pyrazole complex
| 全体 | 名称: Alcohol Dehydrogenase NAD+ Pyrazole complex |
|---|---|
| 要素 |
|
-超分子 #1: Alcohol Dehydrogenase NAD+ Pyrazole complex
| 超分子 | 名称: Alcohol Dehydrogenase NAD+ Pyrazole complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 370 KDa |
-分子 #1: ADH1 isoform 1
| 分子 | 名称: ADH1 isoform 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 36.759906 KDa |
| 配列 | 文字列: SIPETQKGVI FYESHGKLEY KDIPVPKPKA NELLINVKYS GVCHTDLHAW HGDWPLPVKL PLVGGHEGAG VVVGMGENVK GWKIGDYAG IKWLNGSCMA CEYCELGNES NCPHADLSGY THDGSFQQYA TADAVQAAHI PQGTDLAQVA PILCAGITVY K ALKSANLM ...文字列: SIPETQKGVI FYESHGKLEY KDIPVPKPKA NELLINVKYS GVCHTDLHAW HGDWPLPVKL PLVGGHEGAG VVVGMGENVK GWKIGDYAG IKWLNGSCMA CEYCELGNES NCPHADLSGY THDGSFQQYA TADAVQAAHI PQGTDLAQVA PILCAGITVY K ALKSANLM AGHWVAISGA AGGLGSLAVQ YAKAMGYRVL GIDGGEGKEE LFRSIGGEVF IDFTKEKDIV GAVLKATDGG AH GVINVSV SEAAIEASTR YVRANGTTVL VGMPAGAKCC SDVFNQVVKS ISIVGSYVGN RADTREALDF FARGLVKSPI KVV GLSTLP EIYEKMEKGQ IVGRYVVDTS K UniProtKB: UNIPROTKB: A0A6A5Q6H9 |
-分子 #2: ZINC ION
| 分子 | 名称: ZINC ION / タイプ: ligand / ID: 2 / コピー数: 8 / 式: ZN |
|---|---|
| 分子量 | 理論値: 65.409 Da |
-分子 #3: NICOTINAMIDE-ADENINE-DINUCLEOTIDE
| 分子 | 名称: NICOTINAMIDE-ADENINE-DINUCLEOTIDE / タイプ: ligand / ID: 3 / コピー数: 4 / 式: NAD |
|---|---|
| 分子量 | 理論値: 663.425 Da |
| Chemical component information |  ChemComp-NAD: |
-分子 #4: TRIFLUOROETHANOL
| 分子 | 名称: TRIFLUOROETHANOL / タイプ: ligand / ID: 4 / コピー数: 4 / 式: ETF |
|---|---|
| 分子量 | 理論値: 100.04 Da |
| Chemical component information | 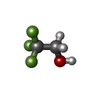 ChemComp-ETF: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL |
|---|---|
| 緩衝液 | pH: 8.2 / 構成要素 - 濃度: 50.0 mM / 構成要素 - 式: C4H11NO3 / 構成要素 - 名称: Tris 詳細: Tris HCl buffer 5mM with 200mM KCl adjusted to pH 8.2. |
| グリッド | モデル: Quantifoil / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 298 K / 装置: FEI VITROBOT MARK II |
| 詳細 | Purified by Size Exclusion chromatography |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 54.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: OTHER / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: INSILICO MODEL |
|---|---|
| 最終 再構成 | アルゴリズム: BACK PROJECTION / 解像度のタイプ: BY AUTHOR / 解像度: 2.77 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: cryoSPARC (ver. 2) / 使用した粒子像数: 1284904 |
| 初期 角度割当 | タイプ: RANDOM ASSIGNMENT |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A / Chain - Residue range: 1-347 / Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 39.3 / 当てはまり具合の基準: Correlation Coefficient |
| 得られたモデル |  PDB-7kcb: |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















