+ Open data
Open data
- Basic information
Basic information
| Entry | Database: EMDB / ID: EMD-22238 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Title | Apo full-length Hsc82 in complex with Aha1 | |||||||||
 Map data Map data | Apo full-length Hsc82 in complex with Aha1 | |||||||||
 Sample Sample |
| |||||||||
 Keywords Keywords | Co-chaperone / activator / CHAPERONE | |||||||||
| Function / homology |  Function and homology information Function and homology informationTetrahydrobiopterin (BH4) synthesis, recycling, salvage and regulation / eNOS activation / Extra-nuclear estrogen signaling / HSP90 chaperone cycle for steroid hormone receptors (SHR) in the presence of ligand / VEGFR2 mediated vascular permeability / HSF1-dependent transactivation / HSF1 activation / response to oxygen levels / box C/D snoRNP assembly / ATPase activator activity ...Tetrahydrobiopterin (BH4) synthesis, recycling, salvage and regulation / eNOS activation / Extra-nuclear estrogen signaling / HSP90 chaperone cycle for steroid hormone receptors (SHR) in the presence of ligand / VEGFR2 mediated vascular permeability / HSF1-dependent transactivation / HSF1 activation / response to oxygen levels / box C/D snoRNP assembly / ATPase activator activity / proteasome assembly / Neutrophil degranulation / telomere maintenance / ATP-dependent protein folding chaperone / protein import into nucleus / : / cellular response to heat / protein-folding chaperone binding / protein folding / protein stabilization / perinuclear region of cytoplasm / ATP hydrolysis activity / protein-containing complex / mitochondrion / ATP binding / nucleus / plasma membrane / cytoplasm / cytosol Similarity search - Function | |||||||||
| Biological species |  | |||||||||
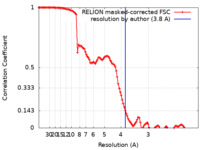
| Method | single particle reconstruction / cryo EM / Resolution: 3.8 Å | |||||||||
 Authors Authors | Liu YX / Sun M | |||||||||
| Funding support |  United States, 2 items United States, 2 items
| |||||||||
 Citation Citation |  Journal: To Be Published Journal: To Be PublishedTitle: Apo full-length Hsc82 in complex with Aha1 Authors: Liu YX / Sun M / Myasnikov AG / Elnatan D / Agard DA | |||||||||
| History |
|
- Structure visualization
Structure visualization
| Movie |
 Movie viewer Movie viewer |
|---|---|
| Structure viewer | EM map:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| Supplemental images |
- Downloads & links
Downloads & links
-EMDB archive
| Map data |  emd_22238.map.gz emd_22238.map.gz | 117.2 MB |  EMDB map data format EMDB map data format | |
|---|---|---|---|---|
| Header (meta data) |  emd-22238-v30.xml emd-22238-v30.xml emd-22238.xml emd-22238.xml | 10.8 KB 10.8 KB | Display Display |  EMDB header EMDB header |
| FSC (resolution estimation) |  emd_22238_fsc.xml emd_22238_fsc.xml | 11.4 KB | Display |  FSC data file FSC data file |
| Images |  emd_22238.png emd_22238.png | 68.6 KB | ||
| Filedesc metadata |  emd-22238.cif.gz emd-22238.cif.gz | 5.5 KB | ||
| Archive directory |  http://ftp.pdbj.org/pub/emdb/structures/EMD-22238 http://ftp.pdbj.org/pub/emdb/structures/EMD-22238 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22238 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22238 | HTTPS FTP |
-Related structure data
| Related structure data |  6xlbMC  6xlcC  6xldC  6xleC  6xlfC  6xlgC  6xlhC M: atomic model generated by this map C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
| EMDB pages |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| Related items in Molecule of the Month |
- Map
Map
| File |  Download / File: emd_22238.map.gz / Format: CCP4 / Size: 125 MB / Type: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) Download / File: emd_22238.map.gz / Format: CCP4 / Size: 125 MB / Type: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Annotation | Apo full-length Hsc82 in complex with Aha1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Projections & slices | Image control
Images are generated by Spider. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Voxel size | X=Y=Z: 1.032 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
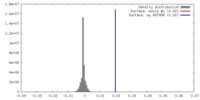
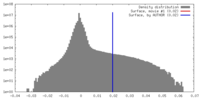
| Density |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symmetry | Space group: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Details | EMDB XML:
CCP4 map header:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-Supplemental data
- Sample components
Sample components
-Entire : Hsc82 in complex with Aha1 CTD
| Entire | Name: Hsc82 in complex with Aha1 CTD |
|---|---|
| Components |
|
-Supramolecule #1: Hsc82 in complex with Aha1 CTD
| Supramolecule | Name: Hsc82 in complex with Aha1 CTD / type: complex / ID: 1 / Parent: 0 / Macromolecule list: all |
|---|---|
| Source (natural) | Organism:  Strain: ATCC 204508 / S288c |
-Macromolecule #1: ATP-dependent molecular chaperone HSC82
| Macromolecule | Name: ATP-dependent molecular chaperone HSC82 / type: protein_or_peptide / ID: 1 / Number of copies: 2 / Enantiomer: LEVO |
|---|---|
| Source (natural) | Organism:  Strain: ATCC 204508 / S288c |
| Molecular weight | Theoretical: 81.003594 KDa |
| Recombinant expression | Organism:  |
| Sequence | String: MAGETFEFQA EITQLMSLII NTVYSNKEIF LRELISNASD ALDKIRYQAL SDPKQLETEP DLFIRITPKP EEKVLEIRDS GIGMTKAEL INNLGTIAKS GTKAFMEALS AGADVSMIGQ FGVGFYSLFL VADRVQVISK NNEDEQYIWE SNAGGSFTVT L DEVNERIG ...String: MAGETFEFQA EITQLMSLII NTVYSNKEIF LRELISNASD ALDKIRYQAL SDPKQLETEP DLFIRITPKP EEKVLEIRDS GIGMTKAEL INNLGTIAKS GTKAFMEALS AGADVSMIGQ FGVGFYSLFL VADRVQVISK NNEDEQYIWE SNAGGSFTVT L DEVNERIG RGTVLRLFLK DDQLEYLEEK RIKEVIKRHS EFVAYPIQLL VTKEVEKEVP IPEEEKKDEE KKDEDDKKPK LE EVDEEEE EKKPKTKKVK EEVQELEELN KTKPLWTRNP SDITQEEYNA FYKSISNDWE DPLYVKHFSV EGQLEFRAIL FIP KRAPFD LFESKKKKNN IKLYVRRVFI TDEAEDLIPE WLSFVKGVVD SEDLPLNLSR EMLQQNKIMK VIRKNIVKKL IEAF NEIAE DSEQFDKFYS AFAKNIKLGV HEDTQNRAAL AKLLRYNSTK SVDELTSLTD YVTRMPEHQK NIYYITGESL KAVEK SPFL DALKAKNFEV LFLTDPIDEY AFTQLKEFEG KTLVDITKDF ELEETDEEKA EREKEIKEYE PLTKALKDIL GDQVEK VVV SYKLLDAPAA IRTGQFGWSA NMERIMKAQA LRDSSMSSYM SSKKTFEISP KSPIIKELKK RVDEGGAQDK TVKDLTN LL FETALLTSGF SLEEPTSFAS RINRLISLGL NIDEDEETET APEASTEAPV EEVPADTEME EVD UniProtKB: ATP-dependent molecular chaperone HSC82 |
-Macromolecule #2: Hsp90 co-chaperone AHA1
| Macromolecule | Name: Hsp90 co-chaperone AHA1 / type: protein_or_peptide / ID: 2 / Number of copies: 2 / Enantiomer: LEVO |
|---|---|
| Source (natural) | Organism:  Strain: ATCC 204508 / S288c |
| Molecular weight | Theoretical: 39.486422 KDa |
| Recombinant expression | Organism:  |
| Sequence | String: MVVNNPNNWH WVDKNCIGWA KEYFKQKLVG VEAGSVKDKK YAKIKSVSSI EGDCEVNQRK GKVISLFDLK ITVLIEGHVD SKDGSALPF EGSINVPEVA FDSEASSYQF DISIFKETSE LSEAKPLIRS ELLPKLRQIF QQFGKDLLAT HGNDIQVPES Q VKSNYTRG ...String: MVVNNPNNWH WVDKNCIGWA KEYFKQKLVG VEAGSVKDKK YAKIKSVSSI EGDCEVNQRK GKVISLFDLK ITVLIEGHVD SKDGSALPF EGSINVPEVA FDSEASSYQF DISIFKETSE LSEAKPLIRS ELLPKLRQIF QQFGKDLLAT HGNDIQVPES Q VKSNYTRG NQKSSFTEIK DSASKPKKNA LPSSTSTSAP VSSTNKVPQN GSGNSTSIYL EPTFNVPSSE LYETFLDKQR IL AWTRSAQ FFNSGPKLET KEKFELFGGN VISELVSCEK DKKLVFHWKL KDWSAPFNST IEMTFHESQE FHETKLQVKW TGI PVGEED RVRANFEEYY VRSIKLTFGF GAVL UniProtKB: Hsp90 co-chaperone AHA1 |
-Experimental details
-Structure determination
| Method | cryo EM |
|---|---|
 Processing Processing | single particle reconstruction |
| Aggregation state | particle |
- Sample preparation
Sample preparation
| Buffer | pH: 7.5 |
|---|---|
| Vitrification | Cryogen name: ETHANE |
- Electron microscopy
Electron microscopy
| Microscope | FEI TITAN KRIOS |
|---|---|
| Image recording | Film or detector model: GATAN K2 SUMMIT (4k x 4k) / Detector mode: SUPER-RESOLUTION / Average electron dose: 72.0 e/Å2 |
| Electron beam | Acceleration voltage: 300 kV / Electron source:  FIELD EMISSION GUN FIELD EMISSION GUN |
| Electron optics | Illumination mode: FLOOD BEAM / Imaging mode: BRIGHT FIELD |
| Experimental equipment |  Model: Titan Krios / Image courtesy: FEI Company |
+ Image processing
Image processing
-Atomic model buiding 1
| Refinement | Space: REAL / Protocol: FLEXIBLE FIT |
|---|---|
| Output model |  PDB-6xlb: |
 Movie
Movie Controller
Controller




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)