+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
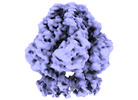
| タイトル | Structure of Primase-Helicase in SaPI5 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Helicase / DNA binding / AMPPNP / REPLICATION | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Qiao CC / Mir-Sanchis I | |||||||||
| 資金援助 |  スウェーデン, 1件 スウェーデン, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nucleic Acids Res / 年: 2022 ジャーナル: Nucleic Acids Res / 年: 2022タイトル: Staphylococcal self-loading helicases couple the staircase mechanism with inter domain high flexibility. 著者: Cuncun Qiao / Gianluca Debiasi-Anders / Ignacio Mir-Sanchis /  要旨: Replication is a crucial cellular process. Replicative helicases unwind DNA providing the template strand to the polymerase and promoting replication fork progression. Helicases are multi-domain ...Replication is a crucial cellular process. Replicative helicases unwind DNA providing the template strand to the polymerase and promoting replication fork progression. Helicases are multi-domain proteins which use an ATPase domain to couple ATP hydrolysis with translocation, however the role that the other domains might have during translocation remains elusive. Here, we studied the unexplored self-loading helicases called Reps, present in Staphylococcus aureus pathogenicity islands (SaPIs). Our cryoEM structures of the PriRep5 from SaPI5 (3.3 Å), the Rep1 from SaPI1 (3.9 Å) and Rep1-DNA complex (3.1Å) showed that in both Reps, the C-terminal domain (CTD) undergoes two distinct movements respect the ATPase domain. We experimentally demonstrate both in vitro and in vivo that SaPI-encoded Reps need key amino acids involved in the staircase mechanism of translocation. Additionally, we demonstrate that the CTD's presence is necessary for the maintenance of full ATPase and helicase activities. We speculate that this high interdomain flexibility couples Rep's activities as initiators and as helicases. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12982.map.gz emd_12982.map.gz | 165.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12982-v30.xml emd-12982-v30.xml emd-12982.xml emd-12982.xml | 17.1 KB 17.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_12982.png emd_12982.png | 88 KB | ||
| マスクデータ |  emd_12982_msk_1.map emd_12982_msk_1.map | 178 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-12982.cif.gz emd-12982.cif.gz | 6.3 KB | ||
| その他 |  emd_12982_half_map_1.map.gz emd_12982_half_map_1.map.gz emd_12982_half_map_2.map.gz emd_12982_half_map_2.map.gz | 139.3 MB 139.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12982 http://ftp.pdbj.org/pub/emdb/structures/EMD-12982 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12982 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12982 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_12982_validation.pdf.gz emd_12982_validation.pdf.gz | 807.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_12982_full_validation.pdf.gz emd_12982_full_validation.pdf.gz | 807.1 KB | 表示 | |
| XML形式データ |  emd_12982_validation.xml.gz emd_12982_validation.xml.gz | 14.9 KB | 表示 | |
| CIF形式データ |  emd_12982_validation.cif.gz emd_12982_validation.cif.gz | 17.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12982 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12982 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12982 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12982 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7om0MC  7olaC  7pdsC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
| 電子顕微鏡画像生データ |  EMPIAR-10881 (タイトル: Staphylococcal self-loading helicases couple the staircase mechanism with inter domain high flexibility EMPIAR-10881 (タイトル: Staphylococcal self-loading helicases couple the staircase mechanism with inter domain high flexibilityData size: 467.6 / Data #1: PriRep5-dsDNA [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12982.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12982.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.82 Å | ||||||||||||||||||||||||||||||||||||
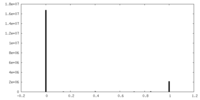
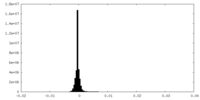
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_12982_msk_1.map emd_12982_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
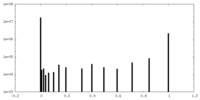
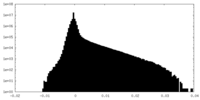
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_12982_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
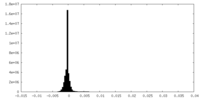
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_12982_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
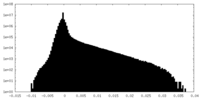
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Primase-Helicase in SaPI5
| 全体 | 名称: Primase-Helicase in SaPI5 |
|---|---|
| 要素 |
|
-超分子 #1: Primase-Helicase in SaPI5
| 超分子 | 名称: Primase-Helicase in SaPI5 / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 669 KDa |
-分子 #1: DNA primase
| 分子 | 名称: DNA primase / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 93.007031 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGHHHHHHAI KKKDRIIGVK ELEIPQELKL VPNWVLWRAE WNEKQQNFGK VPYSINGYRA STTNKKTWCD FESVSIEYEV DEQYSGIGF VLSDGNNFVC LDIDNAIDKK GQINSELALK MMQLTYCEKS PSGTGLHCFF KGKLPDNRKK KRTDLDIELY D SARFMTVT ...文字列: MGHHHHHHAI KKKDRIIGVK ELEIPQELKL VPNWVLWRAE WNEKQQNFGK VPYSINGYRA STTNKKTWCD FESVSIEYEV DEQYSGIGF VLSDGNNFVC LDIDNAIDKK GQINSELALK MMQLTYCEKS PSGTGLHCFF KGKLPDNRKK KRTDLDIELY D SARFMTVT GCTIGQSDIC DNQEVLNTLV DEYFKENLPA NEVVREESNT NIQLSDEDII NIMMKSKQKD KIKDLLQGTY ES YFESSSE AVQSLLHYLA FYTGKNKQQM ERIFLNYNNL TDKWESKRGN TTWGQLELDK AIKNQKTIYT KSIDEFNVIP QGS KDVKQL LNQLGHEERT KMEENWIEEG KRGRKPTTIS PIKCAYILNE HLTFILFDDE ENTKLAMYQF DEGIYTQNTT IIKR VISYL EPKHNSNKAD EVIYHLTNMV DIKEKTNSPY LIPVKNGVFN RKTKQLESFT PDYIFTSKID TSYVRQDIVP EINGW NIDR WIEEIACNDN QVVKLLWQVI NDSMNGNYTR KKAIFFVGDG NNGKGTFQEL LSNVIGYSNI ASLKVNEFDE RFKLSV LEG KTAVIGDDVP VGVYVDDSSN FKSVVTGDPV LVEFKNKPLY RATFKCTVIQ STNGMPKFKD KTGGTLRRLL IVPFNAN FN GIKENFKIKE DYIKNQQVLE YVLYKAINLD FETFDIPDAS KKMLEVFKED NDPVYGFKVN MFDQWTIRKV PKYIVYAF Y KEYCDENGYN ALSSNKFYKQ FEHYLENYWK TDAQRRYDNE ELAKRIYNFN DNRNYIEPIE SGKNYKSYEK VKLKAI UniProtKB: DNA primase |
-分子 #2: PHOSPHOAMINOPHOSPHONIC ACID-ADENYLATE ESTER
| 分子 | 名称: PHOSPHOAMINOPHOSPHONIC ACID-ADENYLATE ESTER / タイプ: ligand / ID: 2 / コピー数: 6 / 式: ANP |
|---|---|
| 分子量 | 理論値: 506.196 Da |
| Chemical component information |  ChemComp-ANP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.4 mg/mL |
|---|---|
| 緩衝液 | pH: 8 / 構成要素 - 濃度: 200.0 mM / 構成要素 - 式: NaCl / 構成要素 - 名称: Sodium Chloride |
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 2 / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: COUNTING / 実像数: 4760 / 平均露光時間: 4.0 sec. / 平均電子線量: 1.16 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 倍率(公称値): 165000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL / 当てはまり具合の基準: Correlation coefficient |
|---|---|
| 得られたモデル |  PDB-7om0: |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)