+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-11950 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of the human mitochondrial HSPD1 single ring | |||||||||
 マップデータ マップデータ | final map filtered by local resolution | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | HSPD1 / Hsp60 / chaperonin / CHAPERONE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報coated vesicle / isotype switching to IgG isotypes / mitochondrial unfolded protein response / TFAP2A acts as a transcriptional repressor during retinoic acid induced cell differentiation / apolipoprotein A-I binding / lipopolysaccharide receptor complex / protein import into mitochondrial intermembrane space / migrasome / high-density lipoprotein particle binding / positive regulation of T cell mediated immune response to tumor cell ...coated vesicle / isotype switching to IgG isotypes / mitochondrial unfolded protein response / TFAP2A acts as a transcriptional repressor during retinoic acid induced cell differentiation / apolipoprotein A-I binding / lipopolysaccharide receptor complex / protein import into mitochondrial intermembrane space / migrasome / high-density lipoprotein particle binding / positive regulation of T cell mediated immune response to tumor cell / Mitochondrial protein import / chaperonin ATPase / positive regulation of macrophage activation / cellular response to interleukin-7 / MyD88-dependent toll-like receptor signaling pathway / biological process involved in interaction with symbiont / 'de novo' protein folding / sperm plasma membrane / B cell proliferation / B cell activation / apolipoprotein binding / DNA replication origin binding / positive regulation of interferon-alpha production / apoptotic mitochondrial changes / protein maturation / positive regulation of interleukin-10 production / response to unfolded protein / chaperone-mediated protein complex assembly / clathrin-coated pit / sperm midpiece / positive regulation of interleukin-12 production / Mitochondrial protein degradation / response to cold / T cell activation / secretory granule / isomerase activity / lipopolysaccharide binding / ATP-dependent protein folding chaperone / : / positive regulation of interleukin-6 production / positive regulation of type II interferon production / double-stranded RNA binding / positive regulation of T cell activation / unfolded protein binding / p53 binding / protein folding / single-stranded DNA binding / protein-folding chaperone binding / protein refolding / mitochondrial inner membrane / early endosome / protein stabilization / mitochondrial matrix / positive regulation of apoptotic process / ubiquitin protein ligase binding / negative regulation of apoptotic process / enzyme binding / cell surface / ATP hydrolysis activity / protein-containing complex / mitochondrion / RNA binding / extracellular space / extracellular exosome / ATP binding / membrane / plasma membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
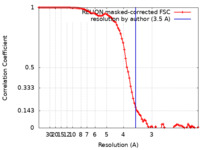
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.5 Å | |||||||||
 データ登録者 データ登録者 | Klebl DP / Feasey MC / Muench SP | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: iScience / 年: 2021 ジャーナル: iScience / 年: 2021タイトル: Cryo-EM structure of human mitochondrial HSPD1. 著者: David P Klebl / Matthew C Feasey / Emma L Hesketh / Neil A Ranson / Heiko Wurdak / Frank Sobott / Robin S Bon / Stephen P Muench /   要旨: Chaperonins play an important role in folding newly synthesized or translocated proteins in all organisms. The bacterial chaperonin GroEL has served as a model system for the understanding of these ...Chaperonins play an important role in folding newly synthesized or translocated proteins in all organisms. The bacterial chaperonin GroEL has served as a model system for the understanding of these proteins. In comparison, its human homolog, known as mitochondrial heat shock protein family member D1 (HSPD1) is poorly understood. Here, we present the structure of HSPD1 in the apo state determined by cryo-electron microscopy (cryo-EM). Unlike GroEL, HSPD1 forms mostly single ring assemblies in the absence of co-chaperonin (HSPE1). Comparison with GroEL shows a rotation and increased flexibility of the apical domain. Together with published structures of the HSPD1/HSPE1 co-chaperonin complex, this work gives insight into the structural changes that occur during the catalytic cycle. This new understanding of HSPD1 structure and its rearrangements upon complex formation may provide new insights for the development of HSPD1-targeting treatments against a diverse range of diseases including glioblastoma. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11950.map.gz emd_11950.map.gz | 39.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11950-v30.xml emd-11950-v30.xml emd-11950.xml emd-11950.xml | 18 KB 18 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_11950_fsc.xml emd_11950_fsc.xml | 9.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_11950.png emd_11950.png | 161.8 KB | ||
| Filedesc metadata |  emd-11950.cif.gz emd-11950.cif.gz | 5.7 KB | ||
| その他 |  emd_11950_additional_1.map.gz emd_11950_additional_1.map.gz emd_11950_half_map_1.map.gz emd_11950_half_map_1.map.gz emd_11950_half_map_2.map.gz emd_11950_half_map_2.map.gz | 48.8 MB 49.4 MB 49.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11950 http://ftp.pdbj.org/pub/emdb/structures/EMD-11950 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11950 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11950 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11950_validation.pdf.gz emd_11950_validation.pdf.gz | 724 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11950_full_validation.pdf.gz emd_11950_full_validation.pdf.gz | 723.6 KB | 表示 | |
| XML形式データ |  emd_11950_validation.xml.gz emd_11950_validation.xml.gz | 15.9 KB | 表示 | |
| CIF形式データ |  emd_11950_validation.cif.gz emd_11950_validation.cif.gz | 21.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11950 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11950 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11950 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11950 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11950.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11950.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | final map filtered by local resolution | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.065 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
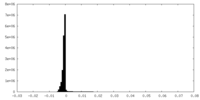
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: unsharpened map
| ファイル | emd_11950_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
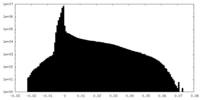
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_11950_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
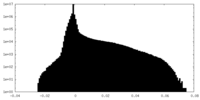
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_11950_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
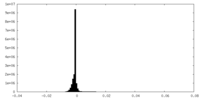
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : human mitochondrial heat shock protein family member D1 (HSPD1)
| 全体 | 名称: human mitochondrial heat shock protein family member D1 (HSPD1) |
|---|---|
| 要素 |
|
-超分子 #1: human mitochondrial heat shock protein family member D1 (HSPD1)
| 超分子 | 名称: human mitochondrial heat shock protein family member D1 (HSPD1) タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: produced by heterologous expression, mature HSPD1, apo state |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: 60 kDa heat shock protein, mitochondrial
| 分子 | 名称: 60 kDa heat shock protein, mitochondrial / タイプ: protein_or_peptide / ID: 1 / コピー数: 7 / 光学異性体: LEVO / EC番号: chaperonin ATPase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 58.306977 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SNAAKDVKFG ADARALMLQG VDLLADAVAV TMGPKGRTVI IEQSWGSPKV TKDGVTVAKS IDLKDKYKNI GAKLVQDVAN NTNEEAGDG TTTATVLARS IAKEGFEKIS KGANPVEIRR GVMLAVDAVI AELKKQSKPV TTPEEIAQVA TISANGDKEI G NIISDAMK ...文字列: SNAAKDVKFG ADARALMLQG VDLLADAVAV TMGPKGRTVI IEQSWGSPKV TKDGVTVAKS IDLKDKYKNI GAKLVQDVAN NTNEEAGDG TTTATVLARS IAKEGFEKIS KGANPVEIRR GVMLAVDAVI AELKKQSKPV TTPEEIAQVA TISANGDKEI G NIISDAMK KVGRKGVITV KDGKTLNDEL EIIEGMKFDR GYISPYFINT SKGQKCEFQD AYVLLSEKKI SSIQSIVPAL EI ANAHRKP LVIIAEDVDG EALSTLVLNR LKVGLQVVAV KAPGFGDNRK NQLKDMAIAT GGAVFGEEGL TLNLEDVQPH DLG KVGEVI VTKDDAMLLK GKGDKAQIEK RIQEIIEQLD VTTSEYEKEK LNERLAKLSD GVAVLKVGGT SDVEVNEKKD RVTD ALNAT RAAVEEGIVL GGGCALLRCI PALDSLTPAN EDQKIGIEII KRTLKIPAMT IAKNAGVEGS LIVEKIMQSS SEVGY DAMA GDFVNMVEKG IIDPTKVVRT ALLDAAGVAS LLTTAEVVVT EIPKEEKDPG MGAMGGMGGG MGGGMF UniProtKB: 60 kDa heat shock protein, mitochondrial |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2.3 mg/mL |
|---|---|
| 緩衝液 | pH: 7.7 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 293 K / 装置: FEI VITROBOT MARK IV / 詳細: blot time 6 s blot force 6. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 平均露光時間: 70.0 sec. / 平均電子線量: 38.5 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)