+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-11469 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | C12 symmetry: Bacterial Vipp1 and PspA are members of the ancient ESCRT-III membrane-remodeling superfamily. | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 | PspA/IM30 / PspA/IM30 family / lipid binding / plasma membrane / Membrane-associated protein Vipp1 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Nostoc punctiforme (バクテリア) Nostoc punctiforme (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.2 Å | |||||||||
 データ登録者 データ登録者 | Liu J / Tassinari M / Souza DP / Naskar S / Noel JK / Bohuszewicz O / Buck M / Williams TA / Baum B / Low HH | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2021 ジャーナル: Cell / 年: 2021タイトル: Bacterial Vipp1 and PspA are members of the ancient ESCRT-III membrane-remodeling superfamily. 著者: Jiwei Liu / Matteo Tassinari / Diorge P Souza / Souvik Naskar / Jeffrey K Noel / Olga Bohuszewicz / Martin Buck / Tom A Williams / Buzz Baum / Harry H Low /   要旨: Membrane remodeling and repair are essential for all cells. Proteins that perform these functions include Vipp1/IM30 in photosynthetic plastids, PspA in bacteria, and ESCRT-III in eukaryotes. Here, ...Membrane remodeling and repair are essential for all cells. Proteins that perform these functions include Vipp1/IM30 in photosynthetic plastids, PspA in bacteria, and ESCRT-III in eukaryotes. Here, using a combination of evolutionary and structural analyses, we show that these protein families are homologous and share a common ancient evolutionary origin that likely predates the last universal common ancestor. This homology is evident in cryo-electron microscopy structures of Vipp1 rings from the cyanobacterium Nostoc punctiforme presented over a range of symmetries. Each ring is assembled from rungs that stack and progressively tilt to form dome-shaped curvature. Assembly is facilitated by hinges in the Vipp1 monomer, similar to those in ESCRT-III proteins, which allow the formation of flexible polymers. Rings have an inner lumen that is able to bind and deform membranes. Collectively, these data suggest conserved mechanistic principles that underlie Vipp1, PspA, and ESCRT-III-dependent membrane remodeling across all domains of life. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11469.map.gz emd_11469.map.gz | 21.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11469-v30.xml emd-11469-v30.xml emd-11469.xml emd-11469.xml | 9.7 KB 9.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_11469.png emd_11469.png | 39.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11469 http://ftp.pdbj.org/pub/emdb/structures/EMD-11469 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11469 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11469 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11469_validation.pdf.gz emd_11469_validation.pdf.gz | 353.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11469_full_validation.pdf.gz emd_11469_full_validation.pdf.gz | 352.9 KB | 表示 | |
| XML形式データ |  emd_11469_validation.xml.gz emd_11469_validation.xml.gz | 6.8 KB | 表示 | |
| CIF形式データ |  emd_11469_validation.cif.gz emd_11469_validation.cif.gz | 7.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11469 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11469 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11469 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11469 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11469.map.gz / 形式: CCP4 / 大きさ: 144.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11469.map.gz / 形式: CCP4 / 大きさ: 144.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.39 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
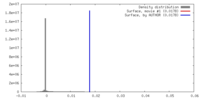
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : vipp1 c12 ring
| 全体 | 名称: vipp1 c12 ring |
|---|---|
| 要素 |
|
-超分子 #1: vipp1 c12 ring
| 超分子 | 名称: vipp1 c12 ring / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Nostoc punctiforme (バクテリア) Nostoc punctiforme (バクテリア) |
| 組換発現 | 生物種:  |
-分子 #1: Vipp1
| 分子 | 名称: Vipp1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 72 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Nostoc punctiforme (バクテリア) Nostoc punctiforme (バクテリア) |
| 分子量 | 理論値: 28.745461 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGLFDRIKRV VSSNLNDLVN KAEDPEKMLE QAILEMQEDL VQLRQGVAQA IAAQKRSEKQ YNDAQNEINK WQRNAQLALQ KGDENLARQ ALERKKTYTD TSAALKASLD TQSTQVETLK RNLIQLESKI SEAKTKKEML KARITTAKAQ EQLQGMVRGM N TSSAMSAF ...文字列: MGLFDRIKRV VSSNLNDLVN KAEDPEKMLE QAILEMQEDL VQLRQGVAQA IAAQKRSEKQ YNDAQNEINK WQRNAQLALQ KGDENLARQ ALERKKTYTD TSAALKASLD TQSTQVETLK RNLIQLESKI SEAKTKKEML KARITTAKAQ EQLQGMVRGM N TSSAMSAF ERMEEKVLMQ ESRAQALGEL AGADLETQFA QLEGGSDVDD ELAALKAQML PPATPVTQAQ LPPQQETTPA KS NEVVDAE LDSLRKQLDQ L |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 1.5 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 7.2 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: RELION / 使用した粒子像数: 7433 |
|---|---|
| 初期 角度割当 | タイプ: NOT APPLICABLE |
| 最終 角度割当 | タイプ: NOT APPLICABLE |
 ムービー
ムービー コントローラー
コントローラー




















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)