+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-10905 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of the P+9 stalled ribosome complex | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | translation / ribosome / rescue / release | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報stringent response / transcriptional attenuation / endoribonuclease inhibitor activity / RNA-binding transcription regulator activity / positive regulation of ribosome biogenesis / negative regulation of cytoplasmic translation / translational termination / DnaA-L2 complex / translation repressor activity / negative regulation of DNA-templated DNA replication initiation ...stringent response / transcriptional attenuation / endoribonuclease inhibitor activity / RNA-binding transcription regulator activity / positive regulation of ribosome biogenesis / negative regulation of cytoplasmic translation / translational termination / DnaA-L2 complex / translation repressor activity / negative regulation of DNA-templated DNA replication initiation / ribosome assembly / mRNA regulatory element binding translation repressor activity / assembly of large subunit precursor of preribosome / cytosolic ribosome assembly / regulation of cell growth / response to reactive oxygen species / DNA-templated transcription termination / response to radiation / ribosomal large subunit assembly / mRNA 5'-UTR binding / large ribosomal subunit / ribosome biogenesis / ribosome binding / ribosomal small subunit biogenesis / ribosomal small subunit assembly / small ribosomal subunit / small ribosomal subunit rRNA binding / transferase activity / 5S rRNA binding / large ribosomal subunit rRNA binding / cytosolic small ribosomal subunit / cytosolic large ribosomal subunit / tRNA binding / cytoplasmic translation / rRNA binding / negative regulation of translation / ribosome / structural constituent of ribosome / ribonucleoprotein complex / translation / response to antibiotic / negative regulation of DNA-templated transcription / mRNA binding / DNA binding / RNA binding / zinc ion binding / metal ion binding / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
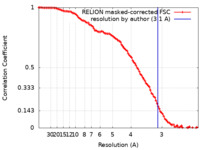
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Chan K-H / Petrychenko V | |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2020 ジャーナル: Nat Commun / 年: 2020タイトル: Mechanism of ribosome rescue by alternative ribosome-rescue factor B. 著者: Kai-Hsin Chan / Valentyn Petrychenko / Claudia Mueller / Cristina Maracci / Wolf Holtkamp / Daniel N Wilson / Niels Fischer / Marina V Rodnina /  要旨: Alternative ribosome-rescue factor B (ArfB) rescues ribosomes stalled on non-stop mRNAs by releasing the nascent polypeptide from the peptidyl-tRNA. By rapid kinetics we show that ArfB selects ...Alternative ribosome-rescue factor B (ArfB) rescues ribosomes stalled on non-stop mRNAs by releasing the nascent polypeptide from the peptidyl-tRNA. By rapid kinetics we show that ArfB selects ribosomes stalled on short truncated mRNAs, rather than on longer mRNAs mimicking pausing on rare codon clusters. In combination with cryo-electron microscopy we dissect the multistep rescue pathway of ArfB, which first binds to ribosomes very rapidly regardless of the mRNA length. The selectivity for shorter mRNAs arises from the subsequent slow engagement step, as it requires longer mRNA to shift to enable ArfB binding. Engagement results in specific interactions of the ArfB C-terminal domain with the mRNA entry channel, which activates peptidyl-tRNA hydrolysis by the N-terminal domain. These data reveal how protein dynamics translate into specificity of substrate recognition and provide insights into the action of a putative rescue factor in mitochondria. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_10905.map.gz emd_10905.map.gz | 466.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-10905-v30.xml emd-10905-v30.xml emd-10905.xml emd-10905.xml | 75.8 KB 75.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_10905_fsc.xml emd_10905_fsc.xml | 10.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_10905.png emd_10905.png | 122.8 KB | ||
| マスクデータ |  emd_10905_msk_1.map emd_10905_msk_1.map | 91.1 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-10905.cif.gz emd-10905.cif.gz | 14.8 KB | ||
| その他 |  emd_10905_half_map_1.map.gz emd_10905_half_map_1.map.gz emd_10905_half_map_2.map.gz emd_10905_half_map_2.map.gz | 71.3 MB 71.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-10905 http://ftp.pdbj.org/pub/emdb/structures/EMD-10905 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10905 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10905 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_10905_validation.pdf.gz emd_10905_validation.pdf.gz | 1.2 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_10905_full_validation.pdf.gz emd_10905_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  emd_10905_validation.xml.gz emd_10905_validation.xml.gz | 19.5 KB | 表示 | |
| CIF形式データ |  emd_10905_validation.cif.gz emd_10905_validation.cif.gz | 24.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10905 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10905 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10905 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10905 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6ysrMC  6yssC  6ystC  6ysuC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10443 (タイトル: Mechanism of Ribosome Rescue by Alternative Release Factor B EMPIAR-10443 (タイトル: Mechanism of Ribosome Rescue by Alternative Release Factor BData size: 788.2 Data #1: Motion-corrected, dose-weighted micrographs & polished particles of P+9 E. coli ribosome-ArfB complex [micrographs - single frame] Data #2: Motion-corrected, dose-weighted micrographs & extracted particles of P+0 E. coli ribosome-ArfB complex [micrographs - single frame]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_10905.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_10905.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.6525 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_10905_msk_1.map emd_10905_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_10905_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_10905_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Stalled E. Coli P+9 ribosome complex 70S-fMet-Phe-tRNAPhe-mRNA
+超分子 #1: Stalled E. Coli P+9 ribosome complex 70S-fMet-Phe-tRNAPhe-mRNA
+分子 #1: 50S ribosomal protein L32
+分子 #2: 50S ribosomal protein L33
+分子 #3: 50S ribosomal protein L34
+分子 #4: 50S ribosomal protein L35
+分子 #5: 50S ribosomal protein L36
+分子 #6: 50S ribosomal protein L10
+分子 #7: 50S ribosomal protein L31
+分子 #10: 50S ribosomal protein L2
+分子 #11: 50S ribosomal protein L3
+分子 #12: 50S ribosomal protein L4
+分子 #13: 50S ribosomal protein L5
+分子 #14: 50S ribosomal protein L6
+分子 #15: 50S ribosomal protein L9
+分子 #16: 50S ribosomal protein L11
+分子 #17: 50S ribosomal protein L13
+分子 #18: 50S ribosomal protein L14
+分子 #19: 50S ribosomal protein L15
+分子 #20: 50S ribosomal protein L16
+分子 #21: 50S ribosomal protein L17
+分子 #22: 50S ribosomal protein L18
+分子 #23: 50S ribosomal protein L19
+分子 #24: 50S ribosomal protein L20
+分子 #25: 50S ribosomal protein L21
+分子 #26: 50S ribosomal protein L22
+分子 #27: 50S ribosomal protein L23
+分子 #28: 50S ribosomal protein L24
+分子 #29: 50S ribosomal protein L25
+分子 #30: 50S ribosomal protein L27
+分子 #31: 50S ribosomal protein L28
+分子 #32: 50S ribosomal protein L29
+分子 #33: 50S ribosomal protein L30
+分子 #35: 30S ribosomal protein S2
+分子 #36: 30S ribosomal protein S3
+分子 #37: 30S ribosomal protein S4
+分子 #38: 30S ribosomal protein S5
+分子 #39: 30S ribosomal protein S6
+分子 #40: 30S ribosomal protein S7
+分子 #41: 30S ribosomal protein S8
+分子 #42: 30S ribosomal protein S9
+分子 #43: 30S ribosomal protein S10
+分子 #44: 30S ribosomal protein S11
+分子 #45: 30S ribosomal protein S12
+分子 #46: 30S ribosomal protein S13
+分子 #47: 30S ribosomal protein S14
+分子 #48: 30S ribosomal protein S15
+分子 #49: 30S ribosomal protein S16
+分子 #50: 30S ribosomal protein S17
+分子 #51: 30S ribosomal protein S18
+分子 #52: 30S ribosomal protein S19
+分子 #53: 30S ribosomal protein S20
+分子 #54: 30S ribosomal protein S21
+分子 #55: P-site fMet-Phe-tRNA(Phe)
+分子 #8: 23S ribosomal RNA
+分子 #9: 5S ribosomal RNA
+分子 #34: 16S ribosomal RNA
+分子 #56: P-site fMet-Phe-tRNA(Phe)
+分子 #57: mRNA
+分子 #58: MAGNESIUM ION
+分子 #59: ZINC ION
+分子 #60: CHLORIDE ION
+分子 #61: SODIUM ION
+分子 #62: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 / 詳細: 50 mM HEPES, 30 mM KCl, 7 mM MgCl2 |
|---|---|
| グリッド | モデル: Quantifoil R3.5/1 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 前処理 - タイプ: GLOW DISCHARGE / 詳細: Custom-made glow-discharge instrument |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 277 K / 装置: HOMEMADE PLUNGER / 詳細: Manual blotting & plunge-freezing. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 特殊光学系 | 球面収差補正装置: Cs image corrector (CEOS company) |
| 詳細 | Aberration corrections performed using Cs image corrector (CEOS company) |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: INTEGRATING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 平均電子線量: 50.0 e/Å2 詳細: Images were collected in movie mode at 40 fractions per image per second |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 最大 デフォーカス(補正後): 2.5 µm / 最小 デフォーカス(補正後): 0.2 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 0.01 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.2 µm / 倍率(公称値): 59000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
























 Z
Z Y
Y X
X