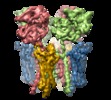
登録情報 データベース : EMDB / ID : EMD-8721タイトル Structure of AMPA receptor-TARP complex protein complex 複合体 : Fully occupied GluA2 AMPA receptor - TARP complex bound with quisqualate and (R,R)-2bタンパク質・ペプチド : Glutamate receptor 2タンパク質・ペプチド : Voltage-dependent calcium channel gamma-2 subunit / / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Rattus norvegicus (ドブネズミ)手法 / / 解像度 : 4.9 Å Chen S / Zhao Y / Wang YS / Shekhar M / Gouaux E 資金援助 Organization Grant number 国 National Institutes of Health/National Institute of Neurological Disorders and Stroke (NIH/NINDS) NS-038631 National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS) P41-GM104601 National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS) U54-GM087519
ジャーナル : Cell / 年 : 2017タイトル : Activation and Desensitization Mechanism of AMPA Receptor-TARP Complex by Cryo-EM.著者 : Shanshuang Chen / Yan Zhao / Yuhang Wang / Mrinal Shekhar / Emad Tajkhorshid / Eric Gouaux / 要旨 : AMPA receptors mediate fast excitatory neurotransmission in the mammalian brain and transduce the binding of presynaptically released glutamate to the opening of a transmembrane cation channel. ... AMPA receptors mediate fast excitatory neurotransmission in the mammalian brain and transduce the binding of presynaptically released glutamate to the opening of a transmembrane cation channel. Within the postsynaptic density, however, AMPA receptors coassemble with transmembrane AMPA receptor regulatory proteins (TARPs), yielding a receptor complex with altered gating kinetics, pharmacology, and pore properties. Here, we elucidate structures of the GluA2-TARP γ2 complex in the presence of the partial agonist kainate or the full agonist quisqualate together with a positive allosteric modulator or with quisqualate alone. We show how TARPs sculpt the ligand-binding domain gating ring, enhancing kainate potency and diminishing the ensemble of desensitized states. TARPs encircle the receptor ion channel, stabilizing M2 helices and pore loops, illustrating how TARPs alter receptor pore properties. Structural and computational analysis suggests the full agonist and modulator complex harbors an ion-permeable channel gate, providing the first view of an activated AMPA receptor. 履歴 ヘッダ(付随情報) 公開 2016年7月6日 - マップ公開 2016年7月6日 - 登録 2017年5月3日 - 更新 2024年10月23日 - 現状 2024年10月23日 処理サイト : RCSB / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報
 データ登録者
データ登録者 米国, 3件
米国, 3件  引用
引用 ジャーナル: Cell / 年: 2017
ジャーナル: Cell / 年: 2017
 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_8721.map.gz
emd_8721.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-8721-v30.xml
emd-8721-v30.xml emd-8721.xml
emd-8721.xml EMDBヘッダ
EMDBヘッダ emd_8721.png
emd_8721.png emd-8721.cif.gz
emd-8721.cif.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-8721
http://ftp.pdbj.org/pub/emdb/structures/EMD-8721 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8721
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8721 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_8721.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_8721.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) 試料の構成要素
試料の構成要素

 Homo sapiens (ヒト)
Homo sapiens (ヒト)
 Homo sapiens (ヒト)
Homo sapiens (ヒト) 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 画像解析
画像解析
 ムービー
ムービー コントローラー
コントローラー




















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















