+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8595 | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM Structure Refinement by Integrating NMR Chemical Shifts with Molecular Dynamics Simulations | |||||||||||||||||||||
 マップデータ マップデータ | HIV-1 CA hexamer | |||||||||||||||||||||
 試料 試料 |
| |||||||||||||||||||||
 キーワード キーワード | Cryo-EM / HIV capsid / Chemical shift / Molecular Dynamics / hydrolase / viral protein | |||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報viral budding via host ESCRT complex / ISG15 antiviral mechanism / host multivesicular body / viral nucleocapsid / viral translational frameshifting / host cell nucleus / host cell plasma membrane / virion membrane / structural molecule activity / RNA binding ...viral budding via host ESCRT complex / ISG15 antiviral mechanism / host multivesicular body / viral nucleocapsid / viral translational frameshifting / host cell nucleus / host cell plasma membrane / virion membrane / structural molecule activity / RNA binding / zinc ion binding / membrane 類似検索 - 分子機能 | |||||||||||||||||||||
| 生物種 |  Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) | |||||||||||||||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 5.0 Å | |||||||||||||||||||||
 データ登録者 データ登録者 | Zhao G / Zhang P | |||||||||||||||||||||
| 資金援助 |  米国, 6件 米国, 6件
| |||||||||||||||||||||
 引用 引用 |  ジャーナル: J Phys Chem B / 年: 2017 ジャーナル: J Phys Chem B / 年: 2017タイトル: CryoEM Structure Refinement by Integrating NMR Chemical Shifts with Molecular Dynamics Simulations. 著者: Juan R Perilla / Gongpu Zhao / Manman Lu / Jiying Ning / Guangjin Hou / In-Ja L Byeon / Angela M Gronenborn / Tatyana Polenova / Peijun Zhang /   要旨: Single particle cryoEM has emerged as a powerful method for structure determination of proteins and complexes, complementing X-ray crystallography and NMR spectroscopy. Yet, for many systems, the ...Single particle cryoEM has emerged as a powerful method for structure determination of proteins and complexes, complementing X-ray crystallography and NMR spectroscopy. Yet, for many systems, the resolution of cryoEM density map has been limited to 4-6 Å, which only allows for resolving bulky amino acids side chains, thus hindering accurate model building from the density map. On the other hand, experimental chemical shifts (CS) from solution and solid state MAS NMR spectra provide atomic level data for each amino acid within a molecule or a complex; however, structure determination of large complexes and assemblies based on NMR data alone remains challenging. Here, we present a novel integrated strategy to combine the highly complementary experimental data from cryoEM and NMR computationally by molecular dynamics simulations to derive an atomistic model, which is not attainable by either approach alone. We use the HIV-1 capsid protein (CA) C-terminal domain as well as the large capsid assembly to demonstrate the feasibility of this approach, termed NMR CS-biased cryoEM structure refinement. | |||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8595.map.gz emd_8595.map.gz | 338.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8595-v30.xml emd-8595-v30.xml emd-8595.xml emd-8595.xml | 15 KB 15 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_8595_fsc.xml emd_8595_fsc.xml | 16 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_8595.png emd_8595.png | 141.6 KB | ||
| Filedesc metadata |  emd-8595.cif.gz emd-8595.cif.gz | 6.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8595 http://ftp.pdbj.org/pub/emdb/structures/EMD-8595 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8595 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8595 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8595.map.gz / 形式: CCP4 / 大きさ: 361.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8595.map.gz / 形式: CCP4 / 大きさ: 361.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | HIV-1 CA hexamer | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.22 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
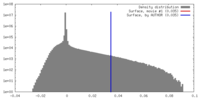
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : HIV-1 Capsid Protein Assembly
| 全体 | 名称: HIV-1 Capsid Protein Assembly |
|---|---|
| 要素 |
|
-超分子 #1: HIV-1 Capsid Protein Assembly
| 超分子 | 名称: HIV-1 Capsid Protein Assembly / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) |
| 分子量 | 理論値: 24 kDa/nm |
-分子 #1: Gag polyprotein
| 分子 | 名称: Gag polyprotein / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) Human immunodeficiency virus type 1 (NEW YORK-5 ISOLATE) (ヒト免疫不全ウイルス) |
| 分子量 | 理論値: 24.654268 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: PIVQNLQGQM VHQAISPRTL NAWVKVVEEK AFSPEVIPMF SALSEGATPQ DLNTMLNTVG GHQAAMQMLK ETINEEAAEW DRLHPVHAG PIAPGQMREP RGSDIAGTTS TLQEQIGWMT HNPPIPVGEI YKRWIILGLN KIVRMYSPTS ILDIRQGPKE P FRDYVDRF ...文字列: PIVQNLQGQM VHQAISPRTL NAWVKVVEEK AFSPEVIPMF SALSEGATPQ DLNTMLNTVG GHQAAMQMLK ETINEEAAEW DRLHPVHAG PIAPGQMREP RGSDIAGTTS TLQEQIGWMT HNPPIPVGEI YKRWIILGLN KIVRMYSPTS ILDIRQGPKE P FRDYVDRF YKTLRAEQAS QEVKNWMTET LLVQNANPDC KTILKALGPG ATLEEMMTAC QGV UniProtKB: Gag polyprotein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | helical array |
- 試料調製
試料調製
| 濃度 | 2 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| |||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 支持フィルム - Film thickness: 10 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 25 sec. / 前処理 - 雰囲気: AIR | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: HOMEMADE PLUNGER 詳細: The assembled sample (1.5 microliter) was applied to the carbon side of a glow discharged perforated Quantifoil grid, followed by application of 3 microliter of low salt buffer (100 milimolar ...詳細: The assembled sample (1.5 microliter) was applied to the carbon side of a glow discharged perforated Quantifoil grid, followed by application of 3 microliter of low salt buffer (100 milimolar NaCl, 50 milimolar Tris pH 8.0) on the back side of the grid, and blotting, from the back side, with a filter paper, before plunge-freezing in liquid ethane. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 実像数: 523 / 平均露光時間: 6.0 sec. / 平均電子線量: 41.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.2 mm / 最大 デフォーカス(公称値): 2.2 µm 最小 デフォーカス(公称値): 0.7000000000000001 µm 倍率(公称値): 31000 |
| 試料ステージ | 試料ホルダーモデル: SIDE ENTRY, EUCENTRIC / ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)