+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6om6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of trans-translation inhibitor bound to E. coli 70S ribosome with P site tRNA | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 要素 要素 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 キーワード キーワード | RIBOSOME / trans-translation / translation / antibiotic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報positive regulation of ribosome biogenesis / DnaA-L2 complex / negative regulation of DNA-templated DNA replication initiation / assembly of large subunit precursor of preribosome / cytosolic ribosome assembly / regulation of cell growth / mRNA 5'-UTR binding / large ribosomal subunit / ribosome binding / transferase activity ...positive regulation of ribosome biogenesis / DnaA-L2 complex / negative regulation of DNA-templated DNA replication initiation / assembly of large subunit precursor of preribosome / cytosolic ribosome assembly / regulation of cell growth / mRNA 5'-UTR binding / large ribosomal subunit / ribosome binding / transferase activity / small ribosomal subunit / 5S rRNA binding / small ribosomal subunit rRNA binding / ribosomal large subunit assembly / cytosolic small ribosomal subunit / cytosolic large ribosomal subunit / cytoplasmic translation / tRNA binding / rRNA binding / structural constituent of ribosome / ribosome / translation / ribonucleoprotein complex / mRNA binding / RNA binding / zinc ion binding / metal ion binding / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 生物種 |  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 データ登録者 データ登録者 | Hoffer, E.D. / Mehrani, A. / Keiler, K.C. / Stagg, S.M. / Dunham, C.M. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2021 ジャーナル: Nat Commun / 年: 2021タイトル: trans-Translation inhibitors bind to a novel site on the ribosome and clear Neisseria gonorrhoeae in vivo. 著者: Zachary D Aron / Atousa Mehrani / Eric D Hoffer / Kristie L Connolly / Pooja Srinivas / Matthew C Torhan / John N Alumasa / Mynthia Cabrera / Divya Hosangadi / Jay S Barbor / Steven C ...著者: Zachary D Aron / Atousa Mehrani / Eric D Hoffer / Kristie L Connolly / Pooja Srinivas / Matthew C Torhan / John N Alumasa / Mynthia Cabrera / Divya Hosangadi / Jay S Barbor / Steven C Cardinale / Steven M Kwasny / Lucas R Morin / Michelle M Butler / Timothy J Opperman / Terry L Bowlin / Ann Jerse / Scott M Stagg / Christine M Dunham / Kenneth C Keiler /  要旨: Bacterial ribosome rescue pathways that remove ribosomes stalled on mRNAs during translation have been proposed as novel antibiotic targets because they are essential in bacteria and are not ...Bacterial ribosome rescue pathways that remove ribosomes stalled on mRNAs during translation have been proposed as novel antibiotic targets because they are essential in bacteria and are not conserved in humans. We previously reported the discovery of a family of acylaminooxadiazoles that selectively inhibit trans-translation, the main ribosome rescue pathway in bacteria. Here, we report optimization of the pharmacokinetic and antibiotic properties of the acylaminooxadiazoles, producing MBX-4132, which clears multiple-drug resistant Neisseria gonorrhoeae infection in mice after a single oral dose. Single particle cryogenic-EM studies of non-stop ribosomes show that acylaminooxadiazoles bind to a unique site near the peptidyl-transfer center and significantly alter the conformation of ribosomal protein bL27, suggesting a novel mechanism for specific inhibition of trans-translation by these molecules. These results show that trans-translation is a viable therapeutic target and reveal a new conformation within the bacterial ribosome that may be critical for ribosome rescue pathways. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6om6.cif.gz 6om6.cif.gz | 3.1 MB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6om6.ent.gz pdb6om6.ent.gz | 表示 |  PDB形式 PDB形式 | |
| PDBx/mmJSON形式 |  6om6.json.gz 6om6.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  6om6_validation.pdf.gz 6om6_validation.pdf.gz | 1.9 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  6om6_full_validation.pdf.gz 6om6_full_validation.pdf.gz | 2.1 MB | 表示 | |
| XML形式データ |  6om6_validation.xml.gz 6om6_validation.xml.gz | 220.1 KB | 表示 | |
| CIF形式データ |  6om6_validation.cif.gz 6om6_validation.cif.gz | 376.5 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/om/6om6 https://data.pdbj.org/pub/pdb/validation_reports/om/6om6 ftp://data.pdbj.org/pub/pdb/validation_reports/om/6om6 ftp://data.pdbj.org/pub/pdb/validation_reports/om/6om6 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-RNA鎖 , 5種, 5分子 12345
| #1: RNA鎖 | 分子量: 941804.625 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
|---|---|
| #2: RNA鎖 | 分子量: 497405.969 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #3: RNA鎖 | 分子量: 38790.090 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #4: RNA鎖 | 分子量: 1609.048 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #5: RNA鎖 | 分子量: 24453.486 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
+50S ribosomal protein ... , 29種, 29分子 BCDEFGJKLMNOPQRSTUVXYZabcdefW
-30S ribosomal protein ... , 20種, 20分子 ghijklmnopqrstuvwxyz
| #34: タンパク質 | 分子量: 26781.670 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
|---|---|
| #35: タンパク質 | 分子量: 26031.316 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #36: タンパク質 | 分子量: 23514.199 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #37: タンパク質 | 分子量: 17629.398 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #38: タンパク質 | 分子量: 15727.512 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #39: タンパク質 | 分子量: 20055.156 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #40: タンパク質 | 分子量: 14146.557 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #41: タンパク質 | 分子量: 14886.270 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #42: タンパク質 | 分子量: 11755.597 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #43: タンパク質 | 分子量: 13870.975 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #44: タンパク質 | 分子量: 13814.249 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #45: タンパク質 | 分子量: 13128.467 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #46: タンパク質 | 分子量: 11606.560 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #47: タンパク質 | 分子量: 10290.816 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #48: タンパク質 | 分子量: 9207.572 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #49: タンパク質 | 分子量: 9724.491 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #50: タンパク質 | 分子量: 9005.472 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #51: タンパク質 | 分子量: 10455.355 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #52: タンパク質 | 分子量: 9708.464 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| #53: タンパク質 | 分子量: 8524.039 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
-非ポリマー , 1種, 1分子 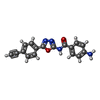
| #55: 化合物 | ChemComp-KKL / |
|---|
-詳細
| Has protein modification | Y |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 |
| |||||||||||||||||||||||||
| 由来(天然) |
| |||||||||||||||||||||||||
| 緩衝液 | pH: 7.6 | |||||||||||||||||||||||||
| 緩衝液成分 |
| |||||||||||||||||||||||||
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | |||||||||||||||||||||||||
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: UltrAuFoil | |||||||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 281.15 K / 詳細: Blot time: 3.5 seconds |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 59000 X / 最大 デフォーカス(公称値): 3000 nm / 最小 デフォーカス(公称値): 1500 nm / Cs: 2.7 mm / C2レンズ絞り径: 70 µm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 19.302 sec. / 電子線照射量: 58 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: DIRECT ELECTRON DE-64 (8k x 8k) 撮影したグリッド数: 2 / 実像数: 2197 詳細: Two separate datesets were combined. The imaging parameter was the same for both datasets. Firth data-set had 1752 micrographs. Second data-set had 445 micrographs. |
| 画像スキャン | サンプリングサイズ: 6.5 µm / 横: 4096 / 縦: 4096 / 動画フレーム数/画像: 78 / 利用したフレーム数/画像: 1-78 |
- 解析
解析
| ソフトウェア | 名称: PHENIX / 分類: 精密化 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 画像処理 | 詳細: Counting mode was used. The 8k x 8k pixels were binned by two using hardware binning to increase the frame rate. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 474382 詳細: 100,537 particles were selected from first dataset and 373,845 partciles from the second dataset. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 28121 / アルゴリズム: BACK PROJECTION / クラス平均像の数: 1 / 対称性のタイプ: POINT | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / 空間: REAL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 5MDV Accession code: 5MDV / Source name: PDB / タイプ: experimental model | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso max: 897.78 Å2 / Biso mean: 169.8625 Å2 / Biso min: 96.44 Å2 |
 ムービー
ムービー コントローラー
コントローラー
























 PDBj
PDBj































