+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-6128 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Negative stain random conical tilt reconstructions of E. coli ribosomal 30S subunit assembly intermediates | |||||||||
 マップデータ マップデータ | Group IV 30S assembly intermediate from wild-type E. coli (Figure 2D) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Ribosome assembly / 30S subunit / Assembly intermediate | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 51.0 Å | |||||||||
 データ登録者 データ登録者 | Sashital DG / Greeman CA / Lyumkis D / Potter CS / Carragher B / Williamson JR | |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2014 ジャーナル: Elife / 年: 2014タイトル: A combined quantitative mass spectrometry and electron microscopy analysis of ribosomal 30S subunit assembly in E. coli. 著者: Dipali G Sashital / Candacia A Greeman / Dmitry Lyumkis / Clinton S Potter / Bridget Carragher / James R Williamson /  要旨: Ribosome assembly is a complex process involving the folding and processing of ribosomal RNAs (rRNAs), concomitant binding of ribosomal proteins (r-proteins), and participation of numerous accessory ...Ribosome assembly is a complex process involving the folding and processing of ribosomal RNAs (rRNAs), concomitant binding of ribosomal proteins (r-proteins), and participation of numerous accessory cofactors. Here, we use a quantitative mass spectrometry/electron microscopy hybrid approach to determine the r-protein composition and conformation of 30S ribosome assembly intermediates in Escherichia coli. The relative timing of assembly of the 3' domain and the formation of the central pseudoknot (PK) structure depends on the presence of the assembly factor RimP. The central PK is unstable in the absence of RimP, resulting in the accumulation of intermediates in which the 3'-domain is unanchored and the 5'-domain is depleted for r-proteins S5 and S12 that contact the central PK. Our results reveal the importance of the cofactor RimP in central PK formation, and introduce a broadly applicable method for characterizing macromolecular assembly in cells. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_6128.map.gz emd_6128.map.gz | 20.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-6128-v30.xml emd-6128-v30.xml emd-6128.xml emd-6128.xml | 12 KB 12 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  400_6128.gif 400_6128.gif 80_6128.gif 80_6128.gif | 23.7 KB 2.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-6128 http://ftp.pdbj.org/pub/emdb/structures/EMD-6128 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6128 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6128 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_6128_validation.pdf.gz emd_6128_validation.pdf.gz | 77.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_6128_full_validation.pdf.gz emd_6128_full_validation.pdf.gz | 77 KB | 表示 | |
| XML形式データ |  emd_6128_validation.xml.gz emd_6128_validation.xml.gz | 493 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6128 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6128 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6128 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6128 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6125C  6126C  6127C  6129C  6130C  6131C  6132C  6133C  6134C  6135C  6136C  6137C  6138C  6139C  6140C  6141C  6142C  6143C 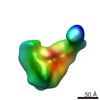 6144C  6145C C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_6128.map.gz / 形式: CCP4 / 大きさ: 41.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_6128.map.gz / 形式: CCP4 / 大きさ: 41.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Group IV 30S assembly intermediate from wild-type E. coli (Figure 2D) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.0504 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
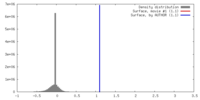
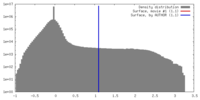
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Group IV 30S ribosomal subunit assembly intermediate from wild-ty...
| 全体 | 名称: Group IV 30S ribosomal subunit assembly intermediate from wild-type E. coli |
|---|---|
| 要素 |
|
-超分子 #1000: Group IV 30S ribosomal subunit assembly intermediate from wild-ty...
| 超分子 | 名称: Group IV 30S ribosomal subunit assembly intermediate from wild-type E. coli タイプ: sample / ID: 1000 詳細: Group IV particles from heterogeneous sample taken from the center of the 30S sucrose gradient peak Number unique components: 1 |
|---|---|
| 分子量 | 理論値: 820 KDa 手法: Sedimentation and calculation of MW of known components |
-超分子 #1: 30S assembly intermediate
| 超分子 | 名称: 30S assembly intermediate / タイプ: complex / ID: 1 / Name.synonym: 30S ribosomal subunit / 詳細: Particles from center of 30S sucrose gradient peak / 組換発現: No / データベース: NCBI / Ribosome-details: ribosome-prokaryote: SSU 30S, PSR16s |
|---|---|
| Ref GO | 0: GO:0005840 |
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 820 KDa |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.015 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 20 mM Tris, pH 7.5, 100 mM NH4Cl, 10 mM MgCl2, 0.5 mM EDTA, 6 mM 2-mercaptoethanol |
| 染色 | タイプ: NEGATIVE 詳細: Negative stain grids were prepared by applying the sample (3 uL) to the grid for 1 min, then blotting from the side to remove excess sample. The grid was washed immediately with 3 uL Buffer ...詳細: Negative stain grids were prepared by applying the sample (3 uL) to the grid for 1 min, then blotting from the side to remove excess sample. The grid was washed immediately with 3 uL Buffer A, then blotted from the side. Concurrent with blotting, 3 uL of fresh 2% uranyl formate was applied to the grid, then blotted from the side. This step was repeated twice, then the grid was allowed to dry for at least 10 minutes. |
| グリッド | 詳細: C-flat grids (Protochips) with 2 micron diameter holes coated with a thin (2-5 nm) layer of continuous carbon support, plasma-cleaned for 5s |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI SPIRIT |
|---|---|
| 温度 | 最低: 298 K |
| アライメント法 | Legacy - 非点収差: Objective lens astigmatism was corrected at 52,000 times magnification using a live image of the power spectrum. |
| 日付 | 2013年5月27日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: TVIPS TEMCAM-F416 (4k x 4k) 実像数: 900 / 平均電子線量: 20 e/Å2 / 詳細: 450 tilt pairs were collected at -50 and 0 degrees. |
| Tilt angle max | 0 |
| 電子線 | 加速電圧: 120 kV / 電子線源: LAB6 |
| 電子光学系 | 倍率(補正後): 52000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2 mm / 最大 デフォーカス(公称値): 2.25 µm / 最小 デフォーカス(公称値): 0.79 µm / 倍率(公称値): 52000 |
| 試料ステージ | 試料ホルダーモデル: SIDE ENTRY, EUCENTRIC / Tilt angle min: -50 |
| 実験機器 |  モデル: Tecnai Spirit / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | Image tilt pairs were collected (-50 and 0 degrees) and particle tilt pairs were identified and extracted as two separate stacks. The untilted stack was aligned and classified iteratively, and RCT volumes were created for a single class average by applying alignment parameters to the corresponding tilt pairs. |
|---|---|
| CTF補正 | 詳細: Each micrograph |
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 51.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: Spider, Appion / 詳細: RCT reconstruction / 使用した粒子像数: 473 |
| 最終 2次元分類 | クラス数: 1 |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)