| 登録情報 | データベース: PDB / ID: 5w8j
|
|---|
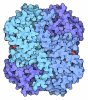
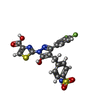
| タイトル | Crystal Structure of Lactate Dehydrogenase A in complex with inhibitor compound 29 |
|---|
 要素 要素 | L-lactate dehydrogenase A chain |
|---|
 キーワード キーワード | OXIDOREDUCTASE / oxidoreductase inhibitor |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
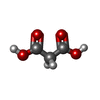
sperm fibrous sheath / pyruvate catabolic process / oxidoreductase complex / L-lactate dehydrogenase / L-lactate dehydrogenase (NAD+) activity / Pyruvate metabolism / lactate metabolic process / : / substantia nigra development / Regulation of pyruvate metabolism ...sperm fibrous sheath / pyruvate catabolic process / oxidoreductase complex / L-lactate dehydrogenase / L-lactate dehydrogenase (NAD+) activity / Pyruvate metabolism / lactate metabolic process / : / substantia nigra development / Regulation of pyruvate metabolism / glycolytic process / cadherin binding / mitochondrion / extracellular exosome / membrane / identical protein binding / nucleus / cytosol類似検索 - 分子機能 L-lactate dehydrogenase / L-lactate dehydrogenase active site. / L-lactate dehydrogenase, active site / L-2-Hydroxyisocaproate Dehydrogenase; Chain A, domain 2 / Lactate dehydrogenase/glycoside hydrolase, family 4, C-terminal / L-lactate/malate dehydrogenase / Lactate/malate dehydrogenase, N-terminal / Lactate/malate dehydrogenase, C-terminal / lactate/malate dehydrogenase, NAD binding domain / lactate/malate dehydrogenase, alpha/beta C-terminal domain ...L-lactate dehydrogenase / L-lactate dehydrogenase active site. / L-lactate dehydrogenase, active site / L-2-Hydroxyisocaproate Dehydrogenase; Chain A, domain 2 / Lactate dehydrogenase/glycoside hydrolase, family 4, C-terminal / L-lactate/malate dehydrogenase / Lactate/malate dehydrogenase, N-terminal / Lactate/malate dehydrogenase, C-terminal / lactate/malate dehydrogenase, NAD binding domain / lactate/malate dehydrogenase, alpha/beta C-terminal domain / Lactate dehydrogenase/glycoside hydrolase, family 4, C-terminal / NAD(P)-binding Rossmann-like Domain / NAD(P)-binding domain superfamily / Alpha-Beta Complex / Rossmann fold / 3-Layer(aba) Sandwich / Alpha Beta類似検索 - ドメイン・相同性 Chem-9Y7 / MALONIC ACID / L-lactate dehydrogenase A chain類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.55 Å 分子置換 / 解像度: 1.55 Å |
|---|
 データ登録者 データ登録者 | Lukacs, C.M. / Moulin, A. |
|---|
 引用 引用 |  ジャーナル: J. Med. Chem. / 年: 2017 ジャーナル: J. Med. Chem. / 年: 2017
タイトル: Discovery and Optimization of Potent, Cell-Active Pyrazole-Based Inhibitors of Lactate Dehydrogenase (LDH).
著者: Rai, G. / Brimacombe, K.R. / Mott, B.T. / Urban, D.J. / Hu, X. / Yang, S.M. / Lee, T.D. / Cheff, D.M. / Kouznetsova, J. / Benavides, G.A. / Pohida, K. / Kuenstner, E.J. / Luci, D.K. / Lukacs, ...著者: Rai, G. / Brimacombe, K.R. / Mott, B.T. / Urban, D.J. / Hu, X. / Yang, S.M. / Lee, T.D. / Cheff, D.M. / Kouznetsova, J. / Benavides, G.A. / Pohida, K. / Kuenstner, E.J. / Luci, D.K. / Lukacs, C.M. / Davies, D.R. / Dranow, D.M. / Zhu, H. / Sulikowski, G. / Moore, W.J. / Stott, G.M. / Flint, A.J. / Hall, M.D. / Darley-Usmar, V.M. / Neckers, L.M. / Dang, C.V. / Waterson, A.G. / Simeonov, A. / Jadhav, A. / Maloney, D.J. |
|---|
| 履歴 | | 登録 | 2017年6月21日 | 登録サイト: RCSB / 処理サイト: RCSB |
|---|
| 改定 1.0 | 2018年1月17日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2024年3月13日 | Group: Data collection / Database references / カテゴリ: chem_comp_atom / chem_comp_bond / database_2
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession |
|---|
| 改定 1.2 | 2024年4月3日 | Group: Refinement description / カテゴリ: pdbx_initial_refinement_model |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 1.55 Å
分子置換 / 解像度: 1.55 Å  データ登録者
データ登録者 引用
引用 ジャーナル: J. Med. Chem. / 年: 2017
ジャーナル: J. Med. Chem. / 年: 2017 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 5w8j.cif.gz
5w8j.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb5w8j.ent.gz
pdb5w8j.ent.gz PDB形式
PDB形式 5w8j.json.gz
5w8j.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード https://data.pdbj.org/pub/pdb/validation_reports/w8/5w8j
https://data.pdbj.org/pub/pdb/validation_reports/w8/5w8j ftp://data.pdbj.org/pub/pdb/validation_reports/w8/5w8j
ftp://data.pdbj.org/pub/pdb/validation_reports/w8/5w8j リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 遺伝子: LDHA, PIG19 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: LDHA, PIG19 / 発現宿主: 







 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  CLSI
CLSI  / ビームライン: 08ID-1 / 波長: 0.97949 Å
/ ビームライン: 08ID-1 / 波長: 0.97949 Å 解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー

















 PDBj
PDBj