+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of human METTL1-WDR4 in complex with Lys-tRNA and SAH. | ||||||||||||
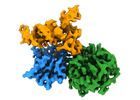
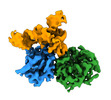
 マップデータ マップデータ | Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH. Full map. | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | Cancer protein / Methyl transferase / TRANSFERASE / TRANSFERASE-RNA complex | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報internal mRNA (guanine-N7-)-methyltransferase activity / tRNA stabilization / tRNA (m7G46) methyltransferase complex / tRNA (guanine-N7)-methylation / RNA (guanine-N7)-methylation / tRNA (guanine46-N7)-methyltransferase / tRNA (guanine(46)-N7)-methyltransferase activity / tRNA methyltransferase activator activity / tRNA methyltransferase complex / tRNA modification in the nucleus and cytosol ...internal mRNA (guanine-N7-)-methyltransferase activity / tRNA stabilization / tRNA (m7G46) methyltransferase complex / tRNA (guanine-N7)-methylation / RNA (guanine-N7)-methylation / tRNA (guanine46-N7)-methyltransferase / tRNA (guanine(46)-N7)-methyltransferase activity / tRNA methyltransferase activator activity / tRNA methyltransferase complex / tRNA modification in the nucleus and cytosol / tRNA modification / tRNA methylation / enzyme activator activity / 転移酵素; 一炭素原子の基を移すもの; メチル基を移すもの / chromosome / tRNA binding / DNA damage response / nucleolus / nucleoplasm / nucleus / cytosol 類似検索 - 分子機能 | ||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.53 Å | ||||||||||||
 データ登録者 データ登録者 | Ruiz-Arroyo VM / Nam Y | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2023 ジャーナル: Nature / 年: 2023タイトル: Structures and mechanisms of tRNA methylation by METTL1-WDR4. 著者: Victor M Ruiz-Arroyo / Rishi Raj / Kesavan Babu / Otgonbileg Onolbaatar / Paul H Roberts / Yunsun Nam /  要旨: Specific, regulated modification of RNAs is important for proper gene expression. tRNAs are rich with various chemical modifications that affect their stability and function. 7-Methylguanosine (mG) ...Specific, regulated modification of RNAs is important for proper gene expression. tRNAs are rich with various chemical modifications that affect their stability and function. 7-Methylguanosine (mG) at tRNA position 46 is a conserved modification that modulates steady-state tRNA levels to affect cell growth. The METTL1-WDR4 complex generates mG46 in humans, and dysregulation of METTL1-WDR4 has been linked to brain malformation and multiple cancers. Here we show how METTL1 and WDR4 cooperate to recognize RNA substrates and catalyse methylation. A crystal structure of METTL1-WDR4 and cryo-electron microscopy structures of METTL1-WDR4-tRNA show that the composite protein surface recognizes the tRNA elbow through shape complementarity. The cryo-electron microscopy structures of METTL1-WDR4-tRNA with S-adenosylmethionine or S-adenosylhomocysteine along with METTL1 crystal structures provide additional insights into the catalytic mechanism by revealing the active site in multiple states. The METTL1 N terminus couples cofactor binding with conformational changes in the tRNA, the catalytic loop and the WDR4 C terminus, acting as the switch to activate mG methylation. Thus, our structural models explain how post-translational modifications of the METTL1 N terminus can regulate methylation. Together, our work elucidates the core and regulatory mechanisms underlying mG modification by METTL1, providing the framework to understand its contribution to biology and disease. #1:  ジャーナル: To be published ジャーナル: To be publishedタイトル: CryoEM structure of human METTL1-WDR4 in complex with Lys-tRNA 著者: Ruiz-Arroyo VM / Nam Y | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_28108.map.gz emd_28108.map.gz | 5.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-28108-v30.xml emd-28108-v30.xml emd-28108.xml emd-28108.xml | 21.3 KB 21.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_28108_fsc.xml emd_28108_fsc.xml | 4.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_28108.png emd_28108.png | 111.7 KB | ||
| Filedesc metadata |  emd-28108.cif.gz emd-28108.cif.gz | 6.4 KB | ||
| その他 |  emd_28108_additional_1.map.gz emd_28108_additional_1.map.gz emd_28108_half_map_1.map.gz emd_28108_half_map_1.map.gz emd_28108_half_map_2.map.gz emd_28108_half_map_2.map.gz | 10.7 MB 10.6 MB 10.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-28108 http://ftp.pdbj.org/pub/emdb/structures/EMD-28108 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28108 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28108 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_28108_validation.pdf.gz emd_28108_validation.pdf.gz | 752.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_28108_full_validation.pdf.gz emd_28108_full_validation.pdf.gz | 752 KB | 表示 | |
| XML形式データ |  emd_28108_validation.xml.gz emd_28108_validation.xml.gz | 11.6 KB | 表示 | |
| CIF形式データ |  emd_28108_validation.cif.gz emd_28108_validation.cif.gz | 14.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28108 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28108 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28108 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28108 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_28108.map.gz / 形式: CCP4 / 大きさ: 11.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_28108.map.gz / 形式: CCP4 / 大きさ: 11.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH. Full map. | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.245 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: Human METTL1-WDR4 heterodimer in complex with Lys tRNA...
| ファイル | emd_28108_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH. Sharpen map. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Human METTL1-WDR4 heterodimer in complex with Lys tRNA...
| ファイル | emd_28108_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH. Half map. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH.
| ファイル | emd_28108_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Human METTL1-WDR4 heterodimer in complex with Lys tRNA and SAH. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human METTL1-WDR4 in complex with Lys-tRNA and SAH.
| 全体 | 名称: Human METTL1-WDR4 in complex with Lys-tRNA and SAH. |
|---|---|
| 要素 |
|
-超分子 #1: Human METTL1-WDR4 in complex with Lys-tRNA and SAH.
| 超分子 | 名称: Human METTL1-WDR4 in complex with Lys-tRNA and SAH. / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#3 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 112 KDa |
-分子 #1: tRNA (guanine-N(7)-)-methyltransferase non-catalytic subunit WDR4
| 分子 | 名称: tRNA (guanine-N(7)-)-methyltransferase non-catalytic subunit WDR4 タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 45.123023 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MHHHHHHENL YFQGSGMAGS VGLALCGQTL VVRGGSRFLA TSIASSDDDS LFIYDCSAAE KKSQENKGED APLDQGSGAI LASTFSKSG SYFALTDDSK RLILFRTKPW QCLSVRTVAR RCTALTFIAS EEKVLVADKS GDVYSFSVLE PHGCGRLELG H LSMLLDVA ...文字列: MHHHHHHENL YFQGSGMAGS VGLALCGQTL VVRGGSRFLA TSIASSDDDS LFIYDCSAAE KKSQENKGED APLDQGSGAI LASTFSKSG SYFALTDDSK RLILFRTKPW QCLSVRTVAR RCTALTFIAS EEKVLVADKS GDVYSFSVLE PHGCGRLELG H LSMLLDVA VSPDDRFILT ADRDEKIRVS WAAAPHSIES FCLGHTEFVS RISVVPTQPG LLLSSSGDGT LRLWEYRSGR QL HCCHLAS LQELVDPQAP QKFAASRIAF WCQENCVALL CDGTPVVYIF QLDARRQQLV YRQQLAFQHQ VWDVAFEETQ GLW VLQDCQ EAPLVLYRPV GDQWQSVPES TVLKKVSGVL RGNWAMLEGS AGADASFSSL YKATFDNVTS YLKKKEERLQ QQLE KKQRR UniProtKB: tRNA (guanine-N(7)-)-methyltransferase non-catalytic subunit WDR4 |
-分子 #2: tRNA (guanine-N(7)-)-methyltransferase
| 分子 | 名称: tRNA (guanine-N(7)-)-methyltransferase / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO / EC番号: tRNA (guanine46-N7)-methyltransferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 31.516012 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAAETRNVAG AEAPPPQKRY YRQRAHSNPM ADHTLRYPVK PEEMDWSELY PEFFAPLTQN QSHDDPKDKK EKRAQAQVEF ADIGCGYGG LLVELSPLFP DTLILGLEIR VKVSDYVQDR IRALRAAPAG GFQNIACLRS NAMKHLPNFF YKGQLTKMFF L FPDPHFKR ...文字列: MAAETRNVAG AEAPPPQKRY YRQRAHSNPM ADHTLRYPVK PEEMDWSELY PEFFAPLTQN QSHDDPKDKK EKRAQAQVEF ADIGCGYGG LLVELSPLFP DTLILGLEIR VKVSDYVQDR IRALRAAPAG GFQNIACLRS NAMKHLPNFF YKGQLTKMFF L FPDPHFKR TKHKWRIISP TLLAEYAYVL RVGGLVYTIT DVLELHDWMC THFEEHPLFE RVPLEDLSED PVVGHLGTST EE GKKVLRN GGKNFPAIFR RIQDPVLQAV TSQTSLPGH UniProtKB: tRNA (guanine-N(7)-)-methyltransferase |
-分子 #3: RNA (65-MER)
| 分子 | 名称: RNA (65-MER) / タイプ: rna / ID: 3 / コピー数: 1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 23.162705 KDa |
| 配列 | 文字列: GCCCGGAUAG CUCAGUCGGU AGAGCAUCAG ACUUUUAAUC UGAGGGUCCA GGGUUCAAGU CCCUGUUCGG GC GENBANK: GENBANK: MN296912.1 |
-分子 #4: S-ADENOSYL-L-HOMOCYSTEINE
| 分子 | 名称: S-ADENOSYL-L-HOMOCYSTEINE / タイプ: ligand / ID: 4 / コピー数: 1 / 式: SAH |
|---|---|
| 分子量 | 理論値: 384.411 Da |
| Chemical component information |  ChemComp-SAH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 375.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 62.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.2 µm 最小 デフォーカス(公称値): 0.7000000000000001 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z
Z Y
Y X
X


























