+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2179 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Electron cryo-microscopy of C. thermophilum RAC bound to the 80S ribosome | |||||||||
 マップデータ マップデータ | Reconstruction of the reconstituted complex of C. thermophilum RAC and C. thermophilum 80S ribosomes (Low-pass filtered between 18-20 A) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | ribosome-associated complex / RAC / ribosome / 80S / chaperone / co-translational folding | |||||||||
| 生物種 |  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 9.6 Å | |||||||||
 データ登録者 データ登録者 | Leidig C / Bange G / Kopp J / Amlacher S / Aravind A / Wickles S / Witte G / Hurt E / Beckmann R / Sinning I | |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2013 ジャーナル: Nat Struct Mol Biol / 年: 2013タイトル: Structural characterization of a eukaryotic chaperone--the ribosome-associated complex. 著者: Christoph Leidig / Gert Bange / Jürgen Kopp / Stefan Amlacher / Ajay Aravind / Stephan Wickles / Gregor Witte / Ed Hurt / Roland Beckmann / Irmgard Sinning /  要旨: Ribosome-associated chaperones act in early folding events during protein synthesis. Structural information is available for prokaryotic chaperones (such as trigger factor), but structural ...Ribosome-associated chaperones act in early folding events during protein synthesis. Structural information is available for prokaryotic chaperones (such as trigger factor), but structural understanding of these processes in eukaryotes lags far behind. Here we present structural analyses of the eukaryotic ribosome-associated complex (RAC) from Saccharomyces cerevisiae and Chaetomium thermophilum, consisting of heat-shock protein 70 (Hsp70) Ssz1 and the Hsp40 Zuo1. RAC is an elongated complex that crouches over the ribosomal tunnel exit and seems to be stabilized in a distinct conformation by expansion segment ES27. A unique α-helical domain in Zuo1 mediates ribosome interaction of RAC near the ribosomal proteins L22e and L31e and ribosomal RNA helix H59. The crystal structure of the Ssz1 ATPase domain bound to ATP-Mg²⁺ explains its catalytic inactivity and suggests that Ssz1 may act before the RAC-associated chaperone Ssb. Our study offers insights into the interplay between RAC, the ER membrane-integrated Hsp40-type protein ERj1 and the signal-recognition particle. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2179.map.gz emd_2179.map.gz | 3.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2179-v30.xml emd-2179-v30.xml emd-2179.xml emd-2179.xml | 9.8 KB 9.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_2179.png emd_2179.png | 117 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2179 http://ftp.pdbj.org/pub/emdb/structures/EMD-2179 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2179 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2179 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2179_validation.pdf.gz emd_2179_validation.pdf.gz | 224.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2179_full_validation.pdf.gz emd_2179_full_validation.pdf.gz | 223.6 KB | 表示 | |
| XML形式データ |  emd_2179_validation.xml.gz emd_2179_validation.xml.gz | 6.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2179 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2179 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2179 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2179 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2179.map.gz / 形式: CCP4 / 大きさ: 39.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2179.map.gz / 形式: CCP4 / 大きさ: 39.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of the reconstituted complex of C. thermophilum RAC and C. thermophilum 80S ribosomes (Low-pass filtered between 18-20 A) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.1 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
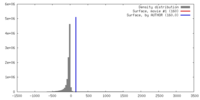
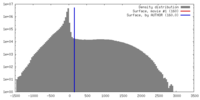
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Ribosome-associated complex (RAC) bound to 80S ribosome
| 全体 | 名称: Ribosome-associated complex (RAC) bound to 80S ribosome |
|---|---|
| 要素 |
|
-超分子 #1000: Ribosome-associated complex (RAC) bound to 80S ribosome
| 超分子 | 名称: Ribosome-associated complex (RAC) bound to 80S ribosome タイプ: sample / ID: 1000 詳細: Sample was reconstituted from the purified components 集合状態: One RAC binds to one ribosome / Number unique components: 2 |
|---|---|
| 分子量 | 理論値: 3.2 MDa |
-超分子 #1: 80S ribosome
| 超分子 | 名称: 80S ribosome / タイプ: complex / ID: 1 / 組換発現: No / Ribosome-details: ribosome-eukaryote: ALL |
|---|---|
| 由来(天然) | 生物種:  Chaetomium thermophilum (菌類) / 細胞中の位置: cytosol Chaetomium thermophilum (菌類) / 細胞中の位置: cytosol |
| 分子量 | 理論値: 3.1 MDa |
-分子 #1: Ribosome-associated complex
| 分子 | 名称: Ribosome-associated complex / タイプ: protein_or_peptide / ID: 1 / Name.synonym: RAC / 組換発現: No |
|---|---|
| 由来(天然) | 生物種:  Chaetomium thermophilum (菌類) / 細胞中の位置: cytosol Chaetomium thermophilum (菌類) / 細胞中の位置: cytosol |
| 分子量 | 理論値: 110 KDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7 詳細: 20 mM Tris-HCl, 100 mM KOAc, 100 mM sucrose, 7.5 mM Mg(OAc)2, 2 mM DTT |
|---|---|
| グリッド | 詳細: carbon supported |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / 装置: FEI VITROBOT MARK III / 手法: Blot for 3.5 s before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 詳細 | Final magnification of the object on the CCD image is 148721 |
| 日付 | 2011年7月6日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: TVIPS TEMCAM-F416 (4k x 4k) 実像数: 6954 / 平均電子線量: 20 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.7 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 75000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | Particles selected by signature. Refinement with spider. |
|---|---|
| CTF補正 | 詳細: Particle groups with similar defocus |
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 9.6 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: SPIDER 詳細: Sorting for ribosome conformation and ligand presence was performed 使用した粒子像数: 26038 |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)