+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2077 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Electron cryo-microscopy of microtubule-bound human kinesin-5 motor domain in AMPPNP state. | |||||||||
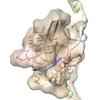
 マップデータ マップデータ | 3D reconstruction of microtubule-bound human kinesin-5 motor domain with AMPPNP bound in the nucleotide-binding site | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | cancer / electron cryo-microscopy / kinesin / microtubule / mitosis | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報spindle elongation / regulation of mitotic centrosome separation / plus-end-directed microtubule motor activity / Kinesins / mitotic centrosome separation / positive regulation of axon guidance / kinesin complex / microtubule motor activity / spindle organization / COPI-dependent Golgi-to-ER retrograde traffic ...spindle elongation / regulation of mitotic centrosome separation / plus-end-directed microtubule motor activity / Kinesins / mitotic centrosome separation / positive regulation of axon guidance / kinesin complex / microtubule motor activity / spindle organization / COPI-dependent Golgi-to-ER retrograde traffic / microtubule-based movement / mitotic spindle assembly / microtubule-based process / MHC class II antigen presentation / mitotic spindle organization / structural constituent of cytoskeleton / mitotic spindle / microtubule cytoskeleton organization / spindle pole / spindle / microtubule cytoskeleton / mitotic cell cycle / nervous system development / microtubule binding / 加水分解酵素; 酸無水物に作用; GTPに作用・細胞または細胞小器官の運動に関与 / microtubule / hydrolase activity / protein heterodimerization activity / cell division / GTPase activity / protein kinase binding / GTP binding / protein-containing complex / ATP binding / nucleus / membrane / metal ion binding / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 9.7 Å | |||||||||
 データ登録者 データ登録者 | Goulet A / Behnke-Parks WM / Sindelar C / Rosenfeld S / Moores C | |||||||||
 引用 引用 |  ジャーナル: J Biol Chem / 年: 2012 ジャーナル: J Biol Chem / 年: 2012タイトル: The structural basis of force generation by the mitotic motor kinesin-5. 著者: Adeline Goulet / William M Behnke-Parks / Charles V Sindelar / Jennifer Major / Steven S Rosenfeld / Carolyn A Moores /  要旨: Kinesin-5 is required for forming the bipolar spindle during mitosis. Its motor domain, which contains nucleotide and microtubule binding sites and mechanical elements to generate force, has evolved ...Kinesin-5 is required for forming the bipolar spindle during mitosis. Its motor domain, which contains nucleotide and microtubule binding sites and mechanical elements to generate force, has evolved distinct properties for its spindle-based functions. In this study, we report subnanometer resolution cryoelectron microscopy reconstructions of microtubule-bound human kinesin-5 before and after nucleotide binding and combine this information with studies of the kinetics of nucleotide-induced neck linker and cover strand movement. These studies reveal coupled, nucleotide-dependent conformational changes that explain many of this motor's properties. We find that ATP binding induces a ratchet-like docking of the neck linker and simultaneous, parallel docking of the N-terminal cover strand. Loop L5, the binding site for allosteric inhibitors of kinesin-5, also undergoes a dramatic reorientation when ATP binds, suggesting that it is directly involved in controlling nucleotide binding. Our structures indicate that allosteric inhibitors of human kinesin-5, which are being developed as anti-cancer therapeutics, bind to a motor conformation that occurs in the course of normal function. However, due to evolutionarily defined sequence variations in L5, this conformation is not adopted by invertebrate kinesin-5s, explaining their resistance to drug inhibition. Together, our data reveal the precision with which the molecular mechanism of kinesin-5 motors has evolved for force generation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2077.map.gz emd_2077.map.gz | 238.1 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2077-v30.xml emd-2077-v30.xml emd-2077.xml emd-2077.xml | 12.3 KB 12.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_2077.jpg emd_2077.jpg | 144.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2077 http://ftp.pdbj.org/pub/emdb/structures/EMD-2077 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2077 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2077 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2077_validation.pdf.gz emd_2077_validation.pdf.gz | 254.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2077_full_validation.pdf.gz emd_2077_full_validation.pdf.gz | 253.9 KB | 表示 | |
| XML形式データ |  emd_2077_validation.xml.gz emd_2077_validation.xml.gz | 4.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2077 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2077 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2077 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2077 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2077.map.gz / 形式: CCP4 / 大きさ: 348.6 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2077.map.gz / 形式: CCP4 / 大きさ: 348.6 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | 3D reconstruction of microtubule-bound human kinesin-5 motor domain with AMPPNP bound in the nucleotide-binding site | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.8 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : 13-protofilament microtubule-bound human kinesin-5 motor domain w...
| 全体 | 名称: 13-protofilament microtubule-bound human kinesin-5 motor domain with AMPPNP |
|---|---|
| 要素 |
|
-超分子 #1000: 13-protofilament microtubule-bound human kinesin-5 motor domain w...
| 超分子 | 名称: 13-protofilament microtubule-bound human kinesin-5 motor domain with AMPPNP タイプ: sample / ID: 1000 集合状態: 13-protofilament microtubule with one kineisn-5 motor domain bound every tubulin heterodimers Number unique components: 2 |
|---|
-分子 #1: alpha-beta tubulin dimer
| 分子 | 名称: alpha-beta tubulin dimer / タイプ: protein_or_peptide / ID: 1 / 集合状態: heterodimer / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #2: Kinesin-5 motor domain
| 分子 | 名称: Kinesin-5 motor domain / タイプ: protein_or_peptide / ID: 2 / 集合状態: monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: Human Homo sapiens (ヒト) / 別称: Human |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 6.8 / 詳細: 80 mM PIPES, 5 mM MgCl2, 1 mM EGTA, 5mM AMPPNP |
|---|---|
| グリッド | 詳細: 400 mesh holey carbon grids |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK I / 手法: chamber at 24 degrees C, blot 2.5 sec |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 温度 | 平均: 90 K |
| アライメント法 | Legacy - 非点収差: Objective lens astigmatism was corrected at 150,000 times magnification |
| 日付 | 2011年1月10日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 7 µm / 実像数: 46 / 平均電子線量: 18 e/Å2 / ビット/ピクセル: 8 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | The particles were selected along individual microtubules. |
|---|---|
| CTF補正 | 詳細: FREALIGN |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 9.7 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: SPIDER, FREALIGN 詳細: Approximately 50,000 asymmetric units were averaged in the final reconstruction. 使用した粒子像数: 3587 |
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A |
|---|---|
| ソフトウェア | 名称: Chimera, FlexEM |
| 詳細 | Protocol: rigid body then flexible fitting. The domain was fitted as a rigid body. The N-terminal residues 6 to 16 were built in the EM map and the final model was refined by flexible fitting. |
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT / 当てはまり具合の基準: cross-correlation |
| 得られたモデル |  PDB-4aqv: |
-原子モデル構築 2
| 初期モデル | PDB ID: Chain - #0 - Chain ID: A / Chain - #1 - Chain ID: B |
|---|---|
| ソフトウェア | 名称:  Chimera Chimera |
| 詳細 | Protocol: rigid body. alpha- and b-tubulin were separately fitted. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: cross-correlation |
| 得られたモデル |  PDB-4aqv: |
 ムービー
ムービー コントローラー
コントローラー


























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)























