+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0159 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Retromer-Vps5: map centred on the Vps5 layer under the Vps26 dimer. | |||||||||
 マップデータ マップデータ | Retromer-Vps5: map centred on the Vps5 layer under the Vps26 dimer. | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) | |||||||||
| 手法 | サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 8.9 Å | |||||||||
 データ登録者 データ登録者 | Kovtun O / Leneva N / Ariotti N / Teasdale RD / Owen DJ / Collins BM / Briggs JAG | |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2018 ジャーナル: Nature / 年: 2018タイトル: Structure of the membrane-assembled retromer coat determined by cryo-electron tomography. 著者: Oleksiy Kovtun / Natalya Leneva / Yury S Bykov / Nicholas Ariotti / Rohan D Teasdale / Miroslava Schaffer / Benjamin D Engel / David J Owen / John A G Briggs / Brett M Collins /    要旨: Eukaryotic cells traffic proteins and lipids between different compartments using protein-coated vesicles and tubules. The retromer complex is required to generate cargo-selective tubulovesicular ...Eukaryotic cells traffic proteins and lipids between different compartments using protein-coated vesicles and tubules. The retromer complex is required to generate cargo-selective tubulovesicular carriers from endosomal membranes. Conserved in eukaryotes, retromer controls the cellular localization and homeostasis of hundreds of transmembrane proteins, and its disruption is associated with major neurodegenerative disorders. How retromer is assembled and how it is recruited to form coated tubules is not known. Here we describe the structure of the retromer complex (Vps26-Vps29-Vps35) assembled on membrane tubules with the bin/amphiphysin/rvs-domain-containing sorting nexin protein Vps5, using cryo-electron tomography and subtomogram averaging. This reveals a membrane-associated Vps5 array, from which arches of retromer extend away from the membrane surface. Vps35 forms the 'legs' of these arches, and Vps29 resides at the apex where it is free to interact with regulatory factors. The bases of the arches connect to each other and to Vps5 through Vps26, and the presence of the same arches on coated tubules within cells confirms their functional importance. Vps5 binds to Vps26 at a position analogous to the previously described cargo- and Snx3-binding site, which suggests the existence of distinct retromer-sorting nexin assemblies. The structure provides insight into the architecture of the coat and its mechanism of assembly, and suggests that retromer promotes tubule formation by directing the distribution of sorting nexin proteins on the membrane surface while providing a scaffold for regulatory-protein interactions. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0159.map.gz emd_0159.map.gz | 20.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0159-v30.xml emd-0159-v30.xml emd-0159.xml emd-0159.xml | 13.6 KB 13.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_0159.png emd_0159.png | 45.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0159 http://ftp.pdbj.org/pub/emdb/structures/EMD-0159 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0159 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0159 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0159_validation.pdf.gz emd_0159_validation.pdf.gz | 238.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0159_full_validation.pdf.gz emd_0159_full_validation.pdf.gz | 237.9 KB | 表示 | |
| XML形式データ |  emd_0159_validation.xml.gz emd_0159_validation.xml.gz | 5.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0159 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0159 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0159 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0159 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0159.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0159.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Retromer-Vps5: map centred on the Vps5 layer under the Vps26 dimer. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.35 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
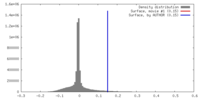
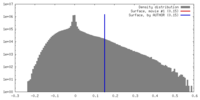
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Retromer-Vps5 complex assembled on the membrane.
| 全体 | 名称: Retromer-Vps5 complex assembled on the membrane. |
|---|---|
| 要素 |
|
-超分子 #1: Retromer-Vps5 complex assembled on the membrane.
| 超分子 | 名称: Retromer-Vps5 complex assembled on the membrane. / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Vps26/Vps35/Vps29 trimer recruited to the membrane via Vps5 PX-BAR protein. |
|---|---|
| 由来(天然) | 生物種:  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) |
| 組換発現 | 生物種:  |
-分子 #1: Vacuolar protein sorting-associated protein 5
| 分子 | 名称: Vacuolar protein sorting-associated protein 5 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 配列 | 文字列: MEDPWADTAS PNSSAPLSQH VEDSSSAPAA AAETPSNTAT TTAPSISTSS RPSRATPRRI VAKPKSLEAV EDDPLGPLGA PTPSSDSDNN GLGGATARGV QPPVPPLKEQ LPLRTTLPPS TTNRGGRGRR SGPPDPHHID DDDDDAALFG SAGRGRPPPP VPASLPSPVK ...文字列: MEDPWADTAS PNSSAPLSQH VEDSSSAPAA AAETPSNTAT TTAPSISTSS RPSRATPRRI VAKPKSLEAV EDDPLGPLGA PTPSSDSDNN GLGGATARGV QPPVPPLKEQ LPLRTTLPPS TTNRGGRGRR SGPPDPHHID DDDDDAALFG SAGRGRPPPP VPASLPSPVK SSTAPSMSVE QAARPTFHIT VGDPHKVGDL ATSHIVYSVR TKTTSKAYKQ PEFEVKRRYR DFLWLYNTLH SNNPGVVVPP PPEKQAVGRF ESNFVESRRA ALEKMLNKIA AHPTLQLDAD LKLFLESESF NIDVKHKERK EPPLGESKGV FGSLGFGGGG NKFVEQDDWF HDRRVYLDAL ENQLKALLKA MDNMVAQRKA MAEAAADFSA SLHALSTVEL SPTLSGPLDA LSELQLAIRD VYERQAQQDV LTFGIIIEEY IRLIGSVKQA FSQRQKAFHS WHSAESELMK KKAAQDKLLR QGKTQQDRLN QVNAEVIDAE RKVHQARLLF EDMGRLLRSE LDRFEREKVE DFKSGVETFL ESAVEAQKEL IEKWETFLMQ LDAEDDESVF YRPPPVQTKK PAGDTAVDRA RARIDEDSD |
-分子 #2: Vacuolar protein sorting-associated protein 26
| 分子 | 名称: Vacuolar protein sorting-associated protein 26 / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 配列 | 文字列: MSYFFSTPVD IDIVLADADK RAMVDVKLDK NRREKVPLYM DGESVKGCVT VRPKDGKRLE HTGIKVQFIG TIEMFFDRGN HYEFLSLVQE LAAPGELQHP QTFDFNFKNV EKQYESYNGI NVKLRYFVRV TVSRRMADVI REKDIWVYSY RIPPELNSSI KMDVGIEDCL ...文字列: MSYFFSTPVD IDIVLADADK RAMVDVKLDK NRREKVPLYM DGESVKGCVT VRPKDGKRLE HTGIKVQFIG TIEMFFDRGN HYEFLSLVQE LAAPGELQHP QTFDFNFKNV EKQYESYNGI NVKLRYFVRV TVSRRMADVI REKDIWVYSY RIPPELNSSI KMDVGIEDCL HIEFEYSKSK YHLKDVIVGR IYFLLVRLKI KHMELSIIRR ETTGVAPNQY NESETLVRFE IMDGSPSRGE TIPIRLFLGG FDLTPTFRDV NKKFSTRYYL SLVLIDEDAR RYFKQSEIIL YRQPPEYDNQ LLPPPPDQKQ VTAPLA |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | 3D array |
- 試料調製
試料調製
| 濃度 | 1.1 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 292 K / 装置: LEICA EM GP | |||||||||
| 詳細 | The solution-assembled complex was incubated with Folch liposomes at room temperature. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: SUPER-RESOLUTION / 撮影したグリッド数: 2 / 平均電子線量: 3.17 e/Å2 詳細: Tomographic tilt series were acquired with the dose-symmetric tilt-scheme (Hagen et al., J Struct Biol. 2017) |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 6.5 µm / 最小 デフォーカス(公称値): 2.5 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)