+検索条件
-Structure paper
| タイトル | Anaerobic cryoEM protocols for air-sensitive nitrogenase proteins. |
|---|---|
| ジャーナル・号・ページ | Nat Protoc, Vol. 19, Issue 7, Page 2026-2051, Year 2024 |
| 掲載日 | 2024年4月4日 |
 著者 著者 | Rebeccah A Warmack / Belinda B Wenke / Thomas Spatzal / Douglas C Rees /  |
| PubMed 要旨 | Single-particle cryo-electron microscopy (cryoEM) provides an attractive avenue for advancing our atomic resolution understanding of materials, molecules and living systems. However, the vast ...Single-particle cryo-electron microscopy (cryoEM) provides an attractive avenue for advancing our atomic resolution understanding of materials, molecules and living systems. However, the vast majority of published cryoEM methodologies focus on the characterization of aerobically purified samples. Air-sensitive enzymes and microorganisms represent important yet understudied systems in structural biology. We have recently demonstrated the success of an anaerobic single-particle cryoEM workflow applied to the air-sensitive nitrogenase enzymes. In this protocol, we detail the use of Schlenk lines and anaerobic chambers to prepare samples, including a protein tag for monitoring sample exposure to oxygen in air. We describe how to use a plunge freezing apparatus inside of a soft-sided vinyl chamber of the type we routinely use for anaerobic biochemistry and crystallography of oxygen-sensitive proteins. Manual control of the airlock allows for introduction of liquid cryogens into the tent. A custom vacuum port provides slow, continuous evacuation of the tent atmosphere to avoid accumulation of flammable vapors within the enclosed chamber. These methods allowed us to obtain high-resolution structures of both nitrogenase proteins using single-particle cryoEM. The procedures involved can be generally subdivided into a 4 d anaerobic sample generation procedure, and a 1 d anaerobic cryoEM sample preparation step, followed by conventional cryoEM imaging and processing steps. As nitrogen is a substrate for nitrogenase, the Schlenk lines and anaerobic chambers described in this procedure are operated under an argon atmosphere; however, the system and these procedures are compatible with other controlled gas environments. |
 リンク リンク |  Nat Protoc / Nat Protoc /  PubMed:38575747 PubMed:38575747 |
| 手法 | EM (単粒子) |
| 解像度 | 2.12 - 2.57 Å |
| 構造データ | EMDB-27317, PDB-8dby: EMDB-27404, PDB-8dfc: EMDB-27405, PDB-8dfd: EMDB-41151, PDB-8tc3: |
| 化合物 | 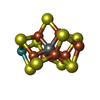 ChemComp-ICS: 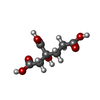 ChemComp-HCA:  ChemComp-FE: 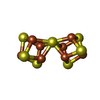 ChemComp-CLF:  ChemComp-HOH:  ChemComp-SF4:  ChemComp-ADP: 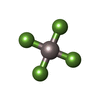 ChemComp-ALF:  ChemComp-MG: |
| 由来 |
|
 キーワード キーワード | METAL BINDING PROTEIN / OXIDOREDUCTASE / Nitrogenase / metalloenzyme / ATPase / metalloprotein / iron-sulfur |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について











 azotobacter vinelandii (窒素固定)
azotobacter vinelandii (窒素固定) discosoma sp. lw-2004 (イソギンチャク)
discosoma sp. lw-2004 (イソギンチャク)