+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 3iy1 | ||||||
|---|---|---|---|---|---|---|---|
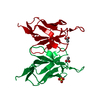
| タイトル | Variable domains of the WAM of Fab B fitted into the cryoEM reconstruction of the virus-Fab B complex | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | IMMUNE SYSTEM / cryoEM / neutralizing antibody / parvovirus / canine / feline / fab footprint | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 18 Å | ||||||
 データ登録者 データ登録者 | Hafenstein, S. / Bowman, V.D. / Sun, T. / Nelson, C.D. / Palermo, L.M. / Battisti, A.J. / Parrish, C.R. / Rossmann, M.G. | ||||||
 引用 引用 |  ジャーナル: J Virol / 年: 2009 ジャーナル: J Virol / 年: 2009タイトル: Structural comparison of different antibodies interacting with parvovirus capsids. 著者: Susan Hafenstein / Valorie D Bowman / Tao Sun / Christian D S Nelson / Laura M Palermo / Paul R Chipman / Anthony J Battisti / Colin R Parrish / Michael G Rossmann /  要旨: The structures of canine parvovirus (CPV) and feline parvovirus (FPV) complexed with antibody fragments from eight different neutralizing monoclonal antibodies were determined by cryo-electron ...The structures of canine parvovirus (CPV) and feline parvovirus (FPV) complexed with antibody fragments from eight different neutralizing monoclonal antibodies were determined by cryo-electron microscopy (cryoEM) reconstruction to resolutions varying from 8.5 to 18 A. The crystal structure of one of the Fab molecules and the sequence of the variable domain for each of the Fab molecules have been determined. The structures of Fab fragments not determined crystallographically were predicted by homology modeling according to the amino acid sequence. Fitting of the Fab and virus structures into the cryoEM densities identified the footprints of each antibody on the viral surface. As anticipated from earlier analyses, the Fab binding sites are directed to two epitopes, A and B. The A site is on an exposed part of the surface near an icosahedral threefold axis, whereas the B site is about equidistant from the surrounding five-, three-, and twofold axes. One antibody directed to the A site binds CPV but not FPV. Two of the antibodies directed to the B site neutralize the virus as Fab fragments. The differences in antibody properties have been linked to the amino acids within the antibody footprints, the position of the binding site relative to the icosahedral symmetry elements, and the orientation of the Fab structure relative to the surface of the virus. Most of the exposed surface area was antigenic, although each of the antibodies had a common area of overlap that coincided with the positions of the previously mapped escape mutations. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  3iy1.cif.gz 3iy1.cif.gz | 54.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb3iy1.ent.gz pdb3iy1.ent.gz | 38.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  3iy1.json.gz 3iy1.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  3iy1_validation.pdf.gz 3iy1_validation.pdf.gz | 649.6 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  3iy1_full_validation.pdf.gz 3iy1_full_validation.pdf.gz | 676.3 KB | 表示 | |
| XML形式データ |  3iy1_validation.xml.gz 3iy1_validation.xml.gz | 18.7 KB | 表示 | |
| CIF形式データ |  3iy1_validation.cif.gz 3iy1_validation.cif.gz | 25 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/iy/3iy1 https://data.pdbj.org/pub/pdb/validation_reports/iy/3iy1 ftp://data.pdbj.org/pub/pdb/validation_reports/iy/3iy1 ftp://data.pdbj.org/pub/pdb/validation_reports/iy/3iy1 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  5106MC  5105C  5107C  5108C  5109C  5110C  5111C  5112C  3gk8C  3iy0C  3iy2C  3iy3C  3iy4C  3iy5C  3iy6C  3iy7C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: 抗体 | 分子量: 11643.067 Da / 分子数: 1 / 断片: antibody B fragment / 由来タイプ: 天然 / 由来: (天然)  |
|---|---|
| #2: 抗体 | 分子量: 11773.996 Da / 分子数: 1 / 由来タイプ: 天然 / 由来: (天然)  |
| Has protein modification | Y |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ウイルスについての詳細 | 中空か: NO / エンベロープを持つか: NO / ホストのカテゴリ: VERTEBRATES / 単離: STRAIN / タイプ: VIRION | |||||||||||||||
| 天然宿主 | 生物種: Felis catus | |||||||||||||||
| ウイルス殻 | 三角数 (T数): 1 | |||||||||||||||
| 緩衝液 | pH: 7.5 / 詳細: 10mM Tris | |||||||||||||||
| 試料 | 濃度: 1 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES / 詳細: 10mM Tris | |||||||||||||||
| 急速凍結 | 装置: HOMEMADE PLUNGER / 凍結剤: ETHANE / Temp: 120 K / 手法: blot before plunging |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 顕微鏡 | モデル: FEI/PHILIPS CM300FEG/T / 日付: 2004年6月30日 |
|---|---|
| 電子銃 | 電子線源: TUNGSTEN HAIRPIN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 45000 X / 倍率(補正後): 47190 X / 最大 デフォーカス(公称値): 3.7 nm / 最小 デフォーカス(公称値): 1.7 nm / カメラ長: 0 mm |
| 試料ホルダ | 試料ホルダーモデル: GATAN LIQUID NITROGEN / 資料ホルダタイプ: side mounted nitrogen cooled / 温度: 93 K / 最高温度: 83 K / 最低温度: 83 K / 傾斜角・最大: 0 ° / 傾斜角・最小: 0 ° |
| 撮影 | 電子線照射量: 28.4 e/Å2 / フィルム・検出器のモデル: KODAK SO-163 FILM |
| 画像スキャン | サンプリングサイズ: 7 µm / 詳細: scanned at 7 microns and bin averaged to 14 / デジタル画像の数: 56 / Od range: 0.9 / Scanner model: ZEISS SCAI |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M |
| 放射波長 | 相対比: 1 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | 詳細: robem | ||||||||||||
| 対称性 | 点対称性: I (正20面体型対称) | ||||||||||||
| 3次元再構成 | 手法: common lines / 解像度: 18 Å / 解像度の算出法: FSC 0.5 CUT-OFF / 粒子像の数: 1126 / 対称性のタイプ: POINT | ||||||||||||
| 精密化ステップ | サイクル: LAST
|
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera








 PDBj
PDBj



