+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1fst | ||||||
|---|---|---|---|---|---|---|---|
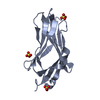
| タイトル | CRYSTAL STRUCTURE OF TRUNCATED HUMAN RHOGDI TRIPLE MUTANT | ||||||
 要素 要素 | RHO GDP-DISSOCIATION INHIBITOR 1 | ||||||
 キーワード キーワード |  SIGNALING PROTEIN INHIBITOR / immunoglobulin fold / beta sandwich motif / isoprenyl-binding domain / GDP-dissociation inhibitor of Rho GTPases SIGNALING PROTEIN INHIBITOR / immunoglobulin fold / beta sandwich motif / isoprenyl-binding domain / GDP-dissociation inhibitor of Rho GTPases | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Rho GDP-dissociation inhibitor activity / regulation of synaptic vesicle cycle / Axonal growth inhibition (RHOA activation) / Axonal growth stimulation / regulation of Rho protein signal transduction / RHOC GTPase cycle / RHOH GTPase cycle / semaphorin-plexin signaling pathway / CDC42 GTPase cycle / Rho protein signal transduction ...Rho GDP-dissociation inhibitor activity / regulation of synaptic vesicle cycle / Axonal growth inhibition (RHOA activation) / Axonal growth stimulation / regulation of Rho protein signal transduction / RHOC GTPase cycle / RHOH GTPase cycle / semaphorin-plexin signaling pathway / CDC42 GTPase cycle / Rho protein signal transduction /  免疫シナプス / RHOG GTPase cycle / RHOA GTPase cycle / RAC2 GTPase cycle / RAC1 GTPase cycle / 免疫シナプス / RHOG GTPase cycle / RHOA GTPase cycle / RAC2 GTPase cycle / RAC1 GTPase cycle /  GTPase activator activity / Schaffer collateral - CA1 synapse / GTPase activator activity / Schaffer collateral - CA1 synapse /  regulation of protein localization / regulation of protein localization /  細胞骨格 / negative regulation of apoptotic process / extracellular exosome / 細胞骨格 / negative regulation of apoptotic process / extracellular exosome /  生体膜 / 生体膜 /  細胞核 / 細胞核 /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / 解像度: 2.7 Å シンクロトロン / 解像度: 2.7 Å | ||||||
 データ登録者 データ登録者 | Longenecker, K.L. / Garrard, S.M. / Sheffield, P.J. / Derewenda, Z.S. | ||||||
 引用 引用 |  ジャーナル: Acta Crystallogr.,Sect.D / 年: 2001 ジャーナル: Acta Crystallogr.,Sect.D / 年: 2001タイトル: Protein crystallization by rational mutagenesis of surface residues: Lys to Ala mutations promote crystallization of RhoGDI. 著者: Longenecker, K.L. / Garrard, S.M. / Sheffield, P.J. / Derewenda, Z.S. #1:  ジャーナル: Structure / 年: 1997 ジャーナル: Structure / 年: 1997タイトル: A modulator of rho family G proteins, rhoGDI, binds these G proteins via an immunoglobulin-like domain and a flexible N-terminal arm 著者: Keep, N.H. / Barnes, M. / Barsukov, I. / Badii, R. / Lian, L. / Segal, A.W. / Moody, P.C. / Roberts, G.C. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1fst.cif.gz 1fst.cif.gz | 69.4 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1fst.ent.gz pdb1fst.ent.gz | 52 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1fst.json.gz 1fst.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/fs/1fst https://data.pdbj.org/pub/pdb/validation_reports/fs/1fst ftp://data.pdbj.org/pub/pdb/validation_reports/fs/1fst ftp://data.pdbj.org/pub/pdb/validation_reports/fs/1fst | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 単位格子 |
| ||||||||
| 詳細 | The asymmetric unit consists of two monomers. The monomer is the biologically active species. |
- 要素
要素
| #1: タンパク質 | 分子量: 20628.340 Da / 分子数: 2 / 断片: C-TERMINAL DOMAIN / 変異: K135A, K138A, K141A / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / プラスミド: PGEX / 発現宿主: Homo sapiens (ヒト) / プラスミド: PGEX / 発現宿主:   Escherichia coli (大腸菌) / 参照: UniProt: P52565 Escherichia coli (大腸菌) / 参照: UniProt: P52565#2: 水 | ChemComp-HOH / |  水 水 |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 3.02 Å3/Da / 溶媒含有率: 59.29 % | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
結晶化 | 温度: 293 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7 詳細: PEG 3400, isopropanol, HEPES buffer, pH 7.0, VAPOR DIFFUSION, HANGING DROP, temperature 293.0K | |||||||||||||||||||||||||
| 結晶化 | *PLUS 手法: 蒸気拡散法 | |||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  EMBL/DESY, HAMBURG EMBL/DESY, HAMBURG  / ビームライン: X11 / 波長: 0.9091 / ビームライン: X11 / 波長: 0.9091 |
| 検出器 | タイプ: MAR CCD 165 mm / 検出器: CCD / 日付: 1999年12月6日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 0.9091 Å / 相対比: 1 : 0.9091 Å / 相対比: 1 |
| 反射 | 解像度: 2.7→20 Å / Num. all: 13241 / Num. obs: 13241 / % possible obs: 99.6 % / Observed criterion σ(F): 0 / Observed criterion σ(I): 0 / 冗長度: 3.8 % / Biso Wilson estimate: 73 Å2 / Rmerge(I) obs: 0.048 / Net I/σ(I): 17.9 |
| 反射 シェル | 解像度: 2.7→2.78 Å / 冗長度: 3.8 % / Rmerge(I) obs: 0.267 / Num. unique all: 1129 / % possible all: 99.6 |
| 反射 | *PLUS Num. measured all: 49713 |
| 反射 シェル | *PLUS % possible obs: 99.6 % / Mean I/σ(I) obs: 3.7 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 解像度: 2.7→20 Å / σ(F): 0 / σ(I): 0 / 立体化学のターゲット値: Engh and Huber
| |||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.7→20 Å
| |||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称: CNS / バージョン: 0.9 / 分類: refinement | |||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj





