+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-7477 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cdc48 in the presence of ADP | |||||||||
 マップデータ マップデータ | Cdc48-Npl4 complex in the presence of ATP-gamma-S | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) | |||||||||
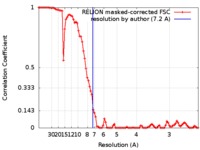
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.2 Å | |||||||||
 データ登録者 データ登録者 | Kim KH / Bodnar NO | |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2018 ジャーナル: Nat Struct Mol Biol / 年: 2018タイトル: Structure of the Cdc48 ATPase with its ubiquitin-binding cofactor Ufd1-Npl4. 著者: Nicholas O Bodnar / Kelly H Kim / Zhejian Ji / Thomas E Wales / Vladimir Svetlov / Evgeny Nudler / John R Engen / Thomas Walz / Tom A Rapoport /  要旨: Many polyubiquitinated proteins are extracted from membranes or complexes by the conserved ATPase Cdc48 (in yeast; p97 or VCP in mammals) before proteasomal degradation. Each Cdc48 hexamer contains ...Many polyubiquitinated proteins are extracted from membranes or complexes by the conserved ATPase Cdc48 (in yeast; p97 or VCP in mammals) before proteasomal degradation. Each Cdc48 hexamer contains two stacked ATPase rings (D1 and D2) and six N-terminal (N) domains. Cdc48 binds various cofactors, including the Ufd1-Npl4 heterodimer. Here, we report structures of the Cdc48-Ufd1-Npl4 complex from Chaetomium thermophilum. Npl4 interacts through its UBX-like domain with a Cdc48 N domain, and it uses two Zn-finger domains to anchor the enzymatically inactive Mpr1-Pad1 N-terminal (MPN) domain, homologous to domains found in several isopeptidases, to the top of the D1 ATPase ring. The MPN domain of Npl4 is located above Cdc48's central pore, a position similar to the MPN domain from deubiquitinase Rpn11 in the proteasome. Our results indicate that Npl4 is unique among Cdc48 cofactors and suggest a mechanism for binding and translocation of polyubiquitinated substrates into the ATPase. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_7477.map.gz emd_7477.map.gz | 4.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-7477-v30.xml emd-7477-v30.xml emd-7477.xml emd-7477.xml | 12.9 KB 12.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_7477_fsc.xml emd_7477_fsc.xml | 8.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_7477.png emd_7477.png | 95.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-7477 http://ftp.pdbj.org/pub/emdb/structures/EMD-7477 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7477 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7477 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_7477_validation.pdf.gz emd_7477_validation.pdf.gz | 78.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_7477_full_validation.pdf.gz emd_7477_full_validation.pdf.gz | 77.3 KB | 表示 | |
| XML形式データ |  emd_7477_validation.xml.gz emd_7477_validation.xml.gz | 493 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7477 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7477 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7477 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-7477 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_7477.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_7477.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Cdc48-Npl4 complex in the presence of ATP-gamma-S | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.24 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Cdc48
| 全体 | 名称: Cdc48 |
|---|---|
| 要素 |
|
-超分子 #1: Cdc48
| 超分子 | 名称: Cdc48 / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) |
| 組換発現 | 生物種:  |
-分子 #1: Cdc48
| 分子 | 名称: Cdc48 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Chaetomium thermophilum (菌類) Chaetomium thermophilum (菌類) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAPESKDHKK KVNLTDPSGA EHREENDTAT AILKKKKKPN QLMVTDAVND DNSIIALSNN TMEALQLFRG DTVLVRGKKR RDTVLIVLAD DDLDDGSARI NRVVRHNLRV KHGDMITIHP CPDIKYAKRI AVLPIADTVE GLTGSLFDVF LAPYFREAYR PVRQGDLFTV ...文字列: MAPESKDHKK KVNLTDPSGA EHREENDTAT AILKKKKKPN QLMVTDAVND DNSIIALSNN TMEALQLFRG DTVLVRGKKR RDTVLIVLAD DDLDDGSARI NRVVRHNLRV KHGDMITIHP CPDIKYAKRI AVLPIADTVE GLTGSLFDVF LAPYFREAYR PVRQGDLFTV RGGMRQVEFK VVEVDPPEYG IVAQDTIIHC EGEPIPREEE ENNLNEVGYD DIGGCRKQLA QIREMVELPL RHPQLFKSIG IKPPRGVLLY GPPGTGKTLM ARAVANETGA FFFLINGPEI MSKMAGESES NLRKAFEEAE KNSPAIIFID EIDSIAPKRE KTNGEVERRV VSQLLTLMDG MKARSNVVVM AATNRPNSID PALRRFGRFD REVDIGIPDP TGRLEILQIH TKNMKLADDV DLEQIAAETH GYVGSDLAAL CSEAAMQQIR EKMDLIDLDE DTIDAEVLDS LGVTMDNFRY ALGVSNPSAL REVAVVEVPN VRWEDIGGLE QVKQELKEQV QYPVDHPEKF LKFGLSPSRG VLFYGPPGTG KTMLAKAVAN ECAANFISVK GPELLSMWFG ESESNIRDIF DKARAAAPCV VFLDELDSIA KARGGSIGDA GGASDRVVNQ LLTEMDGMTS KKNVFVIGAT NRPEQLDPAL CRPGRLDQLI YVPLPDEAGR LSILKAQLRK TPVSKDVDLA YIASKTHGFS GADLAFITQR AVKLAIKESI AAEIERQKAR EAAGEDVNME DDEDPVPELT KRHFEEAMRD ARRSVSDVEI RRYEAFAQQM KNAGPGAFFK FPDSTTDNSA SNAAGNSFGD AGNDDDLYT |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / 前処理 - タイプ: GLOW DISCHARGE | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 80 % / 装置: GATAN CRYOPLUNGE 3 |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 実像数: 1628 / 平均露光時間: 6.0 sec. / 平均電子線量: 1.04 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.6 µm / 倍率(公称値): 31000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー