+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2286 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | 3D map of another peptide conjugated antibody particle by individual-particle electron tomography (IPET) and optimized negative-staining. | |||||||||
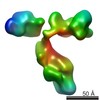
 マップデータ マップデータ | Reconstruction of another IgG1 antibody by Individual-Particle Electron Microscopy (IPET). | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | peptide conjugated human IgG1 antibody | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 電子線トモグラフィー法 / ネガティブ染色法 / 解像度: 16.6 Å | |||||||||
 データ登録者 データ登録者 | Tong H / Zhang L / Kaspar A / Rames M / Huang L / Woodnutt G / Ren G | |||||||||
 引用 引用 |  ジャーナル: Sci Rep / 年: 2013 ジャーナル: Sci Rep / 年: 2013タイトル: Peptide-conjugation induced conformational changes in human IgG1 observed by optimized negative-staining and individual-particle electron tomography. 著者: Huimin Tong / Lei Zhang / Allan Kaspar / Matthew J Rames / Liqing Huang / Gary Woodnutt / Gang Ren /  要旨: Peptides show much promise as potent and selective drug candidates. Fusing peptides to a scaffold monoclonal antibody produces a conjugated antibody which has the advantages of peptide activity yet ...Peptides show much promise as potent and selective drug candidates. Fusing peptides to a scaffold monoclonal antibody produces a conjugated antibody which has the advantages of peptide activity yet also has the pharmacokinetics determined by the scaffold antibody. However, the conjugated antibody often has poor binding affinity to antigens that may be related to unknown structural changes. The study of the conformational change is difficult by conventional techniques because structural fluctuation under equilibrium results in multiple structures co-existing. Here, we employed our two recently developed electron microscopy (EM) techniques: optimized negative-staining (OpNS) EM and individual-particle electron tomography (IPET). Two-dimensional (2D) image analyses and three-dimensional (3D) maps have shown that the domains of antibodies present an elongated peptide-conjugated conformational change, suggesting that our EM techniques may be novel tools to monitor the structural conformation changes in heterogeneous and dynamic macromolecules, such as drug delivery vehicles after pharmacological synthesis and development. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2286.map.gz emd_2286.map.gz | 17.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2286-v30.xml emd-2286-v30.xml emd-2286.xml emd-2286.xml | 13.7 KB 13.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  EMD-2286.tif EMD-2286.tif | 145.3 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2286 http://ftp.pdbj.org/pub/emdb/structures/EMD-2286 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2286 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2286 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2286_validation.pdf.gz emd_2286_validation.pdf.gz | 125.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2286_full_validation.pdf.gz emd_2286_full_validation.pdf.gz | 124.6 KB | 表示 | |
| XML形式データ |  emd_2286_validation.xml.gz emd_2286_validation.xml.gz | 6.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2286 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2286 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2286 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2286 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2286.map.gz / 形式: CCP4 / 大きさ: 29.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2286.map.gz / 形式: CCP4 / 大きさ: 29.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of another IgG1 antibody by Individual-Particle Electron Microscopy (IPET). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.406 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Peptide-conjugated Human IgG1 Antibody
| 全体 | 名称: Peptide-conjugated Human IgG1 Antibody |
|---|---|
| 要素 |
|
-超分子 #1000: Peptide-conjugated Human IgG1 Antibody
| 超分子 | 名称: Peptide-conjugated Human IgG1 Antibody / タイプ: sample / ID: 1000 詳細: The sample was thawed from storage at -80 degrees Celcius before being loaded onto the grid 集合状態: Monomer / Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 160 KDa / 理論値: 160 KDa |
-分子 #1: IgG Antibody
| 分子 | 名称: IgG Antibody / タイプ: protein_or_peptide / ID: 1 / Name.synonym: IgG / コピー数: 1 / 集合状態: Monomer / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: Plasma Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: Plasma |
| 分子量 | 実験値: 160 KDa / 理論値: 160 KDa |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 電子線トモグラフィー法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.01 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 詳細: 1X Dulbeccos phosphate-buffered saline (Invitrogen, La Jolla, CA), 2.7 mM KCl, 1.46 mM KH2PO4, 136.9 mM NaCl, and 8.1 mM Na2HPO4 |
| 染色 | タイプ: NEGATIVE 詳細: EM Specimens were prepared by optimized negative-staining EM specimen preparation protocol as described Zhang L. and Ren G, Journal of Lipid Research, (2010) 51, 1228-1236; (2011) 52, 175-84 ...詳細: EM Specimens were prepared by optimized negative-staining EM specimen preparation protocol as described Zhang L. and Ren G, Journal of Lipid Research, (2010) 51, 1228-1236; (2011) 52, 175-84 and BBA (2013) 1830, 2150-9. In brief, antibody was diluted to 0.01 mg/ml with deionized water. Aliquots (about 3ul) were applied to the 200 mesh glow-discharged thin carbon-coated EM grids (Cu-200CN, Pacific Grid-Tech, USA). The grid was washed by deionized water for three times, and then washed by 1% uranyl formate for three times before blotting to drying. |
| グリッド | 詳細: 200 mesh glow-discharged thin carbon-coated EM grids (Cu-200CN, Pacific Grid-Tech, USA) |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法 #1
電子顕微鏡法 #1
| Microscopy ID | 1 |
|---|---|
| 顕微鏡 | ZEISS LIBRA120PLUS |
| 詳細 | tilt step is 1.5 degree |
| 日付 | 2012年5月1日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) デジタル化 - サンプリング間隔: 1.406 µm / 実像数: 95 / 平均電子線量: 250 e/Å2 / ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 120 kV / 電子線源: LAB6 |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.2 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 80000 |
| 試料ステージ | 試料ホルダー: Gatan / 試料ホルダーモデル: OTHER / Tilt series - Axis1 - Min angle: -70.5 ° / Tilt series - Axis1 - Max angle: 70.5 ° / Tilt series - Axis1 - Angle increment: 1.5 ° |
- 電子顕微鏡法 #2
電子顕微鏡法 #2
| Microscopy ID | 2 |
|---|---|
| 顕微鏡 | FEI TECNAI 20 |
| 詳細 | tilt step is 1.5 degree |
| 日付 | 2009年10月1日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) デジタル化 - サンプリング間隔: 1.406 µm / 実像数: 95 / 平均電子線量: 250 e/Å2 / ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 200 kV / 電子線源: LAB6 |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 80000 |
| 試料ステージ | 試料ホルダー: Gatan / 試料ホルダーモデル: OTHER / Tilt series - Axis1 - Min angle: -70.5 ° / Tilt series - Axis1 - Max angle: 70.5 ° / Tilt series - Axis1 - Angle increment: 1.5 ° |
- 画像解析
画像解析
| 詳細 | Reconstruction was done by Individual-Particle Tomography Reconstruction (IPET) method.{eulerAnglesDetails}: Tomography tilt angle from -70.5 to 70.5 in step of 1.5 |
|---|---|
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 16.6 Å / 解像度の算出法: OTHER ソフトウェア - 名称: Individual-partcile, electron, tomogrphy, (IPET), and, FETR 詳細: Map was reconstructed by individual-particle electron tomography (IPET)and Focus ET Reconstruction Algorithm. 使用した粒子像数: 95 |
| CTF補正 | 詳細: TOMOCTF |
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称: Manual |
| 詳細 | Manually fit each domain into the density map in order to compare the conformational different between the peptide-conjugated antibody structure and PDB structure in term of domain size and shape. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera