+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 9fmg | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
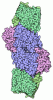
| タイトル | Methylthio-alkane reductase complex | ||||||||||||||||||||||||
 要素 要素 |
| ||||||||||||||||||||||||
 キーワード キーワード | OXIDOREDUCTASE / Methylthioethanol / dimethyl sulfide / ethylmethyl sulfide / methanethiol / ethylene / methane / ethane / metalloenzyme | ||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Oxidoreductases; Acting on iron-sulfur proteins as donors / nitrogenase activity / 4 iron, 4 sulfur cluster binding / ATP binding / metal ion binding 類似検索 - 分子機能 | ||||||||||||||||||||||||
| 生物種 |  Rhodospirillum rubrum (バクテリア) Rhodospirillum rubrum (バクテリア) | ||||||||||||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.71 Å | ||||||||||||||||||||||||
 データ登録者 データ登録者 | Lago-Maciel, A. / Zarzycki, J. / Prinz, S. / Reif-Trauttmansdorff, T. / Rebelein, J.G. | ||||||||||||||||||||||||
| 資金援助 |  ドイツ, 3件 ドイツ, 3件
| ||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Catal / 年: 2025 ジャーナル: Nat Catal / 年: 2025タイトル: Methylthio-alkane reductases use nitrogenase metalloclusters for carbon-sulfur bond cleavage. 著者: Ana Lago-Maciel / Jéssica C Soares / Jan Zarzycki / Charles J Buchanan / Tristan Reif-Trauttmansdorff / Frederik V Schmidt / Stefano Lometto / Nicole Paczia / Jan M Schuller / D Flemming ...著者: Ana Lago-Maciel / Jéssica C Soares / Jan Zarzycki / Charles J Buchanan / Tristan Reif-Trauttmansdorff / Frederik V Schmidt / Stefano Lometto / Nicole Paczia / Jan M Schuller / D Flemming Hansen / Gabriella T Heller / Simone Prinz / Georg K A Hochberg / Antonio J Pierik / Johannes G Rebelein /   要旨: Methylthio-alkane reductases convert methylated sulfur compounds to methanethiol and small hydrocarbons, a process with important environmental and biotechnological implications. These enzymes are ...Methylthio-alkane reductases convert methylated sulfur compounds to methanethiol and small hydrocarbons, a process with important environmental and biotechnological implications. These enzymes are classified as nitrogenase-like enzymes, despite lacking the ability to convert dinitrogen to ammonia, raising fundamental questions about the factors controlling their activity and specificity. Here we present the molecular structure of the methylthio-alkane reductase, which reveals large metalloclusters, including the P-cluster and the [FeSC]-cluster, previously found only in nitrogenases. Our findings suggest that distinct metallocluster coordination, surroundings and substrate channels determine the activity of these related metalloenzymes. This study provides new insights into nitrogen fixation, sulfur-compound reduction and hydrocarbon production. We also shed light on the evolutionary history of P-cluster and [FeSC]-cluster-containing reductases emerging before nitrogenases. | ||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  9fmg.cif.gz 9fmg.cif.gz | 351.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb9fmg.ent.gz pdb9fmg.ent.gz | 279 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  9fmg.json.gz 9fmg.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/fm/9fmg https://data.pdbj.org/pub/pdb/validation_reports/fm/9fmg ftp://data.pdbj.org/pub/pdb/validation_reports/fm/9fmg ftp://data.pdbj.org/pub/pdb/validation_reports/fm/9fmg | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  50553MC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-タンパク質 , 3種, 5分子 ABCDE
| #1: タンパク質 | 分子量: 57560.164 Da / 分子数: 1 / 由来タイプ: 組換発現 由来: (組換発現)  Rhodospirillum rubrum (バクテリア) Rhodospirillum rubrum (バクテリア)遺伝子: Rru_A0794 / 発現宿主:  Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW97, nitrogenase Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW97, nitrogenase | ||
|---|---|---|---|
| #2: タンパク質 | 分子量: 50856.289 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  Rhodospirillum rubrum (バクテリア) Rhodospirillum rubrum (バクテリア)遺伝子: Rru_A0793 / 発現宿主:  Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW98, nitrogenase Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW98, nitrogenase#3: タンパク質 | 分子量: 31914.785 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  Rhodospirillum rubrum (バクテリア) Rhodospirillum rubrum (バクテリア)遺伝子: nifH, Rru_A0795 / 発現宿主:  Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW96, nitrogenase Rhodobacter capsulatus (バクテリア) / 株 (発現宿主): B10S / 参照: UniProt: Q2RW96, nitrogenase |
-非ポリマー , 6種, 9分子 







| #4: 化合物 | ChemComp-S5Q / | ||||||
|---|---|---|---|---|---|---|---|
| #5: 化合物 | ChemComp-CLF / | ||||||
| #6: 化合物 | | #7: 化合物 | #8: 化合物 | #9: 化合物 | ChemComp-SF4 / | |
-詳細
| 研究の焦点であるリガンドがあるか | Y |
|---|---|
| Has protein modification | N |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Methylthio-alkane reductase complex / タイプ: COMPLEX / 詳細: 1:1 complex of catalytic core and reductase dimer / Entity ID: #1-#3 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.28 MDa / 実験値: YES |
| 由来(天然) | 生物種:  Rhodospirillum rubrum (バクテリア) Rhodospirillum rubrum (バクテリア) |
| 由来(組換発現) | 生物種:  Rhodobacter capsulatus (バクテリア) / 株: B10S Rhodobacter capsulatus (バクテリア) / 株: B10S |
| 緩衝液 | pH: 7.8 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | グリッドのタイプ: C-flat-2/1 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE-PROPANE / 湿度: 100 % / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: TFS KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1000 nm |
| 撮影 | 電子線照射量: 50 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.71 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 116370 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / 空間: REAL | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | Source name: AlphaFold / タイプ: in silico model |
 ムービー
ムービー コントローラー
コントローラー



 PDBj
PDBj