[English] 日本語
 Yorodumi
Yorodumi- PDB-8vhe: Crystal Structure of Human IDH1 R132Q in Complex with NADPH-TCEP ... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 8vhe | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Title | Crystal Structure of Human IDH1 R132Q in Complex with NADPH-TCEP Adduct | |||||||||
 Components Components | Isocitrate dehydrogenase [NADP] cytoplasmic | |||||||||
 Keywords Keywords | OXIDOREDUCTASE | |||||||||
| Function / homology |  Function and homology information Function and homology informationAbnormal conversion of 2-oxoglutarate to 2-hydroxyglutarate / NADPH regeneration / regulation of phospholipid catabolic process / regulation of phospholipid biosynthetic process / NFE2L2 regulating TCA cycle genes / isocitrate metabolic process / NADPH regeneration / isocitrate dehydrogenase (NADP+) / isocitrate dehydrogenase (NADP+) activity / NADP+ metabolic process ...Abnormal conversion of 2-oxoglutarate to 2-hydroxyglutarate / NADPH regeneration / regulation of phospholipid catabolic process / regulation of phospholipid biosynthetic process / NFE2L2 regulating TCA cycle genes / isocitrate metabolic process / NADPH regeneration / isocitrate dehydrogenase (NADP+) / isocitrate dehydrogenase (NADP+) activity / NADP+ metabolic process / 2-oxoglutarate metabolic process / glyoxylate cycle / response to steroid hormone / female gonad development / peroxisomal matrix / tricarboxylic acid cycle / glutathione metabolic process / Peroxisomal protein import / NAD binding / NADP binding / tertiary granule lumen / peroxisome / response to oxidative stress / secretory granule lumen / ficolin-1-rich granule lumen / cadherin binding / Neutrophil degranulation / magnesium ion binding / protein homodimerization activity / mitochondrion / extracellular exosome / extracellular region / identical protein binding / cytoplasm / cytosol Similarity search - Function | |||||||||
| Biological species |  Homo sapiens (human) Homo sapiens (human) | |||||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 2.16 Å MOLECULAR REPLACEMENT / Resolution: 2.16 Å | |||||||||
 Authors Authors | Mealka, M. / Sohl, C.D. / Huxford, T. | |||||||||
| Funding support |  United States, 2items United States, 2items
| |||||||||
 Citation Citation |  Journal: Nat Commun / Year: 2024 Journal: Nat Commun / Year: 2024Title: Active site remodeling in tumor-relevant IDH1 mutants drives distinct kinetic features and potential resistance mechanisms. Authors: Mealka, M. / Sierra, N.A. / Avellaneda Matteo, D. / Albekioni, E. / Khoury, R. / Mai, T. / Conley, B.M. / Coleman, N.J. / Sabo, K.A. / Komives, E.A. / Bobkov, A.A. / Cooksy, A.L. / Silletti, ...Authors: Mealka, M. / Sierra, N.A. / Avellaneda Matteo, D. / Albekioni, E. / Khoury, R. / Mai, T. / Conley, B.M. / Coleman, N.J. / Sabo, K.A. / Komives, E.A. / Bobkov, A.A. / Cooksy, A.L. / Silletti, S. / Schiffer, J.M. / Huxford, T. / Sohl, C.D. | |||||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  8vhe.cif.gz 8vhe.cif.gz | 816 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb8vhe.ent.gz pdb8vhe.ent.gz | Display |  PDB format PDB format | |
| PDBx/mmJSON format |  8vhe.json.gz 8vhe.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/vh/8vhe https://data.pdbj.org/pub/pdb/validation_reports/vh/8vhe ftp://data.pdbj.org/pub/pdb/validation_reports/vh/8vhe ftp://data.pdbj.org/pub/pdb/validation_reports/vh/8vhe | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  8vh9C  8vhaC  8vhbC  8vhcC  8vhdC C: citing same article ( |
|---|---|
| Similar structure data | Similarity search - Function & homology  F&H Search F&H Search |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||||||
| 2 | 
| ||||||||||||
| Unit cell |
|
- Components
Components
-Protein , 1 types, 4 molecules ABCD
| #1: Protein | Mass: 48500.117 Da / Num. of mol.: 4 / Mutation: R132Q Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Homo sapiens (human) / Gene: IDH1, PICD / Production host: Homo sapiens (human) / Gene: IDH1, PICD / Production host:  References: UniProt: O75874, isocitrate dehydrogenase (NADP+) |
|---|
-Non-polymers , 6 types, 957 molecules 


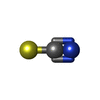





| #2: Chemical | ChemComp-A1AAX / Mass: 995.606 Da / Num. of mol.: 4 / Source method: obtained synthetically / Formula: C30H45N7O23P4 / Feature type: SUBJECT OF INVESTIGATION #3: Chemical | ChemComp-GOL / #4: Chemical | ChemComp-CL / #5: Chemical | ChemComp-CA / #6: Chemical | #7: Water | ChemComp-HOH / | |
|---|
-Details
| Has ligand of interest | Y |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.63 Å3/Da / Density % sol: 53.15 % |
|---|---|
| Crystal grow | Temperature: 277.15 K / Method: vapor diffusion, hanging drop / pH: 7.4 / Details: 200 mM KSCN, 24% (w/v) PEG 6000, and 5 mM TCEP |
-Data collection
| Diffraction | Mean temperature: 100 K / Serial crystal experiment: N |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  APS APS  / Beamline: 24-ID-E / Wavelength: 0.97918 Å / Beamline: 24-ID-E / Wavelength: 0.97918 Å |
| Detector | Type: DECTRIS EIGER X 16M / Detector: PIXEL / Date: Jun 30, 2021 |
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 0.97918 Å / Relative weight: 1 |
| Reflection | Resolution: 2.16→108.53 Å / Num. obs: 101627 / % possible obs: 98.01 % / Redundancy: 3 % / Biso Wilson estimate: 34.07 Å2 / CC1/2: 0.992 / Net I/σ(I): 13 |
| Reflection shell | Resolution: 2.16→2.18 Å / Num. unique obs: 1247 / CC1/2: 0.835 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT / Resolution: 2.16→108.53 Å / SU ML: 0.2405 / Cross valid method: FREE R-VALUE / σ(F): 1.35 / Phase error: 23.3775 MOLECULAR REPLACEMENT / Resolution: 2.16→108.53 Å / SU ML: 0.2405 / Cross valid method: FREE R-VALUE / σ(F): 1.35 / Phase error: 23.3775 Stereochemistry target values: GeoStd + Monomer Library + CDL v1.2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.1 Å / Solvent model: FLAT BULK SOLVENT MODEL | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 39.75 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 2.16→108.53 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group | Refine-ID: X-RAY DIFFRACTION
|
 Movie
Movie Controller
Controller


 PDBj
PDBj





