+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7sk9 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
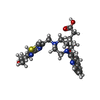
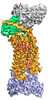
| タイトル | Cryo-EM structure of human ACKR3 in complex with a small molecule partial agonist CCX662, and an intracellular Fab | ||||||||||||||||||||||||
 要素 要素 |
| ||||||||||||||||||||||||
 キーワード キーワード | SIGNALING PROTEIN/IMMUNE SYSTEM / Atypical Chemokine Receptor / MEMBRANE PROTEIN / SIGNALING PROTEIN / SIGNALING PROTEIN-IMMUNE SYSTEM complex | ||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報oculomotor nerve development / C-X-C chemokine binding / positive regulation of mesenchymal stem cell migration / C-X-C chemokine receptor activity / scavenger receptor activity / C-C chemokine receptor activity / negative regulation of intrinsic apoptotic signaling pathway in response to DNA damage / C-C chemokine binding / chemokine-mediated signaling pathway / Chemokine receptors bind chemokines ...oculomotor nerve development / C-X-C chemokine binding / positive regulation of mesenchymal stem cell migration / C-X-C chemokine receptor activity / scavenger receptor activity / C-C chemokine receptor activity / negative regulation of intrinsic apoptotic signaling pathway in response to DNA damage / C-C chemokine binding / chemokine-mediated signaling pathway / Chemokine receptors bind chemokines / vasculogenesis / coreceptor activity / clathrin-coated pit / cell chemotaxis / calcium-mediated signaling / receptor internalization / recycling endosome / positive regulation of cytosolic calcium ion concentration / G alpha (i) signalling events / angiogenesis / early endosome / positive regulation of ERK1 and ERK2 cascade / cell adhesion / endosome / immune response / negative regulation of cell population proliferation / external side of plasma membrane / intracellular membrane-bounded organelle / cell surface / plasma membrane 類似検索 - 分子機能 | ||||||||||||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||||||||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.7 Å | ||||||||||||||||||||||||
 データ登録者 データ登録者 | Yen, Y.C. / Schafer, C.T. / Gustavsson, M. / Handel, T.M. / Tesmer, J.J.G. | ||||||||||||||||||||||||
| 資金援助 |  米国, 7件 米国, 7件
| ||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2022 ジャーナル: Sci Adv / 年: 2022タイトル: Structures of atypical chemokine receptor 3 reveal the basis for its promiscuity and signaling bias. 著者: Yu-Chen Yen / Christopher T Schafer / Martin Gustavsson / Stefanie A Eberle / Pawel K Dominik / Dawid Deneka / Penglie Zhang / Thomas J Schall / Anthony A Kossiakoff / John J G Tesmer / Tracy M Handel /    要旨: Both CXC chemokine receptor 4 (CXCR4) and atypical chemokine receptor 3 (ACKR3) are activated by the chemokine CXCL12 yet evoke distinct cellular responses. CXCR4 is a canonical G protein-coupled ...Both CXC chemokine receptor 4 (CXCR4) and atypical chemokine receptor 3 (ACKR3) are activated by the chemokine CXCL12 yet evoke distinct cellular responses. CXCR4 is a canonical G protein-coupled receptor (GPCR), whereas ACKR3 is intrinsically biased for arrestin. The molecular basis for this difference is not understood. Here, we describe cryo-EM structures of ACKR3 in complex with CXCL12, a more potent CXCL12 variant, and a small-molecule agonist. The bound chemokines adopt an unexpected pose relative to those established for CXCR4 and observed in other receptor-chemokine complexes. Along with functional studies, these structures provide insight into the ligand-binding promiscuity of ACKR3, why it fails to couple to G proteins, and its bias toward β-arrestin. The results lay the groundwork for understanding the physiological interplay of ACKR3 with other GPCRs. | ||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7sk9.cif.gz 7sk9.cif.gz | 245.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7sk9.ent.gz pdb7sk9.ent.gz | 201.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7sk9.json.gz 7sk9.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7sk9_validation.pdf.gz 7sk9_validation.pdf.gz | 953.6 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7sk9_full_validation.pdf.gz 7sk9_full_validation.pdf.gz | 960.8 KB | 表示 | |
| XML形式データ |  7sk9_validation.xml.gz 7sk9_validation.xml.gz | 31.9 KB | 表示 | |
| CIF形式データ |  7sk9_validation.cif.gz 7sk9_validation.cif.gz | 47.1 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/sk/7sk9 https://data.pdbj.org/pub/pdb/validation_reports/sk/7sk9 ftp://data.pdbj.org/pub/pdb/validation_reports/sk/7sk9 ftp://data.pdbj.org/pub/pdb/validation_reports/sk/7sk9 | HTTPS FTP |
-関連構造データ
| 関連構造データ | 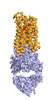 25177MC  7sk3C  7sk4C  7sk5C  7sk6C  7sk7C  7sk8C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 45196.406 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: ACKR3, CMKOR1, CXCR7, GPR159, RDC1 Homo sapiens (ヒト) / 遺伝子: ACKR3, CMKOR1, CXCR7, GPR159, RDC1発現宿主:  参照: UniProt: P25106 | ||
|---|---|---|---|
| #2: 抗体 | 分子量: 25380.223 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) Homo sapiens (ヒト)発現宿主:  | ||
| #3: 抗体 | 分子量: 23471.031 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) Homo sapiens (ヒト)発現宿主:  | ||
| #4: 化合物 | ChemComp-GJ9 / ( | ||
| #5: 化合物 | | 研究の焦点であるリガンドがあるか | Y | |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Complex structure of ACKR3-CCX662- CID24 / タイプ: COMPLEX / Entity ID: #1-#3 / 由来: MULTIPLE SOURCES | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 実験値: NO | |||||||||||||||||||||||||
| 緩衝液 | pH: 8 | |||||||||||||||||||||||||
| 緩衝液成分 |
| |||||||||||||||||||||||||
| 試料 | 濃度: 0.2 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | |||||||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R1.2/1.3 | |||||||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / Cs: 2.7 mm / C2レンズ絞り径: 100 µm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 電子線照射量: 53.8 e/Å2 / フィルム・検出器のモデル: GATAN K3 (6k x 4k) |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.19.2_4158: / 分類: 精密化 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| ||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.7 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 297347 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー




 PDBj
PDBj